





所属成套资源:2024人教版九年级化学下册精做课件
初中人教版(2024)常见的酸和碱图文ppt课件
展开 这是一份初中人教版(2024)常见的酸和碱图文ppt课件,共46页。PPT课件主要包含了学习目标,课堂导入,生活中含有碱的物质,新知探究,无色液体,易挥发,难挥发,瓶口有白雾出现,瓶口无明显现象,有刺激性气味等内容,欢迎下载使用。
1.认识常见的盐酸、硫酸,知道浓硫酸的腐蚀性及使用时的安全注意事项;2.认识酸的主要性质和用途,会书写与酸的化学性质有关的化学方程式;3.通过学习归纳酸的化学性质,知道溶液导电性的原因。
我现在需要帮用户写一个关于 “常见的酸” 的教案,用户给了很多写作素材,我得仔细看看这些素材,然后整合起来。首先,我得确定教案的结构,通常包括教学目标、教学重难点、教学过程、板书设计这些部分。用户提供的素材里有很多关于酸的性质、用途,还有中和反应、指示剂的使用等。比如摘要 1 提到新课标要求知道酸的性质和用途,会用指示剂和 pH 试纸,以及酸碱性对生命活动的影响。摘要 3 和 6 详细讲了盐酸、硫酸的物理和化学性质,比如挥发性、腐蚀性,还有它们与金属、金属氧化物、碱的反应。摘要 4 和 7 的教案结构比较完整,有导入、新课讲授、巩固提高、小结作业这些环节,可以参考。接下来,我需要把这些信息整合成一个连贯的教案。要注意不能直接照搬原文,所以得用自己的话重新组织。比如,在讲盐酸的物理性质时,素材里提到浓盐酸是无色有刺激性气味的液体,易挥发,瓶口有白雾,这些信息要转化为教案中的描述。还要注意教学方法的多样性,比如实验探究、小组讨论、多媒体展示等。比如摘要 1 里提到通过水污染的图片引入,然后进行实验探究酸碱性质,这样的情景设置可以用在导入和新课环节。摘要 5 和 8 提到用酸碱指示剂的变色实验,这部分可以设计成学生分组实验,让学生自己动手操作,观察现象,总结规律。另外,中和反应是重点,素材里多次提到要强调这部分内容,比如在工业废水处理中的应用。所以在教学过程中,需要设计一个环节专门讲解中和反应的原理和应用,可能通过生活实例,比如用熟石灰改良酸性土壤,或者用小苏打治疗胃酸过多,这样学生更容易理解。还要考虑学生的实际情况,比如他们可能对酸的腐蚀性不太了解,所以在讲浓硫酸的稀释时,要特别强调安全操作,可能用视频演示正确的稀释方法,避免学生直接操作带来的危险。摘要 8 里提到的浓硫酸稀释的动画可以作为教学资源。最后,板书设计要简洁明了,突出重点,比如酸的分类、性质、用途,以及中和反应的化学方程式。同时,作业部分可以设计一些实践性的任务,比如自制酸碱指示剂,或者调查酸雨的危害,这样能巩固课堂知识,提高学生的实践能力。现在需要检查是否有遗漏的重要信息,比如酸的命名和分类,素材 3 里提到了酸的命名方法,这部分可以放在酸的通性之前讲解。另外,不同酸的相似化学性质的原因,素材 10 提到是因为 H+,这部分需要解释清楚,可能通过导电性实验来说明。总之,整个教案需要逻辑清晰,结构合理,结合实验和生活实例,让学生在探究中学习,同时注重安全和环保意识的培养。10.2.1 常见的酸教案设计一、教学目标知识与技能认识常见酸(盐酸、硫酸等)的物理性质和化学性质。掌握酸碱指示剂的作用及使用方法,学会用 pH 试纸检验溶液的酸碱性。理解中和反应的原理及其在生产生活中的应用。过程与方法通过实验探究酸的性质,培养观察、分析和归纳能力。通过小组合作设计实验方案,提升科学探究与创新意识。情感态度与价值观体会化学与生活的密切联系,增强环保意识与社会责任感。通过实验操作,强化安全意识与严谨的科学态度。二、教学重难点重点:酸的化学性质(与指示剂、金属、金属氧化物、碱的反应)、中和反应的应用。难点:酸具有相似化学性质的原因(H⁺的存在)、中和反应的微观理解。三、教学过程1. 情境导入(5 分钟)图片展示:呈现酸雨腐蚀建筑物、实验室废水处理的新闻报道,引发学生思考酸的腐蚀性及其与生活的联系。提问互动:“生活中哪些物质含有酸?它们有什么共同特点?”(如食醋、柠檬、碳酸饮料等)“酸为何会有腐蚀性?如何安全使用酸?”2. 新课讲授(1)常见酸的物理性质(10 分钟)实验观察:展示浓盐酸、浓硫酸的试剂瓶,引导学生观察颜色、状态,闻气味(注意安全操作)。盐酸:无色液体,有刺激性气味,易挥发(瓶口出现白雾)。硫酸:无色黏稠液体,不易挥发,具有吸水性(可作干燥剂)。生活应用:结合图片讲解酸的用途(如盐酸除锈、硫酸用于蓄电池、硝酸制造化肥等)。(2)酸的化学性质(15 分钟)活动探究 1:酸与指示剂作用学生分组实验:向白醋、稀盐酸中滴加紫色石蕊试液和无色酚酞试液,观察现象并记录。结论:酸能使紫色石蕊变红,酚酞不变色。活动探究 2:酸与金属反应演示实验:镁条、锌粒、铁钉分别与稀盐酸反应,对比反应剧烈程度。化学方程式:Mg+2HCl→MgCl 2 +H 2 ↑(强调铁与酸反应生成亚铁盐)活动探究 3:酸与金属氧化物反应演示实验:生锈铁钉与稀盐酸反应,观察铁锈溶解、溶液变黄。应用:工业除锈(盐酸或硫酸)。活动探究 4:酸与碱的中和反应实验设计:向氢氧化钠溶液中滴加酚酞,逐滴加入稀盐酸至红色褪去,分析反应实质。微观解释:H + +OH − →H 2 O。(3)酸的通性与分类(5 分钟)归纳总结:酸的化学性质相似,因解离时均产生 H⁺。分类命名:根据酸根离子命名(如盐酸、硫酸、硝酸等)。3. 巩固提高(10 分钟)案例分析:实验室废水需处理后排放,如何中和酸性废水?(加入熟石灰)胃酸过多时,为何可用含氢氧化铝的药物缓解?小组讨论:设计实验鉴别稀盐酸和食盐水(提示:指示剂、活泼金属、碳酸盐等)。4. 课堂小结与作业(5 分钟)小结:通过思维导图梳理酸的性质、用途及中和反应的应用。作业:完成教材习题,总结盐酸与硫酸的异同点。查阅资料:酸雨的成因与危害,提出防治建议。
“酸”一词从有酸味的酒延伸而来。很早以前,在制酒的时候,会把比较珍贵的酒放在窖中保存,在微生物的作用下,产生了酸。
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴、印染等。
知识点1 几种常见的酸
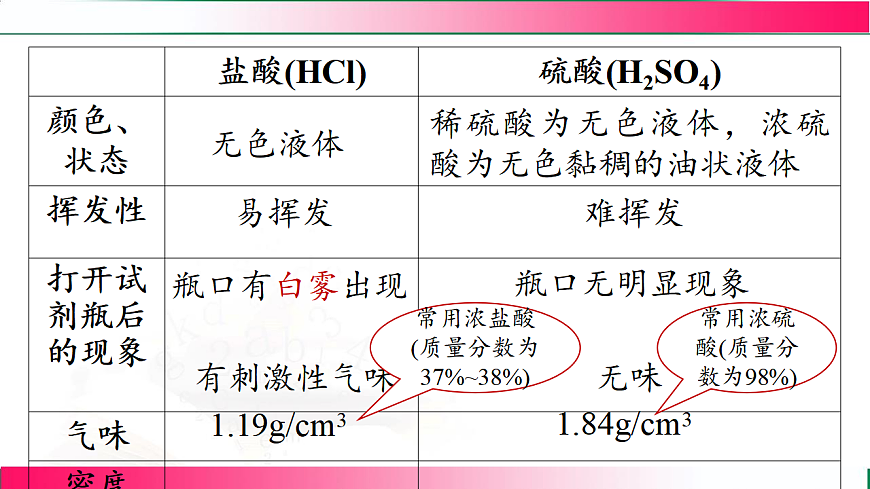
稀硫酸为无色液体,浓硫酸为无色黏稠的油状液体
常用浓盐酸(质量分数为37%~38%)
常用浓硫酸(质量分数为98%)
1.盐酸具有挥发性,浓度越大、温度越高,挥发性越强。2.浓盐酸易挥发,打开瓶盖,瓶口出现白雾,这是由于挥发出来的氯化氢气体与空气中的水蒸气结合,又形成了盐酸小液滴。
浓硫酸具有吸水性,可用作干燥剂,用来干燥不能与其反应的酸性或中性气体,如CO2、HCl、O2、H2等。 稀硫酸无吸水性,不能用作干燥剂。
敞口放置在空气中的浓盐酸和浓硫酸的比较
滴有浓硫酸的部位变黑甚至烧成洞
浓硫酸具有强烈的腐蚀性,能夺取含碳、氢、氧等元素组成的化合物里的水分(氢、氧元素), 生成黑色的炭
浓硫酸具有强烈的腐蚀性。它能将纸张、木材、布料、皮肤里的氢、氧元素按水的组成比脱去,生成黑色的炭。
都由含碳、氢、氧等元素的化合物组成
这种作用通常叫脱水作用。脱水性属于化学性质。
如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液。
酸入水,慢慢倒,沿器壁,不断搅,护目镜,要戴好。
1.稀释浓硫酸应在烧杯中进行,不可以在量筒中直接稀释浓硫酸。2.若是稀硫酸沾到皮肤或衣服上,也应立即用大量水冲洗,因为时间一长,水分蒸发后,稀硫酸也会变成浓硫酸,仍会有很强的腐蚀性。
(1)在实验室和化工生产中常用的酸还有硝酸(HNO3)、醋酸(CH3COOH)等。(2)生活中常见的许多物质中也含有酸。如洁厕灵中含有盐酸,柠檬、柑橘等水果中含有柠檬酸,铅酸蓄电池中含有硫酸等。
典例1 下列说法错误的是( )A.浓硫酸能干燥氢气B.稀释浓硫酸时玻璃棒的作用是搅拌散热C.稀盐酸和稀硫酸都可用于实验室制二氧化碳D.浓硫酸沾到皮肤上,用大量水冲洗后涂3%~5%的碳酸氢钠溶液
解析:稀硫酸与石灰石反应生成的硫酸钙微溶于水,覆盖在石灰石的表面,阻止反应的进行。
在学习盐酸、硫酸之后我们发现它们存在一些相似的性质。酸都有什么通性呢?
知识点2 酸的化学性质
酸能使紫色石蕊溶液变红,不能使无色酚酞溶液变色。
优点:操作简单、节约试剂、便于对照、效果较好。
上述实验也可以在点滴板上进行,想一想用点滴板进行实验有什么优点?
剧烈反应,有大量气泡产生
反应较快,有大量气泡产生
有气泡缓慢产生,溶液由无色变为浅绿色
Mg + 2HCl MgCl2 + H2↑Mg + H2SO4 MgSO4 + H2↑
Zn + 2HCl ZnCl2 + H2↑Zn + H2SO4 ZnSO4 + H2↑
Fe + 2HCl FeCl2 + H2↑Fe + H2SO4 FeSO4 + H2↑
想一想,为什么不可将醋放在铁锅中长时间烹调,不可用铝制品调拌要放醋的凉菜?
因为食醋中含有醋酸,能与铁、铝发生化学反应。
Fe2O3+3H2SO4 Fe2(SO4) 3+3H2O
铁锈逐渐消失,铁钉变得光亮,溶液由无色变为黄色
Fe2O3 + 6HCl 2FeCl3 + 3H2O
1.这两个反应的生成物之一都是水,另一生成物是由金属离子和酸根离子构成的化合物。2.利用酸可以清除铁制品表面的锈,但不能将铁制品长时间浸在足量的酸中,因为酸会继续与铁反应,造成铁制品的腐蚀。
通过以上几个实验的现象与结论,你能总结出酸的通性吗?
1. [2023•辽阳]浓盐酸敞口放置时能闻到刺激性气味,这说明浓盐酸具有的性质是( )A. 挥发性 B. 腐蚀性 C. 吸水性 D. 酸性
【点拨】浓盐酸敞口放置时能闻到刺激性气味,这说明浓盐酸具有挥发性,从浓盐酸中挥发出来的氯化氢气体具有刺激性气味。
2. [2024•北京海淀区模拟]浓硫酸暴露在空气中,质量会增加,是因为浓硫酸具有( )A. 酸性 B. 碱性 C. 吸水性 D. 腐蚀性
【点拨】浓硫酸具有吸水性,暴露在空气中,会吸收空气中的水蒸气,导致溶液质量增加。
3. 下列有关盐酸和硫酸的叙述正确的是( )A. 打开盛浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾B. 浓盐酸和浓硫酸都能用作干燥剂C. 浓盐酸和浓硫酸敞口放置一段时间,溶质质量分数都会变小D. 浓硫酸不慎沾在皮肤上,先用大量水冲洗,再涂上3%~5%的NaOH溶液
【点拨】浓硫酸不具有挥发性,瓶口没有白雾,A错误;浓盐酸不具有吸水性,不能作干燥剂,B错误;浓盐酸具有挥发性,挥发出溶质氯化氢气体,溶质的质量分数减小,浓硫酸具有吸水性,溶液中溶剂的质量增加,溶质质量不变,溶质的质量分数也减小,C正确;浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液,D错误。
【点易错】解答此类题目应明确酸暴露在空气中发生的变化:(1)浓盐酸易挥发,露置在空气中溶质质量减小,溶质质量分数减小。(2)浓硫酸具有吸水性,露置在空气中,溶剂的质量增大,溶质的质量分数减小。
4. 在配制稀硫酸并制备氢气的实验中,下列装置和操作正确并规范的是( )
【点拨】倾倒液体试剂时,量筒应倾斜,瓶塞应倒放,标签要向着手心,A错误;稀释浓硫酸时,应将浓硫酸沿器壁缓慢地注入水中,不能将水注入浓硫酸中,B错误;制取氢气时,长颈漏斗的下端管口要伸入液面以下,防止生成的氢气从长颈漏斗口逸出,C错误。
5. 某同学在实验室用浓硫酸配制100 g质量分数为9. 8%的稀硫酸。他查阅资料得知:常用浓硫酸的质量分数为98. 3%,其密度为1. 84 g•cm-3。浓硫酸是一种高沸点、难挥发的强酸,具有强烈的腐蚀性,能以任意比与水混溶,加水稀释后可以得到稀硫酸。请回答:
(1)通过计算,需量取5. 4 mL浓硫酸,选择量筒________ (填“A”或“B”)量取。(2)若完成溶液的配制,除图中所提供的仪器外,还需用到的玻璃仪器是________,浓硫酸稀释时应将________(填“a”或“b”)中。a. 水注入浓硫酸 b. 浓硫酸注入水(3)若用量筒量取浓硫酸时俯视读数,则所配溶液溶质质量分数________(填“大于”“小于”或“等于”)9. 8%。
【点拨】(1)量筒量程选择的依据有两点:一是尽量保证一次量取,二是量程与液体的取用量最接近,量取5. 4 mL的浓硫酸,应选择10 mL的量筒。(2)用浓硫酸配制一定溶质质量分数的稀硫酸,配制步骤有计算、量取(量筒和胶头滴管)、稀释(烧杯、玻璃棒)等操作,所以还需要的玻璃仪器为玻璃棒;稀释浓硫酸时,要把浓硫酸沿器壁缓缓地注入水中,同时用玻璃棒不断搅拌,以使热量及时扩散。(3)若用量筒量取浓硫酸时俯视读数,读数偏大,则实际量取的浓硫酸的体积偏小,则所配溶液溶质质量分数小于9. 8%。
6. 如果有两瓶失去标签的浓盐酸和浓硫酸,你有什么方法可以将两者区分开?(至少写两种方法) (1)________________________________________________________________________________________________。(2)________________________________________________________________________________________________________________________________________________________________________________________________。
分别打开瓶塞,瓶口上方有白雾出现的是浓盐酸,无明显现象的是浓硫酸
分别用小木条蘸取待测液,一段时间后小木条变黑的是浓硫酸,无明显变化的是浓盐酸(或分别打开瓶塞,用手在瓶口轻轻扇动,闻到刺激性气味的是浓盐酸,无明显气味的是浓硫酸,其他方法合理即可)
7. 下列物质都是常见的酸,它们在国民生产及我们的日常生活中有着十分重要的应用。请用序号填空。①硫酸 ②盐酸 ③碳酸 ④醋酸 ⑤柠檬酸(1)柠檬、柑橘中含有的酸是________。(2)食醋中含有的酸是________。(3)用于精炼石油的是________。(4)汽水中大量含有的一种酸是________。(5)存在于人体胃液中,可帮助消化的酸是________。(6)汽车铅蓄电池中含有的酸是________。
石蕊溶液遇酸变红色酚酞溶液遇酸不变色
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 










