










所属成套资源:【核心素养目标】2024人教版九年级化学下册课件(含视频)+同步分层练习+教学设计(含教学反思))
化学九年级下册(2024)第十单元 常见的酸、碱、盐课题2 常见的酸和碱完美版教学ppt课件
展开这是一份化学九年级下册(2024)第十单元 常见的酸、碱、盐课题2 常见的酸和碱完美版教学ppt课件,文件包含核心素养课题2第2课时《常见的酸和碱》课件PPTpptx、核心素养课题2第2课时《常见的酸和碱》教学设计含答案和教学反思docx、核心素养课题2第2课时《常见的酸和碱》同步练习docx等3份课件配套教学资源,其中PPT共27页, 欢迎下载使用。
本资料由本人原创编写,下载请自行使用不得转载、分享、售卖,一旦发现侵权,本公司将联合司法机关获取相关用户信息并要求侵权者承担相关法律责任。请尊重本人的劳动成果,谢谢配合!
1.了解并记住金属活动性顺序,并能用它来判断某金属与酸能否发生置换反应,掌握酸与金属氧化物的反应。2.通过对盐酸、稀盐酸化学性质的学习,概括出酸的通性,培养学生的比较、归纳能力,通过对金属活动顺序的应用,培养学生分析和解决问题的能力。3.通过对酸的通性的学习,使学生逐渐懂得从个别到一般认识事物的过程,建立个性与共性的辩证关系。
工人师傅在电焊时,通常先用稀盐酸或稀硫酸对焊接面进行清洗,以使焊接后的接头更牢固。为什么用稀盐酸、稀硫酸清洗而不用水清洗呢?
【问题与预测】(1)结合课题1的内容,预测稀盐酸、稀硫酸能使石蕊溶液和酚酞溶液分别呈现什么颜色。(2)稀盐酸和稀硫酸是否具有相似的化学性质?【实验与分析】
无色酚酞遇浓氨水变红色
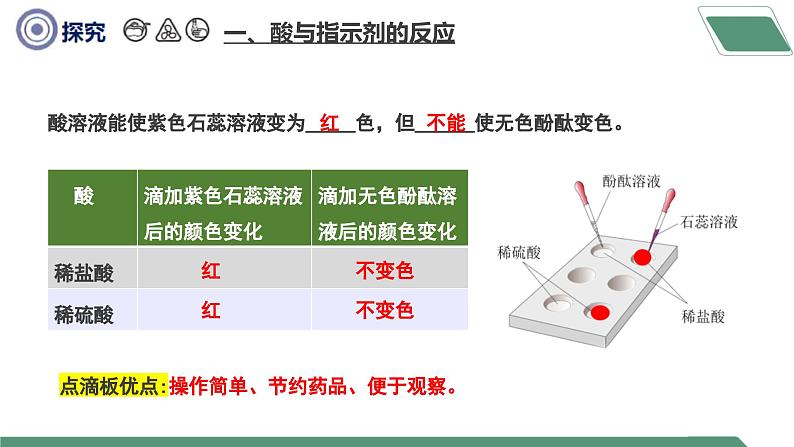
酸溶液能使紫色石蕊溶液变为_____色,但______使无色酚酞变色。
点滴板优点:操作简单、节约药品、便于观察。
二、酸与活泼金属的反应
1.这四种金属都能与盐酸反应吗?答: Cu不可以,排在H之后2.能反应的金属,反应剧烈程度一样吗?答:不一样,Mg>Zn>Fe3.什么是活泼金属?答:排在氢之前
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
氢前面的金属(K、Ca、Na除外)可以置换出酸(盐酸硫酸)中的氢。K、Ca、Na三种金属非常活泼,它们不是与酸反应,而是与水反应。
Mg +2HCl = MgCl2 + H2↑
Zn +2HCl = ZnCl2 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Fe + H2SO4 = FeSO4 + H2↑
Fe +2HCl = FeCl2 + H2↑
剧烈反应,产生大量气泡。
产生大量气泡,速度适中
产生气泡缓慢,溶液由无色变为浅绿色。
【结论】:酸 +活泼金属 → 盐 + 氢气
【分析】:以上反应的生成物有什么共同之处?
1.共同现象是:金属逐渐溶解,并产生气泡。2.含有Fe2+的溶液显浅绿色。铁与酸反应还会看到溶液由无色逐渐变为浅绿色。3.实验室用锌和稀盐酸或者稀硫酸制取氢气,反应速率适中便于控制。
为什么不可将醋放在铁锅中长时间烹调,不可用铝制品调拌要放醋的凉菜?
因为食醋中含有醋酸,能与铁、铝发生化学反应。
硫酸厂有一辆运输过浓硫酸的铁罐车(常温下,浓硫酸使铁表面生成一层致密的氧化膜,阻止铁与浓硫酸进一步反应),某新上岗的工人违反操作规定,边吸烟边用水冲洗该铁罐车,结果发生了爆炸事故。
浓硫酸在冲洗过程中变为稀硫酸和铁发生化学反应生成氢气,氢气是可燃性气体,遇到明火发生了爆炸。
现有两瓶未贴标签的稀盐酸和氯化钠溶液,如何区分?(温馨提示:氯化钠溶液呈中性。)
取溶液于试管中滴入紫色石蕊溶液,变红的溶液是稀盐酸,不变色的溶液是氯化钠溶液。取溶液于试管中加入铁钉,如果有气泡产生的是稀盐酸,无现象的是氯化钠溶液。
能否用同样的方法区别稀硫酸和硫酸钠溶液,为什么?
三、酸与金属氧化物的反应
铁钉表面的铁锈溶解,溶液变为黄色
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
黑色固体溶解,溶液由无色变为蓝色
CuO+2HCl=CuCl2+H2O
CuO+H2SO4=CuSO4+H2O
【结论】:酸 +金属氧化物 → 盐 + 水
利用上面的反应可以清除铁制品表面的锈,除锈时能否将铁制品长时间浸在酸中?为什么?观察到的现象是什么?
答:不能,铁锈被除去后,酸能和铁继续反应,造成铁被腐蚀。实验现象:溶液由无色变为黄色再变为浅绿色并且有气泡产生。
反应初期:酸溶液与铁锈发生了反应
铁锈消失后:酸溶液又与铁发生了反应
Fe2O3 + 6HCl = 2FeCl3+ 3H2O
Fe + 2HCl = FeCl2 + H2↑
Fe2O3+ HCl=
Fe +2HCl =
Fe2O3 +6HCl =2FeCl3 +3H2O
Fe + 2HCl = FeCl2 + H2↑
6 2 3
如图10-11所示,分别试验稀盐酸、稀硫酸、蒸馏水和乙醇的导电性(可以将小灯泡换成发光二极管)。
HCl → H+ + Cl-
H2SO4→2H+ + SO42-
酸在水溶液中都能解离出H+和酸根离子,即在不同的酸溶液中都含有相同的H+,所以酸有一些相似的性质。
1.生活中产生的污垢,常可用稀盐酸来清洗。但下列有一种污垢是不宜用稀盐酸来清洗的,它是( )A.不锈钢茶杯内的茶垢B.陶瓷水槽内的黄色铁锈斑C.保温瓶内的水垢(主要成分是CaCO3)D.长期盛放石灰水试剂瓶内壁上的白色固体
4.如图是稀硫酸与不同物质之间发生化学反应的颜色变化
(1)①处所使用的指示剂是 ;
(2)请你在编号②③处各填入一种物质。②是 ;③是 ;
(3)反应②涉及的基本反应类型是 ;
(4)如果想要得到黄色溶液,那么有稀硫酸参与反应的方程式 。
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
课题2第2课时常见的酸和碱
①酸能使紫色石蕊试液变红②酸使无色酚酞试液不变色
酸+活泼金属→盐+氢气
酸+金属氧化物→盐+水
1.练习与应用2.同步练习
相关课件
这是一份人教版(2024)九年级下册(2024)课题2 常见的酸和碱获奖教学ppt课件,文件包含核心素养课题2第5课时《常见的酸和碱》课件PPTpptx、核心素养课题2第5课时《常见的酸和碱》教学设计含答案和教学反思docx、核心素养课题2第5课时《常见的酸和碱》同步练习docx等3份课件配套教学资源,其中PPT共25页, 欢迎下载使用。
这是一份初中化学人教版(2024)九年级下册(2024)课题2 常见的酸和碱完整版教学课件ppt,文件包含核心素养课题2第4课时《常见的酸和碱》课件PPTpptx、核心素养课题2第4课时《常见的酸和碱》教学设计含答案和教学反思docx、核心素养课题2第4课时《常见的酸和碱》同步练习docx等3份课件配套教学资源,其中PPT共21页, 欢迎下载使用。
这是一份初中化学人教版(2024)九年级下册(2024)课题2 常见的酸和碱公开课教学ppt课件,文件包含核心素养课题2第3课时《常见的酸和碱》课件PPTpptx、核心素养课题2第3课时《常见的酸和碱》教学设计含答案和教学反思docx、核心素养课题2第3课时《常见的酸和碱》同步练习docx等3份课件配套教学资源,其中PPT共24页, 欢迎下载使用。














