




2024九年级化学上册第1章物质及其变化第3节常见的酸第1课时盐酸习题课件浙教版
展开
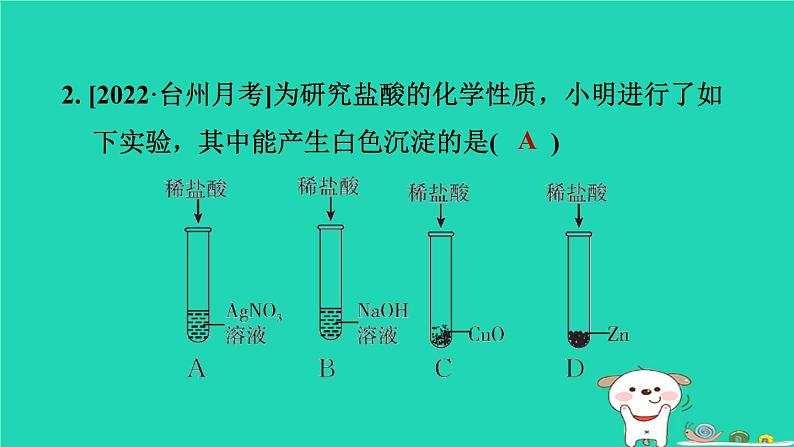
这是一份2024九年级化学上册第1章物质及其变化第3节常见的酸第1课时盐酸习题课件浙教版,共33页。
浙教版九年级上册第1章 物质及其变化1.3.1 盐酸1. 下列关于盐酸的用途中,不能用稀硫酸代替的是( )A. 制氢气 B. 除铁锈C. 制二氧化碳 D. 溶解氧化铜【点拨】实验室制二氧化碳要用石灰石(或大理石)与稀盐酸,不能用稀硫酸,因为稀硫酸与碳酸钙反应生成的硫酸钙微溶于水,会覆盖在石灰石(或大理石)表面,阻止反应的进行。C2. [2022·台州月考]为研究盐酸的化学性质,小明进行了如下实验,其中能产生白色沉淀的是( )A3. [2022·金华期中]实验室中一瓶浓盐酸敞口放置一定时间,下列四幅图中,能正确反映其变化关系的是( )A4. 稀盐酸是化学实验中常用的试剂,但下列实验中不宜使用稀盐酸的是( )A. 除去氯化钠溶液中的碳酸钠 B. 除去铜粉中混有的铁粉 C. 除去氧化钙中的石灰石D. 除去铁丝上的铁锈C5. [2022·杭州改编]氯化氢(HCl)是极易溶于水的无色气体,其水溶液称为盐酸。(1)在充满HCl气体的试管中放入用石蕊试液染成紫色的干燥纸条,无明显现象;再滴入水,现象是_____________________。紫色的纸条变为红色(2)向盛有NaOH溶液的试管中通入HCl气体,直至溶液的PH=7,反应前后溶液中离子的种类如图所示,其中能使酚酞试液变红的是________(填“①”“②”或“③”)。②6. 观察和实验是学习科学的两种基本方法。请回答下列问题:(1)打开盛有浓盐酸的试剂瓶的瓶盖,瓶口会看到________,这是挥发出来的氯化氢气体与空气中的水蒸气结合形成的盐酸小液滴。(2)将鸡蛋放入盛有稀盐酸的烧杯中,发现蛋壳(主要成分是CaCO3)表面有_______________。白雾气泡产生 (3)将一枚生锈的铁钉(主要成分是Fe2O3)放入试管中。①滴入足量稀盐酸,观察到的现象是______________________________________,反应的化学方程式为_________________________________。 ②当铁锈消失后,铁钉表面产生气泡,产生此现象的原因是_______________________(用化学方程式表示)。铁锈消失,溶液由无色变为黄色Fe2O3+6HCl=== 2FeCl3+3H2OFe+2HCl=== FeCl2+H2↑7. [2023·台州]浓盐酸具有挥发性,敞口放置于空气中,溶质质量分数会变小。稀盐酸会发生同样的变化吗?某同学通过如下步骤进行探究:①取两个烧杯,各倒入40 mL 3%的稀盐酸,分别标为甲和乙;②甲密封,液体体积不变;乙敞口放置于空气中至液体体积变为20 mL(溶液密度变化忽略不计);③向甲、乙中各滴加几滴石蕊试液,再分别缓慢滴加相同溶质质量分数的氢氧化钠溶液,恰好完全反应时,消耗的氢氧化钠溶液的体积分别为30 mL、26 mL。(1)实验中“恰好完全反应”的判断依据是:溶液颜色_____________________________。恰好由红色变成紫色(2)乙烧杯中的稀盐酸敞口放置后,溶质质量分数变大,依据是_____________________________________________________________________________________________________________________________________________ (合理即可)。乙烧杯中稀盐酸的体积变为原来的一半(即甲烧杯中稀盐酸体积的一半),所消耗的氢氧化钠溶液的体积大于甲烧杯中所消耗的氢氧化钠溶液的体积的一半(3)为了确定稀盐酸敞口放置于空气中,溶质质量分数一定会变大,请简要阐述应补充的实验:_____________________________________________。换用不同溶质质量分数的稀盐酸多次重复实验【点拨】(2)甲密封,液体体积不变,为40 mL,乙敞口放置,液体体积变为20 mL,它们与氢氧化钠恰好完全反应时,消耗氢氧化钠溶液的体积分别为30 mL、26 mL,稀盐酸的体积变为原来的一半,所消耗的氢氧化钠溶液的体积大于稀盐酸的体积未变化时所消耗的氢氧化钠溶液的体积的一半,故乙烧杯中的稀盐酸敞口放置后,溶质质量分数变大。(3)为了确定稀盐酸敞口放置于空气中,溶质质量分数一定会变大,可换用不同溶质质量分数的稀盐酸多次重复实验。【点易错】敞口放置在空气中的浓盐酸,因为具有挥发性,会挥发出HCl气体,故溶质质量减小,溶剂质量不变,溶液质量减小,溶质质量分数减小。8. [2023·义乌月考]自来水生产中常通入适量氯气进行杀菌消毒,氯气与水反应的化学方程式为Cl2+H2O===HCl+HClO。市场上有一些不法商贩为牟取暴利,用自来水冒充纯净水(蒸馏水)出售。下列能用来鉴别纯净水真伪的试剂是( )A. 酚酞试液 B. 稀硫酸 C. 硝酸银溶液 D. 氢氧化钠溶液C【点拨】由题可知,自来水中含有盐酸和次氯酸两种酸性物质,其中盐酸能与硝酸银溶液反应生成氯化银白色沉淀,而纯净水中只含有水,与硝酸银溶液混合时无明显现象,可以鉴别。9. [2024·杭州期末]人体的胃壁细胞能分泌胃酸,可以帮助消化食物,但胃酸分泌过多,会导致胃部不适,可通过服用药物来治疗。(1)如图为血液、胃壁细胞和胃腔间的微粒交换示意图,其中胃壁细胞内有大量的碳酸苷酶,能催化二氧化碳与水反应。请你解释胃酸的形成过程:______________________________________________________________________________________________________________________________________________________。胃壁细胞中的碳酸苷酶催化二氧化碳与水反应,在胃壁细胞内产生大量的HCO3-和H+,Cl-从血液进入胃壁细胞,胃壁细胞中的H+和Cl-扩散进入胃腔,形成胃酸(2)抗酸药能与胃酸反应,从而治疗胃酸过多。常见的抗酸药有碳酸氢钠、氢氧化铝、氢氧化镁和碳酸钙等。①写出氢氧化铝与胃酸反应的化学方程式:_______________________________________。②胃溃疡患者若服用不合适的抗酸药,会因胃内气体压力增大而引起胃穿孔。胃溃疡患者不宜服用上述抗酸药中的___________________________。AL(OH)3+3HCl===ALCl3+3H2O碳酸氢钠、碳酸钙【点拨】(2)②碳酸氢钠、碳酸钙这两种抗酸药与胃酸反应会生成二氧化碳气体,导致胃内气体压力增大而引起胃穿孔。10. 盐酸不小心走进了有许多“食人兽”(能与盐酸发生反应的物质)的迷宫,盐酸必须避开它们,否则无法通过,请你帮助它走出迷宫。(1)用图中物质前的序号表示盐酸所走的路线:入口→________→________→________→⑨→出口。③⑤⑦(2)盐酸刚走进入口时,碰到两种阻止它前进的物质,其中一种能“吃掉”盐酸且反应前后有元素化合价发生变化,该反应的化学方程式为___________________________。(3)迷宫中潜伏着黑色的“食人兽”化合物,若盐酸遇到它,发生反应的化学方程式为__________________________。Zn+2HCl=== ZnCl2+H2↑CuO+2HCl=== CuCl2+H2O (4)迷宫中有一种污染空气的有毒气体,我们可以喷洒浓石灰水来“消灭”它,写出该反应的化学方程式:_______________________________ (提示:该有毒气体和石灰水的反应与二氧化碳和石灰水的反应类似)。(5)根据盐酸的化学性质,你认为盐酸还没有遇到哪类“食人兽”的威胁? ____________。Ca(OH)2+SO2=== CaSO3↓+H2O酸碱指示剂11. 某兴趣小组的同学在做镁条和盐酸反应的实验时,发现试管的外壁很烫,试管口出现白雾。白雾是什么呢?(1)做出猜想:猜想一:是小水滴。因为盐酸中的水受热会汽化上升,在试管口________成小水滴。猜想二:是盐酸小液滴。因为浓盐酸具有________性,可能实验中使用的盐酸浓度较大,试管口就会形成盐酸小液滴。液化挥发同学们将干燥的蓝色石蕊试纸放在内有正在反应的镁条和盐酸的试管口,试纸变红,证明猜想二正确。(2)小柯提出疑问:为什么刚打开盛放实验所用盐酸的试剂瓶时,瓶口没有白雾,却在反应过程中出现了白雾?小柯联系反应时试管外壁很烫,于是猜想:白雾的形成可能与温度有关。他用试管取少量盐酸,将干燥的蓝色石蕊试纸放在试管口,试纸不变红;然后____________________________________________(填操作),试纸变红。由此得出结论:这种盐酸的浓度并不高,是镁和盐酸反应放热促使盐酸挥发形成白雾。加热试管,将干燥的蓝色石蕊试纸放在试管口12. [2023·丽水]小科在某次家庭劳动实践时发现,厕所污垢通常用洁厕灵进行清洗,他对家里某品牌洁厕灵的有效成分及其含量进行了实验研究。查阅资料可知洁厕灵的有效成分是HCl,HCl的含量可利用NaHCO3溶液来测定,反应的化学方程式为HCl+NaHCO3===NaCl+H2O+CO2↑。洁厕灵的其他成分均不参加反应。向一个锥形瓶中加入100 g该品牌洁厕灵,再逐次加入相同溶质质量分数的NaHCO3溶液,测出每次锥形瓶中充分反应后溶液的总质量,数据记录如表。(1)该洁厕灵呈________(填“酸性”或“碱性”)。(2)第一次实验产生的气体质量为________g。(3)求该品牌洁厕灵中HCl的质量分数。酸性2. 2 解:100 g该品牌洁厕灵中的HCl能与200 g NaHCO3溶液恰好完全反应,产生CO2的质量为100 g+200 g-295. 6 g=4. 4 g。设100 g该品牌洁厕灵中HCl的质量为x。HCl+NaHCO3===NaCl+H2O+CO2↑36. 5 44 x 4. 4 g(4)下列关于家庭小实验活动的说法中,你认为合理的有________(填字母)。A. 开展家庭小实验活动时,需要规范操作B. 明白实验原理和安全事项后,有安全保障才能开展实验C. 只要网上能买到的,可随意购买药品或器材进行各类实验AB






