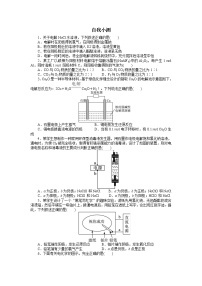
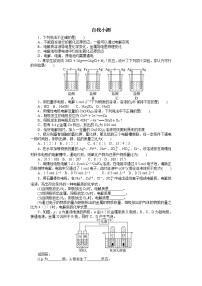
选修4 化学反应原理第三节 化学平衡第3课时同步测试题
展开A.0.24 ml·L-1 B.0.28 ml·L-1C.0.32 ml·L-1 D.0.26 ml·L-1
2.2 000 K时,反应CO(g)+O2(g) CO2(g)的平衡常数为K,则相同温度下反应2CO2(g) 2CO(g)+O2(g)的平衡常数K′为( )
A. B.K2 C. D.
3.低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g)
ΔH<0
在恒容的密闭容器中,下列有关说法正确的是( )
A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C.单位时间内消耗NO和N2的物质的量比为1∶2时,反应达到平衡
D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
4.某温度下,反应SO2(g)+O2(g) SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g) 2SO2(g)+O2(g)的平衡常数K2的值为( )
A.2 500 B.100 C.4×10-4 D.2×10-2
5.某温度下,H2(g)+CO2(g) H2O(g)+CO(g)的平衡常数K=。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
下列判断不正确的是( )
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 ml·L-1
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
6.在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y2Z,其平衡常数为1 600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.改变温度可以改变此反应的平衡常数
7.汽车尾气净化中的一个反应如下:
NO(g)+CO(g) N2(g)+CO2(g) ΔH=-373.4 kJ·ml-1
在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是( )[K表示反应平衡常数。α(CO)表示CO的转化率]
8.一定条件下,在体积为3 L的密闭容器中,CO与H2反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)。
(1)反应达到平衡时,平衡常数表达式K=______。升高温度,K值______(填“增大”“减小”或“不变”)。
(2)在500 ℃,从反应开始到平衡,H2的平均反应速率v(H2)=__________________。
(3)在其他条件不变的情况下,将处于E点的体系体积压缩到原来的,下列有关该体系的说法正确的是______。
a.H2的浓度减小
b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加
d.重新平衡时,值增大
9.高炉炼铁过程中发生的主要反应为Fe2O3(s)+CO(g) Fe(s)+CO2(g)。
已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应的平衡常数表达式K=________,ΔH________0(填“>”“<”或“=”);
(2)在一个容积为10 L的密闭容器中,1 000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 ml,反应经过10 min 后达到平衡。求该时间范围内反应的平均反应速率v(CO2)=________、CO的平衡转化率=________;
(3)欲提高(2)中CO的平衡转化率,可采取的措施是________。
A.减少Fe的量
B.增加Fe2O3的量
C.移出部分CO2
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂
参考答案
1.
解析: 2SO2(g)+O2(g) 2SO3(g)
0.4 1 0
x 0.5x x
0.4-x 1-0.5x x
由平衡常数的定义:K===19,解得x=0.32 。
答案:C
2.
解析:反应CO2(g) CO(g)+O2(g)的平衡常数K″=,反应2CO2(g) 2CO(g)+O2(g)的平衡常数K′=(K″)2=。
答案:C
3.
解析:因该反应为放热反应,故升高温度,平衡常数减小,A错误;增大一种反应物浓度,另外一种反应物的转化率必增大,B错误;使用催化剂,化学平衡不移动,转化率不变,D错误。
答案:C
4.
解析:K2=====4×10-4。
答案:C
5.
解析:依三段式:
H2 + CO2 H2O+CO
甲始态/(ml·L-1): 0.010 0.010 0 0
甲反应/(ml·L-1): x x x x
甲终态/(ml·L-1): 0.010-x 0.010-x x x
=,所以x=0.006,甲中H2的转化率为60%,乙相当于在甲的基础上又充入了H2,CO2的转化率增大,A正确;丙相当于在甲的基础上加压,平衡不移动,丙中CO2的浓度是甲中CO2浓度的2倍,甲平衡时CO2浓度为0.004 ml·L-1,B正确、C错误;B、C也可以用三段式来求解。由浓度可知D正确。
答案:C
6.
解析:题中有一明显的错误,就是C选项,增大压强不可能使平衡常数增大。A、B选项均为平衡中的基础计算和基础知识,关键是根据表中数据(0.1-0.05)∶(0.2-0.05)∶(0.1-0)=1∶3∶2可推导出该反应的化学方程式可表示为X+3Y2Z。
答案:C
7.
解析:该反应为气体体积减小的放热反应。升温,平衡逆向移动,生成物浓度减小,反应物浓度增大,平衡常数减小,同时,CO的转化率减小;平衡常数只与温度有关,与物质的量无关;增加氮气的物质的量,平衡逆向移动,CO的转化率减小。
答案:C
8.
解析:由图像可知升高温度,甲醇的物质的量减少,平衡向左移动,故正反应为放热反应。K=,升高温度,平衡左移,K减小。生成nB ml甲醇,消耗H2的物质的量为2nB,v(H2)== ml·(L·min)-1。压缩体积即增大压强,正、逆反应速率都增大,平衡右移,甲醇的物质的量增大,H2的物质的量减小,但是体积缩小,H2的浓度增大,b、c正确。
答案:(1) 减小
(2) ml·(L·min)-1
(3)bc
9.
解析:(1)注意物质的状态,随着温度升高K逐渐减小,所以此反应是放热反应。
(2)三段式:
Fe2O3(s)+CO(g) Fe(s)+CO2(g)
始态/(ml·L-1): 0.1 0.1
终态/(ml·L-1): 0.1-x 0.1+x
反应/(ml·L-1): x x
温度为1 000 ℃,所以K===4.0,所以x=0.06,v(CO2)==0.006 ml·(L·min)-1。
(3)Fe2O3、Fe均是固体,改变Fe、Fe2O3的量不影响反应速率和化学平衡,故A、B反应速率、化学平衡均不改变;C移出部分CO2,平衡右移,正确;D此反应为放热反应,升高温度,平衡左移,错误;E减小容器容积,相当于加压,平衡不移动,错误;F催化剂只影响化学反应速率,对平衡移动无影响,错误。
答案:(1) <
(2)0.006 ml·(L·min)-1 60%
(3)C
起始浓度
甲
乙
丙
c(H2)/(ml·L-1)
0.010
0.020
0.020
c(CO2)/(ml·L-1)
0.010
0.010
0.020
物质
X
Y
Z
初始浓度/(ml·L-1)
0.1
0.2
0
平衡浓度/(ml·L-1)
0.05
0.05
0.1
温度/℃
1 000
1 150
1 300
平衡常数
4.0
3.7
3.5
化学选修4 化学反应原理第三节 化学平衡第1课时综合训练题: 这是一份化学选修4 化学反应原理第三节 化学平衡第1课时综合训练题,共4页。试卷主要包含了在一密闭容器中进行反应等内容,欢迎下载使用。
高中化学人教版 (新课标)选修4 化学反应原理第三节 化学平衡第2课时测试题: 这是一份高中化学人教版 (新课标)选修4 化学反应原理第三节 化学平衡第2课时测试题,共5页。试卷主要包含了可逆反应,可用下面示意图表示的是等内容,欢迎下载使用。
高中化学人教版 (新课标)选修4 化学反应原理第三节 化学平衡一课一练: 这是一份高中化学人教版 (新课标)选修4 化学反应原理第三节 化学平衡一课一练,共15页。试卷主要包含了在密闭容器中进行如下反应,4ml·L-1,Y2为1,已知反应,下列说法正确的是,已知等内容,欢迎下载使用。