






初中化学人教版(2024)九年级下册(2024)常见的酸和碱优秀ppt课件
展开 这是一份初中化学人教版(2024)九年级下册(2024)常见的酸和碱优秀ppt课件,共59页。PPT课件主要包含了第十单元酸和碱,课题1常见的酸和碱,第一课时,常见的酸,第二课时,常见的碱,第三课时,中和反应等内容,欢迎下载使用。
“酸”一词从有酸味的酒而来。最早,在制酒的时候,有时把比较珍贵的酒放在窖中保存,在微生物的作用下,产生了酸。
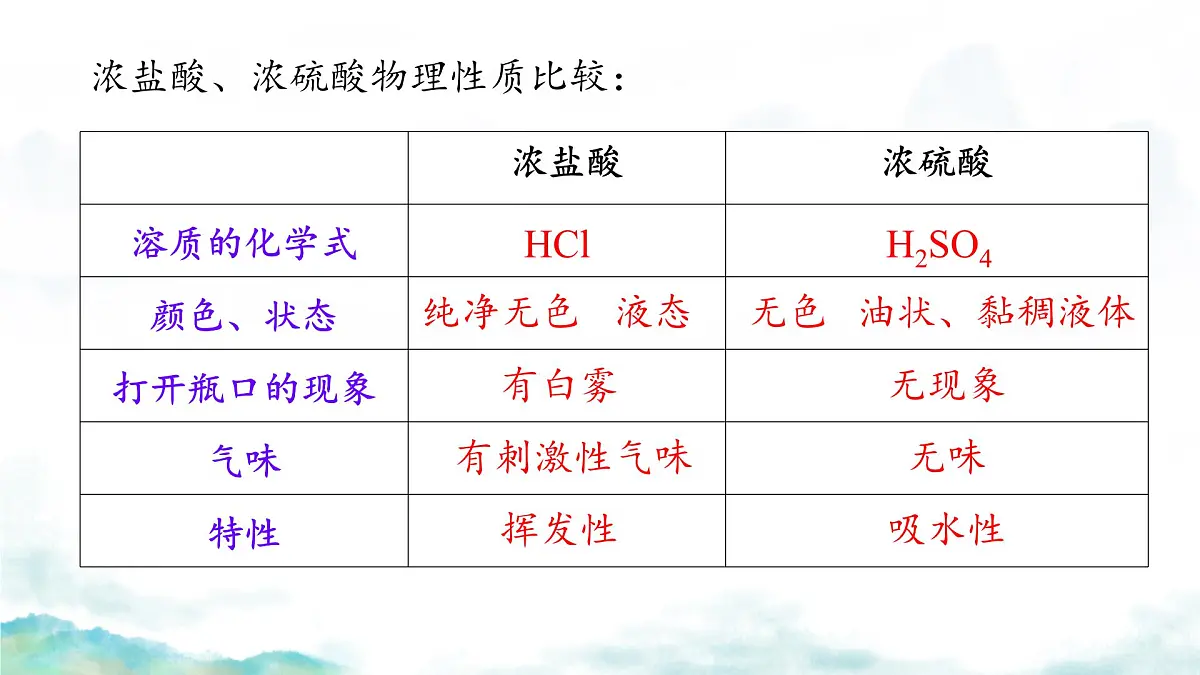
探究浓盐酸、浓硫酸的物理性质
① 观察浓盐酸、浓硫酸的颜色和状态;② 打开瓶塞,观察发生的现象,闻一闻是否有气味。
浓盐酸、浓硫酸物理性质比较:
1.浓盐酸具有挥发性,产生的白雾是什么物质?
挥发出来的HCl气体溶解在空气中的水蒸气中,形成盐酸小液滴。
2.浓硫酸具有吸水性,这属于什么性质?
3.性质决定用途,浓硫酸具有吸水性,决定着它在化学实验中可以用作 。
敞口放置在空气中的浓盐酸、浓硫酸,各成分会发生怎样的变化?
通过讨论可知: 实验室浓硫酸、浓盐酸必须 保存。
将纸张、小木棍、布片放在玻璃片上,做如下实验,观察现象。
注意:浓硫酸有很强的腐蚀性,使用时要特别小心。
浓硫酸接触到水,会放出大量的热,那应该怎样正确地稀释浓硫酸呢?
稀释时,水浮在浓硫酸上面,并迅速沸腾,液体向四周飞溅,非常危险!
稀释浓硫酸时,一定要将 沿烧杯内壁慢慢注入 中,并用玻璃棒不断搅拌。
如果不慎使浓硫酸沾到皮肤上,应该如何正确处理?为什么?
碳酸氢钠能与残留的硫酸反应(涉及到酸的化学性质)
大量水可以带走浓硫酸稀释时放出的热量
盐酸、硫酸有哪些用途呢?
②人体胃液中含有盐酸,帮助消化;
②浓硫酸吸水性,常用于做干燥剂;
① 浓硫酸一般用于气体干燥,除 外,其它气体都可以用浓硫酸干燥;
②干燥时,气体从导管 通入瓶内。
①酸能使紫色石蕊溶液变 色;
②酸 使无色酚酞溶液变色。
【性质1】酸能使指示剂变色
剧烈反应,产生大量气泡
反应规律:酸 + 活泼金属 = 盐 + 氢气
【性质2】酸与活泼金属单质反应
反应比较平缓,产生少量气泡,溶液变为浅绿色
反应比较剧烈,产生大量气泡
①红色固体消失;②溶液变为黄色;
①黑色固体消失;②溶液变为蓝色;
资料:铁锈的主要成分为氧化铁(Fe2O3),常用稀盐酸、稀硫酸清洗铁锈。
【性质3】酸与金属氧化物反应
试着写出稀盐酸和氧化铁、稀硫酸和氧化铁,两个反应的化学方程式
反应规律:酸 + 金属氧化物 = 盐 + 水
试着按照规律,写出稀硫酸和氧化镁、稀盐酸和氧化铝,两个反应的化学方程式
Fe2O3+6HCl=2FeCl3 +3H2O
CuO+H2SO4=CuSO4+H2O
性质2:酸 + 活泼金属 = 盐 + 氢气
性质1:酸能使指示剂变色
性质3:酸 + 金属氧化物 = 盐 + 水
性质5:酸 + 碱 = 盐 + 水
性质4:酸 + 盐 = 新酸 + 新盐
【讨论】为什么不同的酸化学性质相似呢?
因为酸溶于水后都会产生相同的氢离子(H+)。
1.三种常见的酸是指 、 、 ;
2.酸溶于水产生的阳离子全部是 ;
酸 = 氢离子(H+) + 酸根离子
【结论】酸、碱、盐溶液具有 。
【原因分析】酸、碱、盐溶于水产生了可以自由移动的 ,这些微粒通电后作 移动,从而使溶液导电。
如何证明酸和碱的溶液中存在离子?
1.以下关于浓盐酸或浓硫酸的说法正确的是( ) A.浓盐酸和浓硫酸都是无色无味的液体 B.打开瓶塞,浓盐酸和浓硫酸瓶口会出现白雾 C.浓盐酸和浓硫酸长期敞口放置,质量都会变小 D.浓硫酸滴到纸张、蔗糖上,会使纸张、蔗糖炭化
2.用足量的稀盐酸长时间浸泡生锈的铁钉,可观察到的实验现象是( )①铁钉上的铁锈消失;②铁钉上有气泡产生;③溶液呈黄色。A.只有①② B.只有①③ C.只有③ D.①②③
3.某同学发现实验室中有两瓶标签失落的浓酸,询问老师后只知道它们是盐酸和硫酸各一瓶。请用三种不同的方法对这两瓶酸加以鉴别。方法一:___________________________________________。方法二:_________________________________________。方法三:_________________________________________。
打开瓶塞,瓶口有白雾的是浓盐酸,没有的是浓硫酸
打开瓶塞,闻气味,有刺激性气味的是浓盐酸,无气味的是浓硫酸
用玻璃棒蘸取少量待检测的液体,滴到纸张上,纸张变黑的是浓硫酸,纸张没有变黑的是浓盐酸
你知道生活中哪些物质含有碱吗?
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴、印染等,草木灰中的K2CO3虽然不是碱,但它的溶液也是呈碱性。
氢氧化钠化学式为 ; 俗称为 、 、 。
用镊子取几块NaOH,观察氢氧化钠的颜色和状态。
由于NaOH固体在空气中易潮解,所以需要 保存。
思考:向试管内水中加入NaOH固体,U形管内红墨水的变化是 ;这一现象的原因是: 。
a端液面下降、b端液面上升
NaOH溶于水放热,气体体积膨胀
① NaOH是 色固体;
② NaOH易吸收空气中的水分而发生 ;
③ NaOH易溶于水,溶解时放出大量的 ;
事故处理:若NaOH沾到皮肤上,先用大量水冲洗,再涂上硼酸溶液。
NaOH具有强烈的腐蚀性,使用时要注意安全!
俗称为 、 。
氢氧化钙化学式为 ;
氢氧化钙 于水,且溶解度随温度升高而 。
NaOH、Ca(OH)2的重要用途
NaOH固体能否干燥HCl、CO2、SO2气体?
不能,NaOH能和这些物质反应
②无色酚酞试液遇碱变 色。
【性质1】碱使指示剂变色
①紫色石蕊试液遇碱变 色;
【性质2】碱与某些非金属氧化物反应
实验室检验CO2的化学方程式:
碱 + 非金属氧化物 = 盐 + 水
2NaOH+ CO2 = Na2CO3+H2O
2NaOH+ SO2 = Na2SO3+H2O
性质1:碱可以使指示剂变色
性质2:碱 + 非金属氧化物 = 盐 + 水
性质3:碱 + 酸 = 盐 + 水
性质4:碱 + 盐 = 新碱 + 新盐
【讨论】为什么不同的碱化学性质相似呢?
因为碱溶于水后都会产生相同的氢氧根离子 (OH-)。
1.两种常见的碱是指 、 ;
2.碱溶于水产生的阴离子全部是 ;
碱 = 金属离子 + 氢氧根离子(OH-)
1.物质的性质决定其保存方法。固体氢氧化钠具有以下性质:①白色固体;②有腐蚀性;③易吸收水分;④能与空气中的二氧化碳反应。由此可知,氢氧化钠固体必须密封保存的主要原因是( )A.①② B.②③ C.①③ D.③④
2.下列各组物质的名称或俗称和化学式表示的是同一种物质的是( )A.熟石灰、消石灰、CaOB.铁锈、氢氧化铁、Fe(OH)3C.生石灰、消石灰、Ca(OH)2D.烧碱、火碱、NaOH
【实验方案】
固体溶解,产生大量气泡
【分析】NaOH的变质,是与空气中的 发生反应,生成 ,
3.实验室有一瓶未密封保存的NaOH固体,设计实验,检验其是否变质。
取适量样品,滴加稀盐酸,若有气泡冒出,则已变质。
1.认识酸和碱之间发生的中和反应。2.知道中和反应在实际生活中的应用。
酸有相似的化学性质,碱也有相似的化学性质,那么,酸和碱之间能否发生反应呢?
用滴管向盛有5%的NaOH溶液的试管中滴加5%的稀盐酸,观察现象。
当加入一定量稀盐酸后,混合液由红色变无色
酸和碱反应,使溶液不再显碱性
经过研究发现,HCl与NaOH反应,生成NaCl和H2O
氢离子和氢氧根离子结合生成水。
氢氧化钠与盐酸反应示意图
HCl+NaOH= NaCl+H2O
氢氧化钙也是一种常见的碱,它也能和稀盐酸、稀硫酸发生反应,请你写出氢氧化钙与稀盐酸、氢氧化钠与稀硫酸反应的化学方程式,并总结酸、碱反应的特点。
2NaOH+H2SO4=Na2SO4+ 2H2O
酸都能与碱发生反应,且生成物存在一定规律。
中和反应:酸和碱作用生成盐和水的反应。
盐:由金属阳离子(或NH4+)和酸根离子结合, 构成的物质。
酸 + 碱 = 盐 + 水
1、下列对于中和反应的判断正确的是( )A.生成盐和水的反应一定是中和反应B.二氧化碳与氢氧化钠的反应是中和反应C.酸与碱反应生成的盐和水的反应是中和反应D.实验室制取二氧化碳的反应就是中和反应
2、下列关于中和反应的说法正确的是( )
A. 中和反应会放出热量B. 有盐和水生成的反应一定是中和反应C. 所有的中和反应不加指示剂都观察不到现象D. 中和反应一定可以生成水
农作物一般适宜在中性或接近中性的土壤中生长,如果土壤的酸性或碱性太强都不利于农作物的生长。
2.处理工厂的废水,解决环境问题。
Ca(OH)2+H2SO4=CaSO4+ 2H2O
由胃酸过多导致胃部不适或疼痛时可口服碱性药物,以降低胃酸的含量。
蚊虫叮咬时“注射”的蚁酸可以用含碱性物质的溶液中和,如肥皂水、稀氨水,以减轻痛痒。
相关课件
这是一份初中化学人教版(2024)九年级下册(2024)常见的酸和碱优秀ppt课件,共59页。PPT课件主要包含了第十单元酸和碱,课题1常见的酸和碱,第一课时,常见的酸,第二课时,常见的碱,第三课时,中和反应等内容,欢迎下载使用。
这是一份初中化学人教版(2024)九年级下册(2024)常见的酸和碱优秀ppt课件,共42页。PPT课件主要包含了应用与拓展等内容,欢迎下载使用。
这是一份初中化学人教版(2024)九年级下册(2024)常见的酸和碱完美版课件ppt,共29页。PPT课件主要包含了几种常见的碱,碱的化学性质等内容,欢迎下载使用。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)




