



所属成套资源:高一化学课件(苏教版2019)
专题三 从海水中获得的化学物质 第一单元 第三课时 氧化还原反应 高一化学课件(苏教版2019)
展开 这是一份专题三 从海水中获得的化学物质 第一单元 第三课时 氧化还原反应 高一化学课件(苏教版2019),共60页。
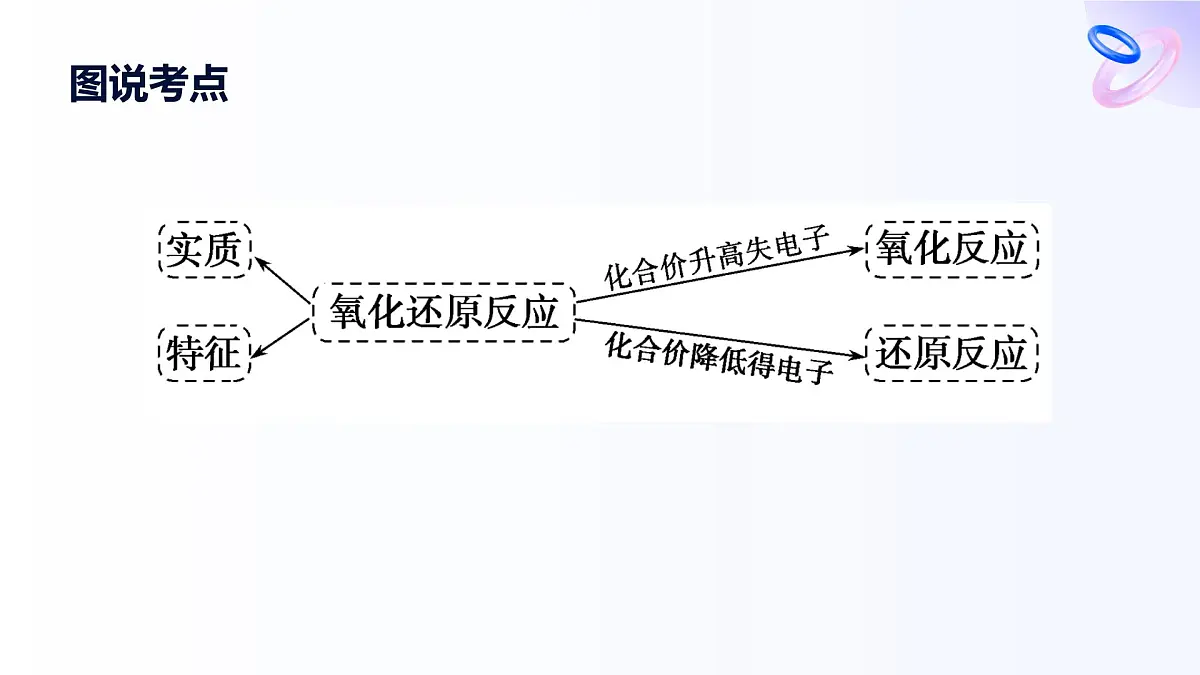
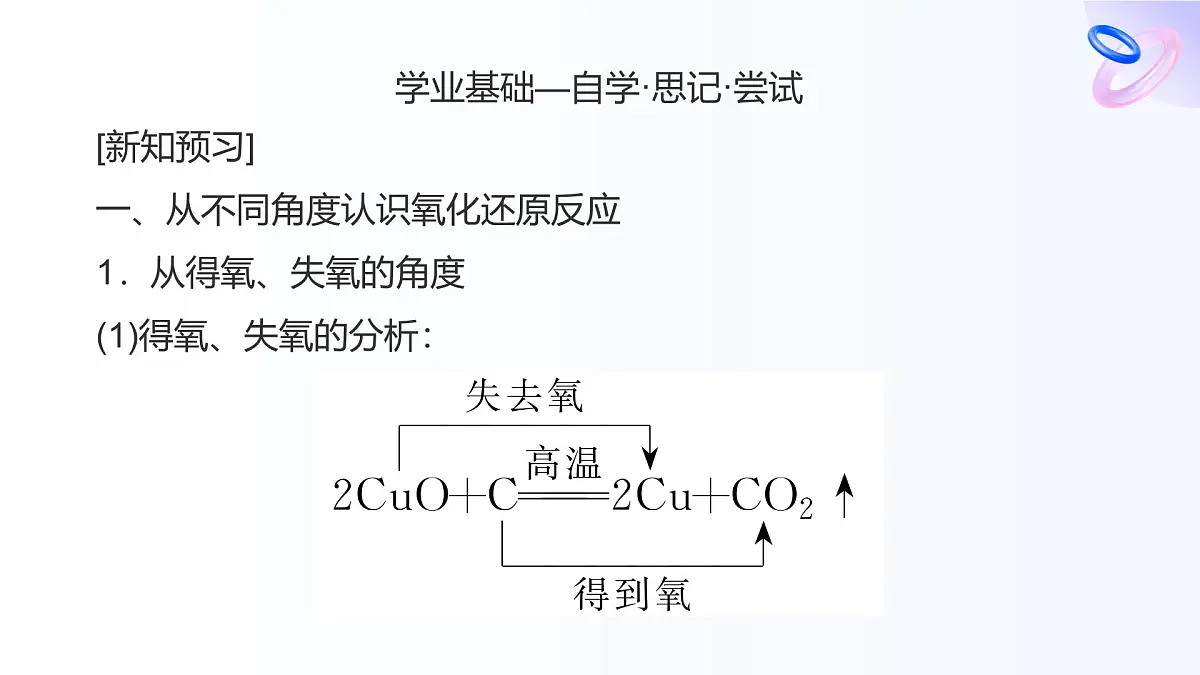
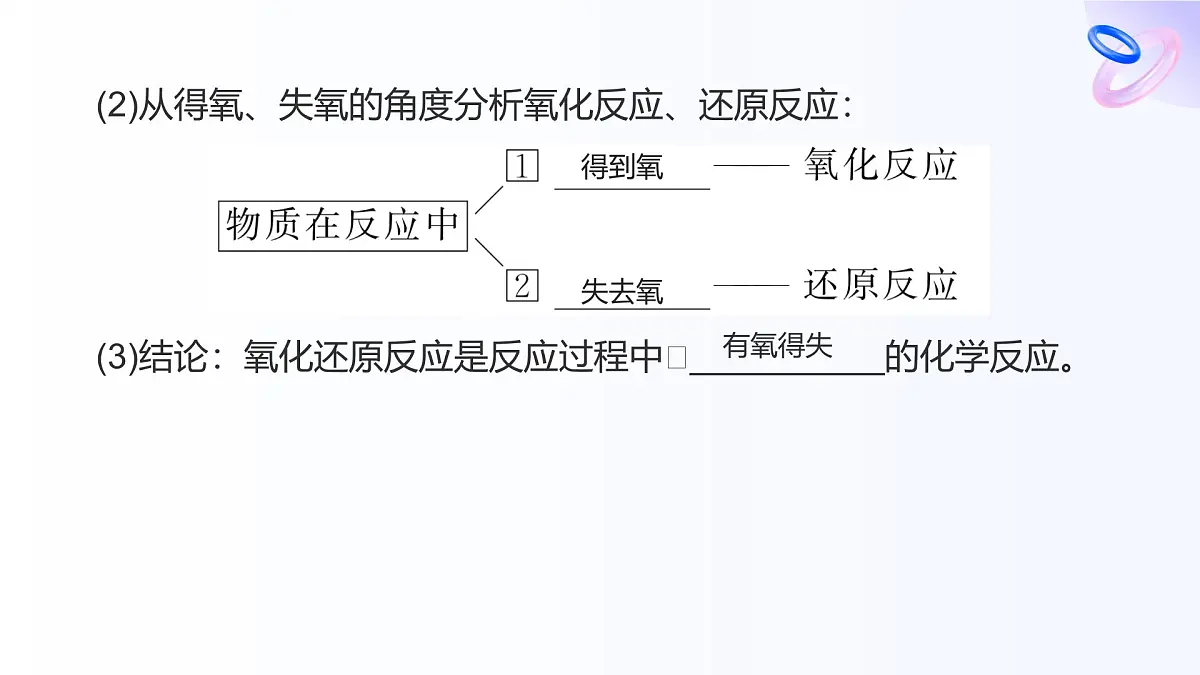
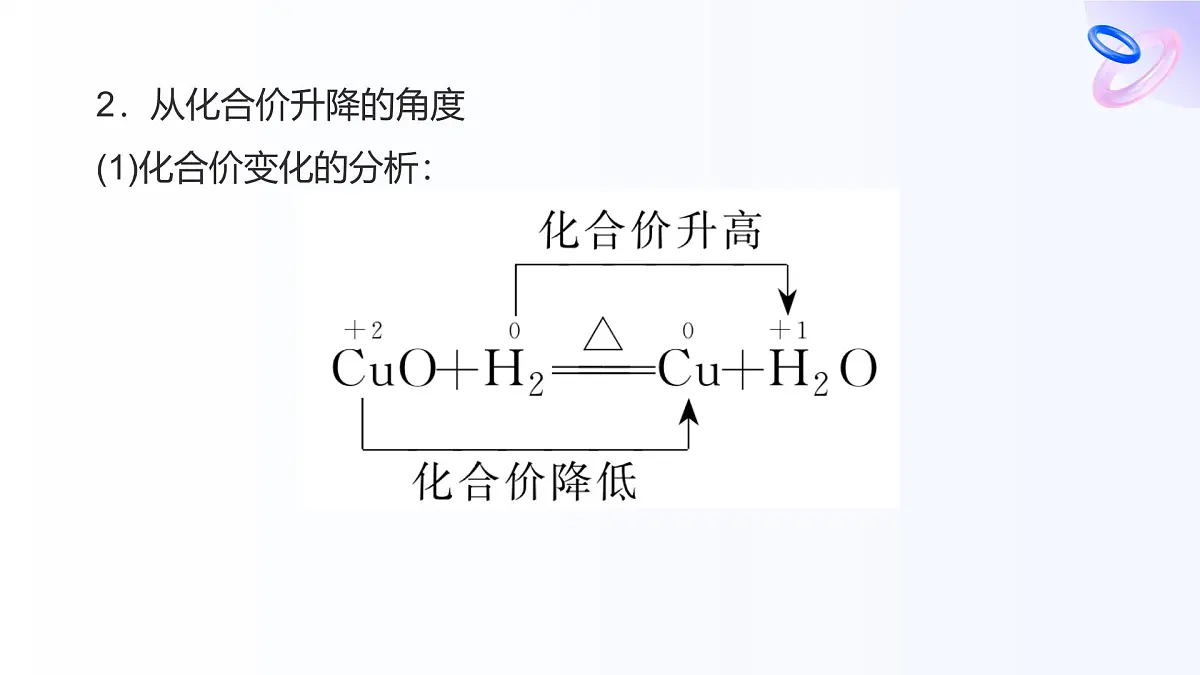
第3课时 氧化还原反应单击此处添加副标题课程目标1. 了解氧化反应、还原反应的概念。2.从化合价升降、电子的得失或电子对偏移角度理解氧化还原反应。3.培养由现象到本质的科学探究意识。图说考点内容索引0101.学业基础——自学·思记·尝试02.核心素养——合作·探究·分享0203.学考评价——夯实·测控·演练0304.课时作业(十二)0401.学业基础——自学·思记·尝试章节副标题01学业基础—自学·思记·尝试[新知预习]一、从不同角度认识氧化还原反应1.从得氧、失氧的角度(1)得氧、失氧的分析: (2)从得氧、失氧的角度分析氧化反应、还原反应:(3)结论:氧化还原反应是反应过程中__________的化学反应。得到氧失去氧有氧得失2.从化合价升降的角度(1)化合价变化的分析: (2)从化合价变化的角度认识氧化反应和还原反应: (3)结论:氧化还原反应是反应过程中元素化合价________的化学反应。升高降低有变化3.从电子转移的角度(1)有电子得失的反应:①电子得失的分析②从电子得失的角度分析氧化反应、还原反应③结论:氧化还原反应过程中元素的原子间有电子的__________。失去电子得到电子得失 降低偏向还原升高偏离氧化有电子转移(电子得失或共用电子对偏移)二、氧化还原反应的基本概念和实质1.基本概念和实质(1)基本概念:(2)实质:电子的转移(即电子的得失或共用电子对偏移)。(3)特征:元素化合价发生变化。得到偏向失去偏离氧化还原2.反应中概念间的关系 (1)氧化剂在反应中化合价__________→具有__________性→被__________→生成__________产物,发生还原反应。(2)还原剂在反应中化合价__________→具有__________性→被__________→生成__________产物,发生氧化反应。降低氧化还原还原升高还原氧化氧化失去得到三、氧化还原反应的表示方法(双线桥法) 2.农业、生活方面:(1)植物的光合作用、呼吸作用是复杂的氧化还原过程。如6CO2+6H2O―→C6H12O6+6O2(2)易燃物的自燃、食物的腐败。3.环境保护方面:消除汽车尾气,吸收氮氧化物,反应的化学方程式为2CO+2NO催化剂N2+2CO2。[即时自测]1.判断正误,正确的打“√”,错误的打“×”(1)氧化还原反应中一定有氧元素参加。( )(2)有单质生成的反应一定是氧化还原反应。( )(3)在氧化还原反应中可能只有元素化合价的升高,而无元素化合价的降低。( )(4)氧化还原反应过程中得电子的物质是还原剂,失电子的原子被还原。( )××××(5)当反应中有一种元素被氧化时,一定有另一种元素被还原。( )(6)反应中不一定所有元素的化合价都发生变化。( )(7)某元素从游离态变为化合态,该元素一定被氧化。( )(8)氧化还原反应中的反应物,不是氧化剂就一定是还原剂。( )√×××答案:C2.下列古代技术的应用中,不涉及氧化还原反应的是( ) 答案:C 答案:C解析:根据置换反应的定义可知,该反应属于置换反应,反应前后有元素的化合价发生变化,也属于氧化还原反应。02.核心素养——合作·探究·分享章节副标题02核心素养——合作·探究·分享提升点1 氧化还原反应有关概念例1 某国外化学教材中有一张关于氧化还原反应的插图:由图可知, 在该反应中是( )A.氧化剂 B.还原剂 C.氧化产物 D.还原产物答案:B 解析: 在反应中失去电子,作还原剂。状元随笔 把氧化还原反应概念中的:①得氧失氧,②化合价升降,③电子得失,进行关联记忆理解。 答案:C解析:A项中FeCl3中的Fe,B项中CO2中的C化合价都是降低的,所以FeCl3和CO2都发生还原反应;C项中的Al化合价升高,发生氧化反应;D项不是氧化还原反应。关键能力氧化还原反应各概念间的关系即:氧化剂→得到电子→所含元素化合价降低→被还原→发生还原反应→得到还原产物;还原剂→失去电子→所含元素化合价升高→被氧化→发生氧化反应→得到氧化产物。状元随笔 记忆口诀:氧→得→降→还→还→还 还→失→升→氧→氧→氧 解析:先标出发生变化的元素化合价,再用“双线桥”表示。 2Al+6H6e-Cl===2AlCl3+3H2↑状元随笔 注意“双线桥”和“单线桥”两种分析法的区别和联系。关键能力氧化还原反应中电子转移的两种表示方法1.双线桥法:表示反应前后同一元素原子间电子转移情况。基本步骤——“三步曲”。状元随笔 注意:①箭头、箭尾必须对应化合价变化的同种元素;②必须注明“得”“失”;③氧化剂和还原剂得、失电子要守恒。2.单线桥法:表示反应前后不同元素原子间电子转移情况。基本步骤——“三步曲”。状元随笔 注意:①不需标明“得”或“失”,只标明电子转移数目;②箭头标明电子转移的方向;③单线桥箭头从反应物中失电子的元素原子指向得电子的元素原子。03.学考评价——夯实·测控·演练章节副标题03学考评价——夯实·测控·演练1.下列是某学生自己总结的一些规律,其中正确的是( )A.氧化物可能是还原产物,也可能是氧化产物B.一种元素可能有多种氧化物,但同一化合价只对应一种氧化物C.只要能导电的物质就一定是电解质D.所有化学反应都属于化合、分解、置换、复分解反应中的一种反应答案:A 答案:C解析:该反应中单质硫中的硫元素化合价为0价,一部分升高到+4价,一部分降低到-2价,故在反应中硫单质既被氧化又被还原。 答案:D解析:本题给出四大基本反应类型与氧化还原反应的相互关系,考查学生识图分析的能力。解答本题的关键是理解化合反应、分解反应、置换反应和复分解反应的特点,并清楚这四大基本反应类型与氧化还原反应的关系。A项是置换反应,所有的置换反应都是氧化还原反应;B项属于分解反应,没有化合价变化,属于非氧化还原反应;C项是有单质参加的化合反应,属于氧化还原反应;D项是氧化还原反应且不属于四种基本反应类型。4.古诗词是我国重要的文化遗产,下列诗句中加点字部分涉及氧化还原反应的是( )A.月波成露露成霜,借与南枝作淡妆B.春蚕到死丝方尽,蜡炬成灰泪始干C.粉身碎骨全不怕,要留清白在人间D.莫道雪融便无迹,雪融成水水成冰答案:B解析:A项,露水变成霜没有新物质生成,属于物理变化,错误;B项,蜡炬燃烧生成二氧化碳和水等,C和O元素的化合价发生变化,属于氧化还原反应,正确;C项,石灰石受热分解生成CaO和二氧化碳,元素的化合价没有发生变化,不属于氧化还原反应,错误;D项,雪融化成水的过程中没有新物质生成,属于物理变化,错误。5.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4===2ClO2↑+2CO2↑+K2SO4+2H2O。下列有关该反应的说法正确的是( )A.KClO3在反应中失去电子B.ClO2是氧化产物C.H2C2O4在反应中被还原D.1 mol H2C2O4参加反应有2 mol电子转移答案:D解析:在该反应中,KClO3中氯元素化合价降低,在反应中得到电子被还原,生成还原产物ClO2;H2C2O4中碳元素价态由+3价升高到+4价被氧化,1 mol H2C2O4转移2 mol电子。6.高温下铝粉与氧化铁反应可用来焊接钢轨。其原理:该反应放出大量的热,置换出的铁呈熔融状态。熔融状态的铁流入钢轨的裂缝里,冷却后将钢轨牢牢地焊接在一起。该反应的化学方程式为Fe2O3+2Al高温2Fe+Al2O3。(1)反应中________是氧化剂,发生________反应。(2)铝元素的化合价由________变为________,铝________电子,被________。Fe2O3还原0+3失去氧化7.有反应①2H2O+Cl2+SO2===H2SO4+2HCl,②2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O。针对上述两个反应回答下列问题:(1)反应①中还原剂是________,还原产物是________。(2)反应②中HCl表现出的性质是________(填字母)。a.还原性 b.酸性c.氧化性SO2HClab解析:(1)由①2H2O+Cl2+SO2===H2SO4+2HCl可知,该反应中,氯气是氧化剂、硫酸是氧化产物、二氧化硫是还原剂、HCl是还原产物;由②2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O可知,该反应中高锰酸钾是氧化剂、氯气是氧化产物、HCl是还原剂、氯化锰是还原产物。(2)反应②中HCl中氯元素的化合价部分升高,部分不变,HCl表现出的性质是还原性和酸性。(3)指出反应②的氧化剂:________,氧化产物:________,用双线桥法标出反应②电子转移的方向和数目:______________________________________________。KMnO4Cl2解析:反应②中高锰酸钾是氧化剂、氯气是氧化产物,用双线桥法标出反应②电子转移的方向和数目如下: 04.课时作业(十二)章节副标题04 答案:C2.在下列物质间的变化中,加入氧化剂能实现的是( )A.H2SO4→MgSO4 B.NaCl→Cl2C.CuSO4→Cu D.HClO→Cl2解析:需要加入氧化剂,则选项中反应的物质是还原剂,发生的是氧化反应,也就是从前到后应该是化合价升高的变化。A中无化合价的变化;B中氯元素化合价升高;C中铜元素的化合价降低;D中氯元素的化合价降低。答案:B3.保险粉学名“连二亚硫酸钠”,但实际上是不“保险”的,属于一级遇湿易燃物品,遇水后可发生剧烈反应:2Na2S2O4+2H2O+O2===4NaHSO3。在该反应中Na2S2O4表现( )A.氧化性B.还原性C.既表现氧化性又表现还原性D.既不表现氧化性也不表现还原性答案:B解析:反应中,氧气中的氧元素得电子,Na2S2O4中的硫元素失电子,所以Na2S2O4表现还原性。4.成语是中华民族灿烂文化中的瑰宝,许多成语中蕴含着丰富的化学原理。下列成语中涉及氧化还原反应的是( )A.木已成舟 B.蜡炬成灰C.铁杵成针 D.滴水成冰答案:B解析:木已成舟没有新的物质生成,则没有涉及化学变化,A项错误;蜡炬成灰有新的物质生成,属于化学变化,且碳、氧元素的化合价发生变化,则属于氧化还原反应,B项正确;铁杵成针没有新的物质生成,则没有涉及化学变化,C项错误;滴水成冰没有新的物质生成,则没有涉及化学变化,D项错误。 答案:C解析:A项和C项属于双线桥,A项铜有1 mol参与反应,所以A项错误,C项正确;B和D属于单线桥,B项转移电子数错误,D项电子转移方向错误。6.氯气是一种重要的工业原料,工业上利用反应3Cl2+2NH3===N2+6HCl检查氯气管道是否漏气,下列说法错误的是( )A.氧化产物为N2B.该反应NH3被还原C.该反应HCl是还原产物D.氯气管道漏气时有白烟生成答案:B解析:反应中氮元素化合价升高被氧化,则NH3被氧化,氧化产物为N2,还原产物为HCl,选项A和C均正确,B错误;生成的HCl遇NH3化合成NH4Cl,形成白烟,选项D正确。7.某菜谱中记载:河虾不宜与西红柿同食。主要原因是河虾中含有五价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的三价砷。下列说法正确的是( )A.五价砷在维生素C作用下发生了还原反应B.“两者同食”发生的反应中维生素C作氧化剂C.因为河虾中含有砷元素,所以不能食用D.可以推测砒霜中所含的砷元素化合价为+5价答案:A解析:由信息可知,五价砷在维生素C作用下被还原为有毒的三价砷,发生了还原反应,维生素C作还原剂,A正确,B、C错误;砒霜剧毒,故砷元素化合价应为+3价。8.日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )A.铜器出现铜绿[Cu2(OH)2CO3]B.铁制菜刀生锈C.大理石雕像被酸雨腐蚀毁坏D.铝锅表面生成致密的薄膜答案:C解析:A、B、D三项均是由金属单质生成化合物,所以A、B、D三项都是氧化还原反应;C项中发生的反应是复分解反应。 答案:B 二、非选择题(共33分)10.(8分)已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O(1)被氧化的元素是____________,被还原的元素是____________,发生氧化反应的物质是____________,发生还原反应的物质是____________。CuNCuHNO3(2)用双线桥法表示反应电子得失的方向和数目:______________________________________。(3)用单线桥法表示反应电子转移的方向和数目:__________________________________________。解析:由化学方程式可知铜元素化合价升高,从0价变为+2价,被氧化;氮元素化合价降低,从+5价变为+2价,被还原;故Cu发生氧化反应,HNO3发生还原反应。 还原还原失1解析:①反应中铁元素的化合价降低,则Fe3+作氧化剂,被还原。维生素C是还原剂。②若有1 mol Fe3+转化为Fe2+共得到1 mol电子,根据电子守恒,则维生素C失1 mol电子。12.(6分)我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:KIO3+5KI+3H2SO4===3K2SO4+3I2+3H2O。(1)用双线桥表示电子转移方向和数目_________________________________。解析:(1)氧化还原反应KIO3+5KI+3H2SO4===3K2SO4+3I2+3H2O中,电子转移情况如下:(2)如果反应中转移0.5 mol电子,则生成I2的物质的量为________。(3)若要提取生成的碘,所用的萃取剂可以是________(填序号)。①水 ②酒精③淀粉溶液 ④四氯化碳0.3 mol④解析:(2)在上述反应中,转移5 mol电子生成碘单质的量是3 mol,所以如果反应中转移0.5 mol电子,则生成I2的物质的量为0.3 mol;(3)碘在有机溶液中的溶解度远大于在水中的溶解度,所以采用萃取的方法提取碘,可以选用四氯化碳作萃取剂。13.(6分)根据反应①~④四个反应,回答下列问题:①Cl2+2KI===2KCl+I2②2FeCl2+Cl2===2FeCl3③2FeCl3+2HI===2FeCl2+2HCl+I2④H2S+I2===S+2HI(1)反应①的反应类型为________(填序号)。A.置换反应 B.复分解反应C.化合反应 D.氧化还原反应AD(2)对于反应②,还原剂与氧化剂的物质的量之比为________。(3)对于反应③,当有0.1 mol的Fe2+生成时,转移电子数目为____________。(4)根据上述四个反应可判断出Cl2、I2、Fe3+、S四种物质的氧化性强弱顺序为___________。6.02×1022Cl2>Fe3+>I2>S解析:对于反应③2FeCl3+2HI===2FeCl2+2HCl+I2,由电子转移情况看每生成0.1 mol Fe2+转移0.1 mol电子,其个数为6.02×1022。2∶114.(7分)《南村辍耕录》中记载:“杭人削松木为小片,其薄如纸,熔硫黄涂木片顶端分许,名曰发烛。”《资治通鉴》中记载:“陈宣帝太建九年,齐后妃贫苦,至以卖烛为业。”文中的发烛就是原始的火柴。K2Cr2O7是火柴工业用作制造火柴的氧化剂。在下列反应中:K2Cr2O7+14HCl(浓)===2KCl+2CrCl3+3Cl2↑+7H2O(1)________元素被氧化,________是氧化剂。(2)________是氧化产物,________发生氧化反应。氯K2Cr2O7Cl2HCl解析:(1)反应中氯元素的化合价-1升高到0,被氧化;K2Cr2O7中铬元素的化合价由+6价降低到+3价,被还原,K2Cr2O7作氧化剂。(2)HCl→Cl2,氯元素化合价升高,发生氧化反应,Cl2为氧化产物。(3)在参加反应的盐酸中,起还原剂(被氧化)作用的HCl与起酸性作用的HCl的质量比为________。(4)该反应中每生成3 mol Cl2转移电子数为________个。6NA解析:(3)14个HCl分子参加反应,有6个HCl分子被氧化,生成3个Cl2分子,另外8个HCl分子起酸性作用,所以起还原剂(被氧化)作用的HCl与起酸性作用的HCl的质量比为6∶8=3∶4。(4)氯元素的化合价由-1价变到0价,故生成3 mol Cl2转移电子数为3×2×[0-(-1)]NA=6NA个。3∶4感谢观看Thank you
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 



.png)





