
所属成套资源:鲁教版九年级化学下册课件、教案、备课素材
初中鲁教版(2024)酸碱中和反应教案设计
展开 这是一份初中鲁教版(2024)酸碱中和反应教案设计,共6页。
教学设计
教学反思:
1.学生是否掌握中和反应的概念,能否正确运用概念判断中和反应?
2.学生是否掌握中和反应的微观实质?
3.学生是否掌握中和反应在生产和生活中的应用?
4.学生能否理解无明显现象的中和反应,如何才能判断反应是否发生?教学分析:
通过前面的学习,对于什么是酸,什么是碱,什么是盐以及如何鉴别酸或碱,学生已经熟悉,而且对酸、碱的相关物理性质、化学性质有所了解,但对于酸和碱之间会发生什么反应及反应后溶液的酸碱性没有进行系统的探究,如何通过具体的实验来探究呢?这些问题大多数学生从来没有思考过,所以需教师设置问题来激发学生的探究欲望。所以本节课教学的起点应定位于学生已有的酸碱知识的基础上,设计有利于学生自主学习的情境,对酸碱中和反应进行再探究!
教学目标:
1.通过实验和分析讨论,认识中和反应的实质,学会利用中和反应来改变溶液的酸碱性。
2.通过酸和碱反应的探究,提高发现和提出问题的能力,初步学会借助pH判断物质是否发生化学反应。
3.通过交流和讨论,了解中和反应在生产、生活中的应用,认识化学对生产和改善人们生活质量的重要性。
教学重点:中和反应的实质和应用。
教学难点:中和反应的实质及借助pH判断酸碱中和反应能否发生。
教学用具:多媒体课件、NaOH溶液、盐酸、pH试纸、标准比色卡、玻璃棒、pH传感器等。
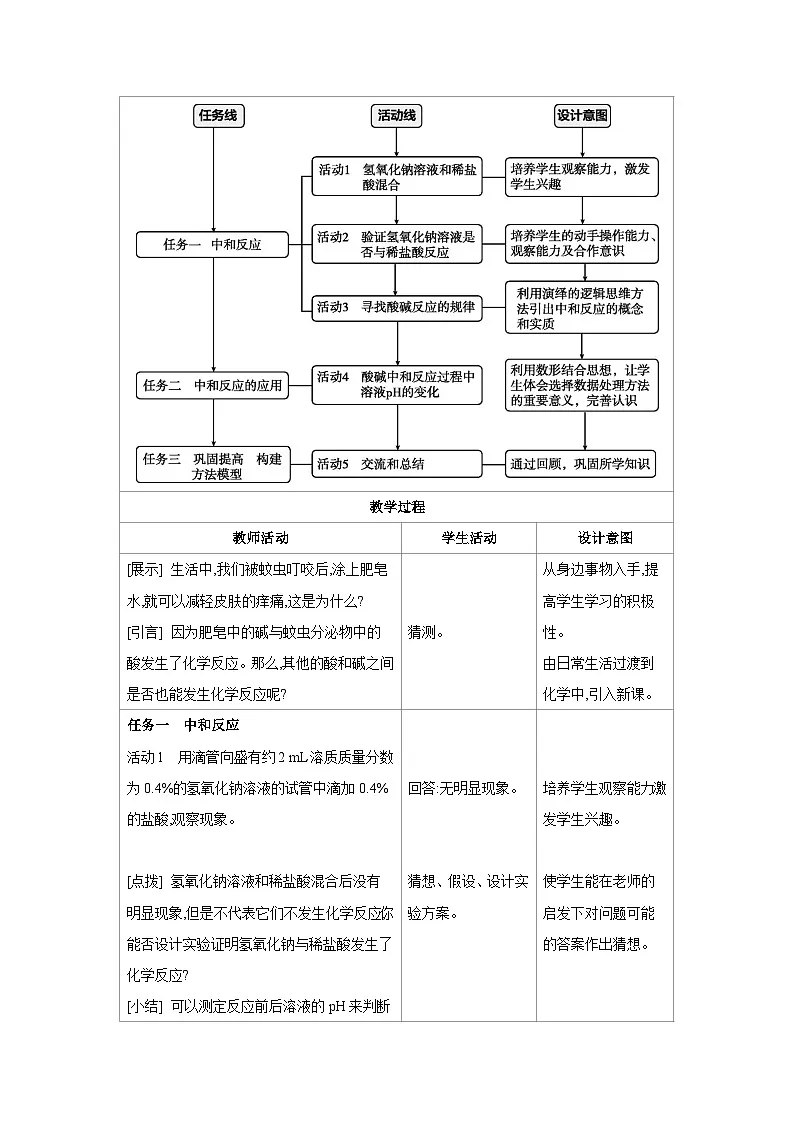
教学思路
教学过程
教师活动
学生活动
设计意图
[展示] 生活中,我们被蚊虫叮咬后,涂上肥皂水,就可以减轻皮肤的痒痛,这是为什么?
[引言] 因为肥皂中的碱与蚊虫分泌物中的酸发生了化学反应。那么,其他的酸和碱之间是否也能发生化学反应呢?
猜测。
从身边事物入手,提高学生学习的积极性。
由日常生活过渡到化学中,引入新课。
任务一 中和反应
活动1 用滴管向盛有约2 mL溶质质量分数为0.4%的氢氧化钠溶液的试管中滴加0.4%的盐酸,观察现象。
[点拨] 氢氧化钠溶液和稀盐酸混合后没有明显现象,但是不代表它们不发生化学反应,你能否设计实验证明氢氧化钠与稀盐酸发生了化学反应?
[小结] 可以测定反应前后溶液的pH来判断是否发生了化学反应。
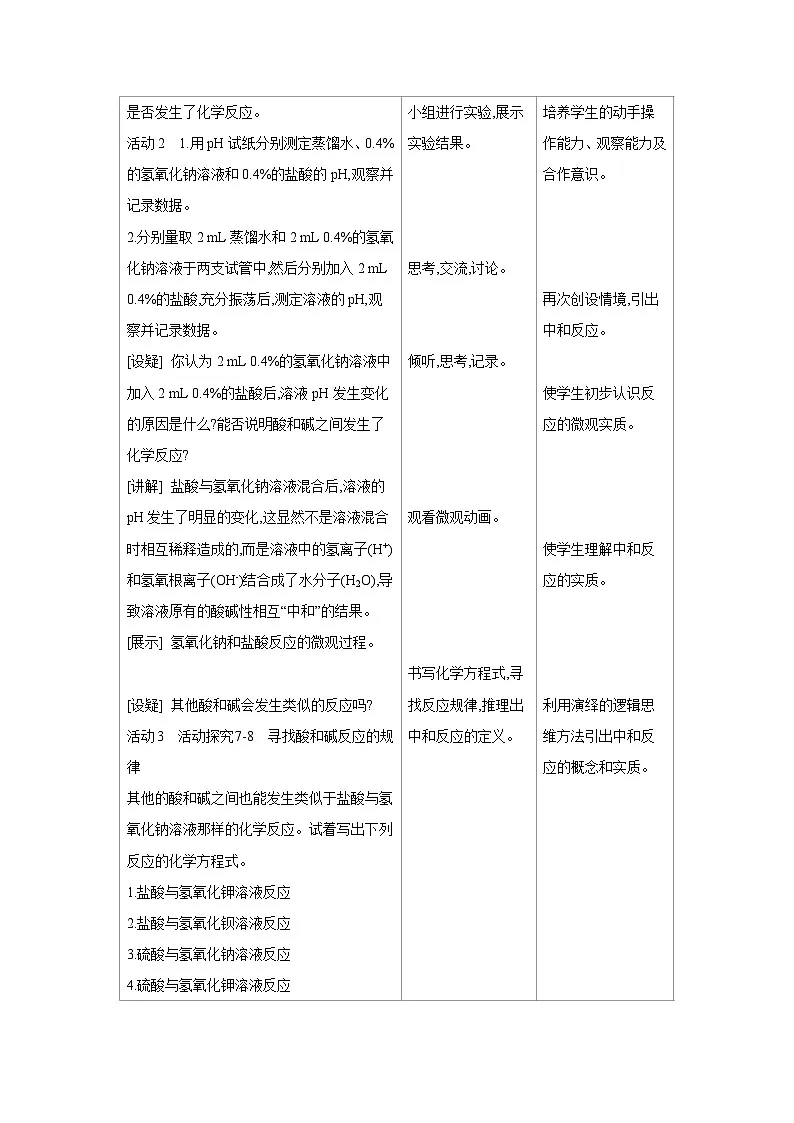
活动2 1.用pH试纸分别测定蒸馏水、0.4%的氢氧化钠溶液和0.4%的盐酸的pH,观察并记录数据。
2.分别量取2 mL蒸馏水和2 mL 0.4%的氢氧化钠溶液于两支试管中,然后分别加入2 mL 0.4%的盐酸,充分振荡后,测定溶液的pH,观察并记录数据。
[设疑] 你认为2 mL 0.4%的氢氧化钠溶液中加入2 mL 0.4%的盐酸后,溶液pH发生变化的原因是什么?能否说明酸和碱之间发生了化学反应?
[讲解] 盐酸与氢氧化钠溶液混合后,溶液的pH发生了明显的变化,这显然不是溶液混合时相互稀释造成的,而是溶液中的氢离子(H+)和氢氧根离子(OH-)结合成了水分子(H2O),导致溶液原有的酸碱性相互“中和”的结果。
[展示] 氢氧化钠和盐酸反应的微观过程。
[设疑] 其他酸和碱会发生类似的反应吗?
活动3 活动探究7-8 寻找酸和碱反应的规律
其他的酸和碱之间也能发生类似于盐酸与氢氧化钠溶液那样的化学反应。试着写出下列反应的化学方程式。
1.盐酸与氢氧化钾溶液反应
2.盐酸与氢氧化钡溶液反应
3.硫酸与氢氧化钠溶液反应
4.硫酸与氢氧化钾溶液反应
回答:无明显现象。
猜想、假设、设计实验方案。
小组进行实验,展示实验结果。
思考,交流,讨论。
倾听,思考,记录。
观看微观动画。
书写化学方程式,寻找反应规律,推理出中和反应的定义。
培养学生观察能力,激发学生兴趣。
使学生能在老师的启发下对问题可能的答案作出猜想。
培养学生的动手操作能力、观察能力及合作意识。
再次创设情境,引出中和反应。
使学生初步认识反应的微观实质。
使学生理解中和反应的实质。
利用演绎的逻辑思维方法引出中和反应的概念和实质。
[小结] 中和反应的定义:酸与碱作用生成盐和水的反应,叫作中和反应。
中和反应的实质是H+和OH-结合生成H2O。
[思考] 1.判断下列反应是否属于中和反应。
2.有盐和水生成的反应都是中和反应吗?
[小结] 中和反应一定有盐和水生成,但有盐和水生成的反应不一定是中和反应。
思考,交流。
检测学生对中和反应定义的理解,引导学生进一步认识中和反应的含义。
任务二 中和反应的应用
[过渡] 在氢氧化钠溶液和盐酸反应的实验中,溶液的pH是如何变化的呢?
活动4 活动探究7-9 酸碱中和反应过程中溶液pH的变化
[演示] 利用图Ⅰ装置,向20 mL 0.4%的氢氧化钠溶液中逐滴滴入0.4%的盐酸,连接在传感器上的计算机随即绘制出了溶液pH(纵坐标)随所加盐酸体积(横坐标)变化的曲线(图Ⅱ)。
[思考] 1.在向氢氧化钠溶液中滴加稀盐酸时,溶液的pH是怎样变化的?
2.你能说出曲线上坐标为(18,7)的点所表示的意义吗?
[点拨] 在向氢氧化钠溶液中滴加稀盐酸时,溶液的pH逐渐变小,最终小于7。坐标为(18,7)的点表示当滴加的稀盐酸的体积为18 mL时,溶液的pH为7,此时它们恰好完全反应。当滴入的盐酸量较少时,溶液中氢氧化钠有剩余,溶液呈碱性,pH>7;当滴入的盐酸恰好与溶液中氢氧化钠完全反应时,溶液显中性,pH=7;当滴入的盐酸过量时,溶液中盐酸有剩余,溶液呈酸性,pH
相关教案
这是一份初中鲁教版(2024)酸碱中和反应教案设计,共6页。
这是一份初中化学鲁教版(2024)九年级下册(2024)酸碱中和反应教学设计,共6页。
这是一份初中化学鲁教版九年级下册第四节 酸碱中和反应教案,共13页。教案主要包含了引入新课,讲授新课,知识回顾,演示实验,观点调查,教师提问,启发学生,学生活动等内容,欢迎下载使用。
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 






.png)
.png)



