




所属成套资源:2025-2026学年人教版化学九年级下册
人教版(2024)九年级下册(2024)常见的盐课文ppt课件
展开 这是一份人教版(2024)九年级下册(2024)常见的盐课文ppt课件,共32页。PPT课件主要包含了有白色沉淀生成,与碱反应,答案D,复分解反应,化合物,有白色絮状沉淀生成,答案A,思考与讨论,Cl-,CO32-等内容,欢迎下载使用。
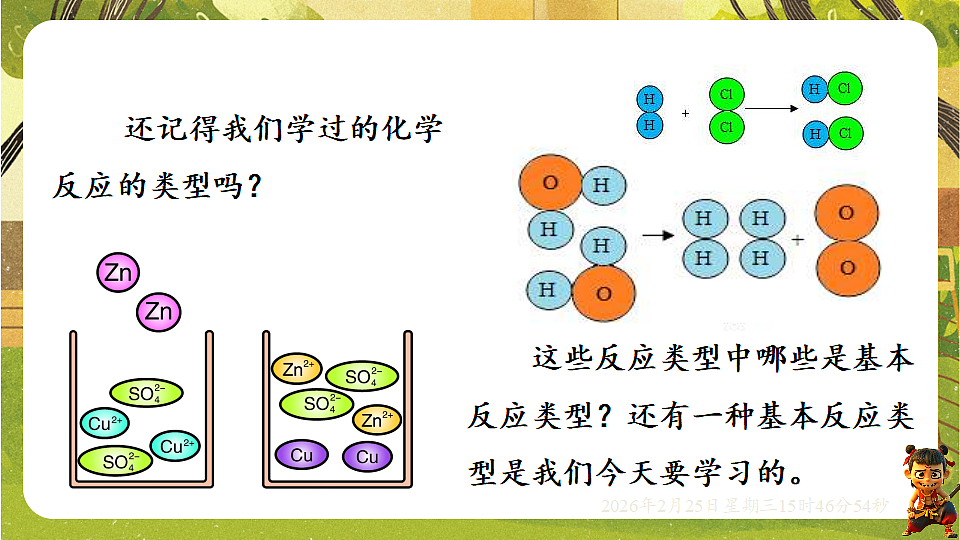
还记得我们学过的化学反应的类型吗?
这些反应类型中哪些是基本反应类型?还有一种基本反应类型是我们今天要学习的。
向盛有少量碳酸钠溶液的试管里滴入澄清的石灰水,观察现象。
碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀
Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
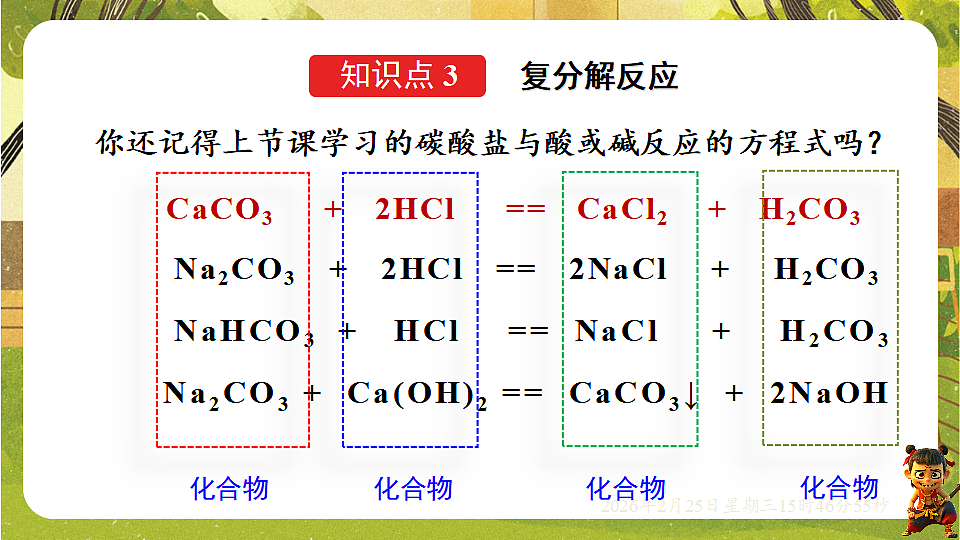
你还记得上节课学习的碳酸盐与酸或碱反应的方程式吗?
CaCO3 + 2HCl == CaCl2 + H2CO3
Na2CO3 + 2HCl == 2NaCl + H2CO3
NaHCO3 + HCl == NaCl + H2CO3
Na2CO3 + Ca(OH)2 == CaCO3↓ + 2NaOH
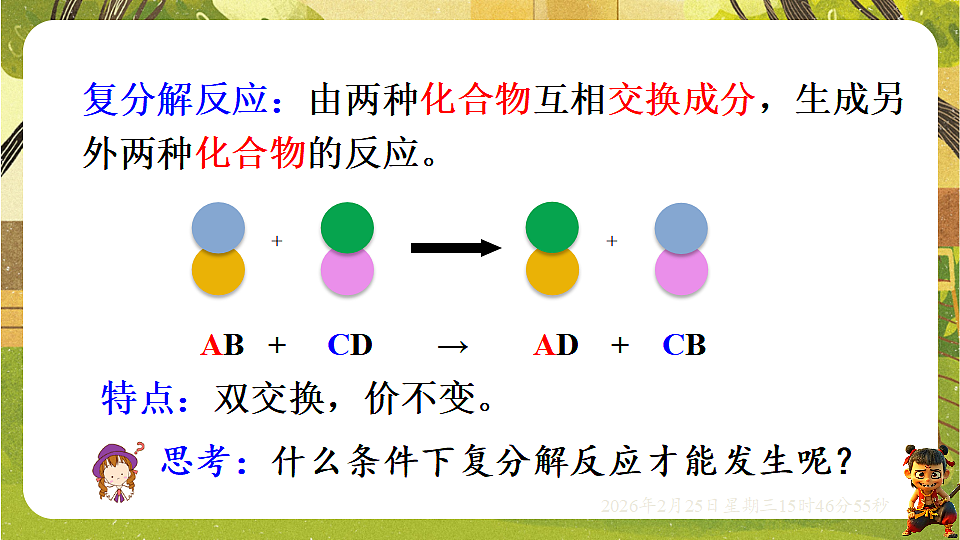
思考:什么条件下复分解反应才能发生呢?
复分解反应:由两种化合物互相交换成分,生成另外两种化合物的反应。
特点:双交换,价不变。
向两支分别盛有少量氢氧化钠溶液和氯化钡溶液的试管中滴加硫酸铜溶液,观察现象并填写下表。
有少量蓝色絮状沉淀生成
CuSO4 + 2NaOH==Cu(OH)2↓+Na2SO4
CuSO4 + BaCl2==BaSO4↓+ CuCl2
(1)上述两个反应是否属于复分解反应?观察到的现象有什么共同之处?(2)碳酸钠、碳酸钙等含碳酸根离子的盐与稀盐酸发生复分解反应时,可观察到的共同现象是什么?(3)前面学过的酸碱中和反应是否也属于复分解反应?中和反应的生成物中,相同的生成物是什么?
酸、碱、盐之间有的能发生复分解反应,有的不能发生。只有两种化合物互相交换成分,有沉淀或有气体或有水生成时,才是发生了复分解反应。
下列各组离子,可以在水中大量共存且溶液为无色的是( )A.K+、Na+、SO42-、Cl-B.H+、Fe2+、CO32-、NO3-C.H+、Ca2+、OH-、Cl-D.Ba2+、Cu2+、SO42-、NO3-
【点拨】H+、CO32-两种离子能结合成二氧化碳气体和水,且含Fe2+的水溶液呈浅绿色,B错误;H+、OH-能结合成水,C错误;Ba2+、SO42-能结合成硫酸钡沉淀,且含Cu2+的水溶液呈蓝色,D错误。
参考“部分酸、碱、盐的溶解性表” ,判断下列溶液两两混合后能否发生复分解反应。
稀硫酸、稀盐酸、NaOH溶液、NaCl溶液、K2CO3溶液、Ba(NO3)2溶液。
酸、碱、盐的溶解性(20℃)
判断的时候你都考虑了哪些因素?对于能发生复分解反应的,试写出化学方程式。
判断反应是否发生时考虑的因素是反应物是否可溶于水(或酸),生产物中是否有沉淀、气体或水。发生反应的化学方程式有:NaOH + HCl ==NaCl + H₂OK₂CO3 + 2HCl == 2KCl +H₂O + CO₂↑2NaOH + H₂SO4 == Na₂SO4 + H₂0K₂C03 + H2SO4 == K₂SO4 + H₂O + CO₂↑Ba(NO3)2 + H₂SO4 == BaSO4 ↓+ 2HNO3Ba(NO3)2 + K2CO3 == BaCO₃↓ + 2KNO3
KCl+AgNO3===KNO3+AgCl↓
判断下列各组物质间能否发生化学反应,能反应的,直接写出化学方程式,不能反应的,说明原因。(1)氯化钾溶液与硝酸银溶液混合:____________________________。(2)碳酸钠溶液与氯化钙溶液混合:__________________________________。 (3)硫酸铜溶液与氢氧化钡溶液混合:____________________________________。
Na2CO3+CaCl2===CaCO3↓+2NaCl
CuSO4+Ba(OH)2===Cu(OH)2↓+BaSO4↓
(4) 氢氧化钠溶液与氯化钾溶液混合:________________________________________________。(5)碳酸钾溶液与稀盐酸混合:_________________________________。(6)硫酸钠溶液与硝酸钡溶液混合:_____________________________________。
不能反应,因为相互交换成分后没有沉淀、气体或水生成
K2CO3+2HCl===2KCl+H2O+CO2↑
Na2SO4+Ba(NO3)2===BaSO4↓+2NaNO3
【点技巧】复分解反应发生的条件巧记复分解,两头顾,先顾头,后顾尾;顾头要看溶解性,顾尾气体沉淀水;有酸参加可不溶,无酸参加需都溶。
溶液中离子种类发生改变
2HCl+Na2CO3 ——
2NaCl + H2O+CO2↑
复分解反应发生时的离子变化
K2SO4 + NaNO3
Na2SO4 + KNO3 ——
溶液中离子种类没发生改变
盐的水溶液的颜色铜盐溶液一般呈蓝色 铁盐溶液一般呈黄色亚铁盐溶液一般呈浅绿色 高锰酸钾溶液呈紫红色
离子共存的条件:相互之间不发生反应生成水、气体、沉淀。
②通入澄清石灰水,现象:
有一瓶标签无法辨认的试剂,是碳酸钠溶液或硫酸钠溶液中的一种。仅用下列试剂无法进行鉴别的是( )A.pH试纸 B.酚酞溶液C.稀硫酸 D.硝酸钡溶液
【点拨】碳酸钠溶液呈碱性,pH大于7,能使酚酞溶液变红,而硫酸钠溶液显中性,pH等于7,不能使酚酞溶液变色,A、B不符合题意;硫酸与碳酸钠反应产生气体,与硫酸钠不反应,C 不符合题意;硝酸钡与硫酸钠和碳酸钠反应均能生成白色沉淀,所以无法鉴别,D符合题意。
①滴加氢氧化钠溶液,现象:
②用红色石蕊试纸检验,现象:
及时归纳是学好化学的重要方法之一。利用如图所示的结构图归纳盐的四个方面的化学性质(图中编号①~④),请归纳有关知识。
(1)在归纳性质②时,选取了澄清石灰水和碳酸钠溶液两种物质,它们在溶液中相互反应时产生的现象是____________________,反应的化学方程式为______________________________________。(2)在性质③中,X代表________类物质。(3)在归纳性质④时,从“某些盐”中选取了硝酸银,写出与硝酸银反应的物质的化学式:_________________(写 一个)。
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
[2025·宁波模拟]物质转化是化学研究的重要内容。甲、乙、丙、丁是不同类别的常见物质,甲是单质,丁是配制波尔多液的原料,转化关系如图所示(“—”表示相互反应,“→”表示一步转化,涉及的反应均为初中化学常见反应)。
下列说法正确的是( ) A.反应①一定是置换反应B.反应②有氢气生成C.反应③④一定有沉淀生成D.丙是盐
【点拨】甲、乙、丙、丁是不同类别的常见物质,甲是单质,丁是配制波尔多液的原料,甲与丁能反应,所以丁是硫酸铜,甲是比铜活泼的常见金属(如铁等),甲能和乙反应且乙能转化为丁,所以乙是稀硫酸,丙能和酸、盐反应,故丙是碱(如氢氧化钠等),代入验证,推断正确。甲是铁等较活泼金属,丁是硫酸铜,反应①可以是活泼金属和硫酸铜反应生成铜和另一种硫酸盐,此类反应是一种单质和一种化合物生成另一种单质和另一种
化合物,属于置换反应,故A正确;乙是稀硫酸,丁是硫酸铜,反应②可以是氧化铜或氢氧化铜和稀硫酸反应生成硫酸铜和水,故B错误;乙是稀硫酸,若丙是氢氧化钠,稀硫酸和氢氧化钠反应生成硫酸钠和水,没有沉淀生成,故C错误;由分析可知,丙是碱,故D错误。故选A。
相关课件
这是一份人教版(2024)九年级下册(2024)常见的盐课文ppt课件,共32页。PPT课件主要包含了有白色沉淀生成,与碱反应,答案D,复分解反应,化合物,有白色絮状沉淀生成,答案A,思考与讨论,Cl-,CO32-等内容,欢迎下载使用。
这是一份初中化学常见酸、碱的化学性质评优课ppt课件,共41页。PPT课件主要包含了讲授新课,导入新课,化学方程式,都发生在溶液中,新知探究,通入澄清石灰水,白色粉末,加入水,无色溶液,加入盐酸等内容,欢迎下载使用。
这是一份人教版(2024)九年级下册(2024)常见的盐课前预习ppt课件,共42页。PPT课件主要包含了讲授新课,导入新课,化学方程式,都发生在溶液中,新知探究,通入澄清石灰水,白色粉末,加入水,无色溶液,加入盐酸等内容,欢迎下载使用。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 






.png)




