

人教版九年级上册第五单元 化学方程式综合与测试复习ppt课件
展开参加——————— —各— — — — 质量总和____________ ——各— ———质量总和
知识点1:质量守恒定律
1、质量守恒定律的定义
运用质量守恒定律要注意以下几点
⒈适用范围是化学反应,不能用来解释物理变化。⒉“守恒”是指质量守恒,并不是指体积等守恒。⒊“质量守恒”对反应前的物质而言,是指“参加反应”的物质质量的总和,不参加反应的物质的质量不能计算在内。
1.判断下列是否正确?A、纸燃烧化为灰烬,灰烬的质量比纸的质量小B、2克氢气和8克氧气在点燃的条件下发生化合 反应生成10克水C、10克水受热变为10克水蒸气D、蜡烛燃烧后质量变小
镁条燃烧是镁条与空气中的氧气反应,生成了白色固体氧化镁。根据质量守恒定律可知:生成物氧化镁的质量应等于反应物镁条与氧气的质量之和。所以,氧化镁的质量要比镁条的质量大。
2. 镁条在空气中燃烧后,生成的白色粉末的质量比原来镁条的质量增加,这符合质量守恒定律吗?
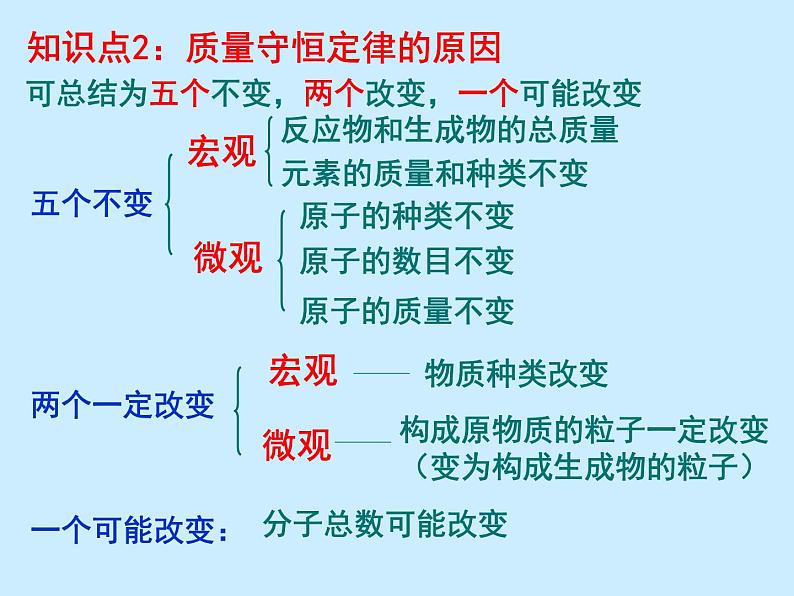
知识点2:质量守恒定律的原因
可总结为五个不变,两个改变,一个可能改变
反应物和生成物的总质量
2、参加反应的各物质质量总和等于反应后生成的 各物质质量总和。是因为 ( ) A.反应后物质的种类没有变化 B.反应后分子的种类没有变化 C.反应后原子的种类、数目和质量没有变化 D.反应后分子的种类、数目和质量没有变化
1、在化学反应前后下列微粒可能发生变化的是 ( ) A、原子种类 B、分子个数 C、原子个数 D、原子质量
3、某物质在纯氧气中完全燃烧后生成了二氧化碳和水,则关于该物质的组成的说法正确的是——A、一定含有碳、氢、氧三种元素。 B、一定含有碳、氧元素。C 、一定含碳、氢元素。 D、无法确定4、某化合物X完全燃烧的化学方程式为 X+O2→CO2+H2O﹙未配平﹚则X不可能是——A、CO B、CH4 C、CH3OH D、C2H5OH
5、在一个密闭容器内有A、B、C、D、四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
(1)表格中M=________(2)密闭容器中发生的化学变化属于________ 反应(填基本反应类型)(3)该反应中A、B、C、D四种物质(参加反应或生成)的质量比为______
22:9:111:80
1、化学方程式的涵义(化学方程式提供的信息)
a. 哪些物质参加了反应(反应物)b .生成了哪些物质(生成物)c .反应条件d .反应物与生成物之间的粒子数量比e. 反应物与生成物之间的质量比
例如:C+O2==CO2① 宏观 (质的方面):碳与氧气在点燃的条件下生成二氧化碳。② 量的方面:每12份质量的碳跟32份质量的氧气完全反应生成44份质量的二氧化碳。③微观(粒子方面):每1个碳原子与1个氧分子反应生成1个二氧化碳分子。
1、根据化学方程式不能获得的信息是——A、该反应中的反应物和生成物 B、各反应物和生成物的质量比C、发生反应所需要的条件 D、化学反应的快慢2、10克A和足量的B混合加热发生反应,10克A完全反应,生成8克C和4克D,则参加反应的A与B的质量比为——A、1:1 B、2:1 C、4:1 D、5:13、化学方程式3Fe + 2O2 点燃 Fe3O4可读作:__A.铁加氧气等于四氧化三铁 B.三个铁加两个氧气等于一个四氧化三铁C.铁和氧气点燃后生成四氧化三铁 D.铁加氧气点燃等于四氧化三铁
1、书写原则:①——————— ②———————2、书写步骤:①——、②——、③——3、涵 义:①———————— ②————————4、 读 法:①———、②————
表示反应物、生成物和反应条件
表示反应物、生成物之间的质量比
3、如何正确书写化学方程式
1、配平下列化学方程式(反应条件已省略)1、﹙﹚H2O=﹙﹚H2↑+﹙﹚O2↑ 2、 ﹙ ﹚AI + ﹙ ﹚ O2= ﹙ ﹚ AI2O3 3、( )Fe2O3+( )C = ( )Fe+ ( )CO2↑ 4、﹙ ﹚KCIO3=﹙ ﹚KCI+﹙ ﹚O2↑2.下列各式中,正确表示铝与稀硫酸反应的化学方程式是( )A.Al + H2SO4 ==== AlSO4 + H2↑ B.2Al+ 3H2SO4 ==== Al2(SO4)3 + 3H2↑C. Al + 2H2SO4 ==== Al(SO4)2 + 2H2↑ D. 2Al + H2SO4 ==== Al2SO4 + H2↑
3. 请按“一写、二配、三注明”的书写步骤正确书写出下列两个化学方程式。
(1)、水在通电的条件下生成氢气和氧气;(2)、实验室用双氧水制取氧气;(3)、乙炔(C2H2)在氧气中燃烧生成水和二氧化碳;(4)、氧化铝和稀硫酸(H2SO4)作用生成硫酸铝和水。
知识点4:根据化学方程式计算
1.设未知量(求什么就设什么,将所求的问题一次设出)2.写出化学方程式并配平(计算中所用到的化学方程式)3.写出有关物质的相对分子质量和已知量、未知量(只写与已知和所求有关的物质,上写相对分子质量,下写物质的质量,已知的带单位)4.列出比例式、求解(列正比例式,上下同种量,左右同一物质)5.简明地写出答案
1、已知反应物的质量求生成物的质量;2、已知生成物的质量求反应物的质量; 3、已知一种反应物的质量求另一种反应物的质量;4、已知一种生成物的质量求另一种生成物的质量;
1、三要领:(1)步骤要完整;(2)格式要规范; (3)得数要准确。
2、三关键:(1)书写化学式要正确; (2)方程式要配平; (3)相对分子质量计算要准确。
化学方程式的计算时容易犯的错误
1、化学方程式书写不正确2、代入化学方程式的不是纯净物的质量3、解题格式不规范,计算不准确,相对分子质量计算错误4、在计算过程中单位不一致5、结果没有单位,
2、有氯酸钾和二氧化锰混合物15克,加热使它完 全反应,结果发现试管内固体物质为10.2克, 试回答: (1)生成多少克氧气? (2)充分反应后,试管内含有那些固体物质? 其质量分别为少克?
1、实验室用6.5克锌粒,与足量的稀硫酸充分 反应( Zn+H2SO4=ZnSO4+H2↑)可生成氢气多 少升?(在标况下,氢气的密度为0.09g/L)
1.质量守恒定律揭示了化学反应中的( ) A.反应条件 B.哪些物质起反应 C.哪些物质是生成物 D.反应物和生成物的质量的关系2.下列叙述符合质量守恒定律的是( )A.水加热变成水蒸气,变化后质量相等B.50mL水与50ml酒精混合不等于100mLC.在90g水中含有10g氢气和80g氧气 D.1g硫与1g氧气化合生成2g二氧化硫
3.在2A+B == 2C反应中,已知A的相对分子质量为24,C的相对分子质量为40,则B的相对分子质量为A. 16 g B. 32 g C. 16 D. 32 4.在 2H2O2 MnO2 2H2O+O2↑ 的反应中,反应前后肯定发生变化的是A.元素种类 B.各种原子的数目C.各元素的化合价 D.物质的质量总和5.铝在氧气中燃烧生成氧化铝。在这个反应中,铝、氧气、氧化铝的质量比是 A. 27∶32∶102 B. 27∶24∶43 C. 4∶3∶2 D. 108∶96∶204
6、近几年来,科学发现在生物体内存在少量一氧化氮,它有扩张血管和增强记忆力的功能,成为当前生物科学研究的热点。一氧化氮是工业制取硝酸的中间产物,生成一氧化氮的化学方程式为: 4NH3 + 5O2 催化剂 4NO + 6X ,则X的化学式是7、 我国自行设计和制造的长征3号火箭用液氧和液氢作推进剂,点火时发生反应的化学方程式 8、饲养观赏鱼,可以陶冶人的情操,增进人们对生活的热爱。空运观赏鱼,必须密封。为了解决鱼的吸氧问题,可在水中加入过氧化钙(化学式CaO2),过氧化钙与水反应生成的是氢氧化钙和氧气。写出过氧化钙与水反应的化学方程式
2H2+O2点燃2H2O
2CaO2+2H2O=2Ca﹙OH﹚2+02↑
人教版初中化学九上复习课:第五单元 化学方程式 课件: 这是一份人教版初中化学九上复习课:第五单元 化学方程式 课件
2022届初中化学一轮复习 第五单元 化学方程式 课件: 这是一份2022届初中化学一轮复习 第五单元 化学方程式 课件,共60页。PPT课件主要包含了真题体验,答案D,答案B,考点梳理,参加化学反应,质量总和,总质量,化合价,反应物,生成物等内容,欢迎下载使用。
人教版课题 3 利用化学方程式的简单计算图片ppt课件: 这是一份人教版课题 3 利用化学方程式的简单计算图片ppt课件,共17页。PPT课件主要包含了情景引入,学习目标,设未知量,列比例式求解,简明地写出答案,例题1P102,上标相对分子质量,下标已知质量和未知数,注意事项,顺口溜等内容,欢迎下载使用。