










所属成套资源:人教版高中化学同步选择性必修第一册课件PPT+讲义+专练(新教材)
- 第三章 第三节 第1课时 盐类的水解--人教版高中化学选择性必修第一册同步课件+讲义+专练(新教材) 课件 0 次下载
- 第三章 第三节 第2课时 影响盐类水解的主要因素及盐的水解常数的应用--高中化学选择性必修第一册同步讲练测(新教材) 试卷 0 次下载
- 第三章 第三节 第4课时 电解质溶液中微粒间的关系--人教版高中化学选择性必修第一册同步课件+讲义+专练(新教材) 课件 0 次下载
- 第三章 第三节 第5课时 溶液中粒子浓度大小比较--人教版高中化学选择性必修第一册同步课件+讲义+专练(新教材) 课件 0 次下载
- 第三章 第三节 第6课时 溶液中粒子浓度图像分析--人教版高中化学选择性必修第一册同步课件+讲义+专练(新教材) 课件 0 次下载
高中人教版 (2019)实验活动3 盐类水解的应用精品ppt课件
展开
这是一份高中人教版 (2019)实验活动3 盐类水解的应用精品ppt课件,文件包含第三章第三节第3课时盐类水解的应用及广义水解pptx、第三章第三节第3课时盐类水解的应用及广义水解专练docx、第三章第三节第3课时盐类水解的应用及广义水解教师版docx、第三章第三节第3课时盐类水解的应用及广义水解学习笔记docx、盐类水解的应用mp4等5份课件配套教学资源,其中PPT共60页, 欢迎下载使用。
第3课时 盐类水解的应用 及广义水解
1.了解盐类水解在生产生活、化学实验、科学研究中的应用。2.能够对盐类水解的知识进行拓展迁移,解决类盐水解问题。
核心素养 发展目标
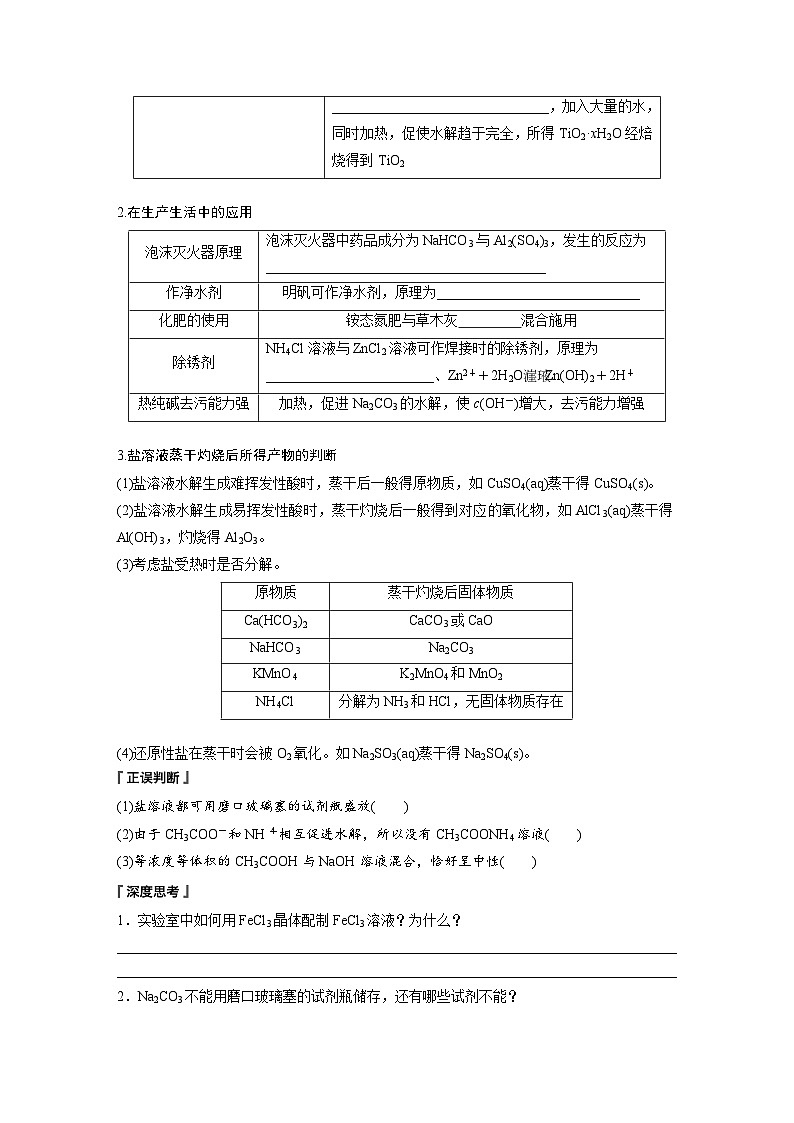
1.在化学实验中的应用
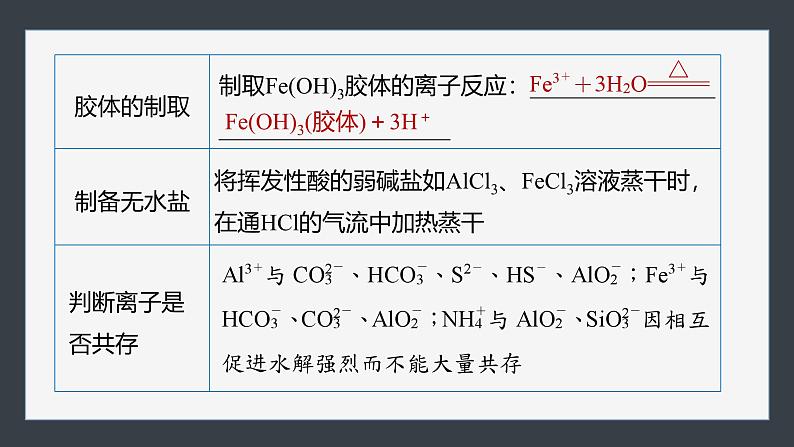
Fe(OH)3(胶体)+3H+
(x+2)H2O===TiO2·xH2O↓+4HCl
2.在生产生活中的应用
3.盐溶液蒸干灼烧后所得产物的判断(1)盐溶液水解生成难挥发性酸时,蒸干后一般得原物质,如CuSO4(aq)蒸干得CuSO4(s)。(2)盐溶液水解生成易挥发性酸时,蒸干灼烧后一般得到对应的氧化物,如AlCl3(aq)蒸干得Al(OH)3,灼烧得Al2O3。
(3)考虑盐受热时是否分解。
(4)还原性盐在蒸干时会被O2氧化。如Na2SO3(aq)蒸干得Na2SO4(s)。
(1)盐溶液都可用磨口玻璃塞的试剂瓶盛放(2)由于CH3COO-和 相互促进水解,所以没有CH3COONH4溶液(3)等浓度等体积的CH3COOH与NaOH溶液混合,恰好呈中性
1.实验室中如何用FeCl3晶体配制FeCl3溶液?为什么?
提示 将FeCl3晶体溶于较浓的盐酸中,然后加水稀释到所需的浓度;加酸抑制FeCl3水解。
2.Na2CO3不能用磨口玻璃塞的试剂瓶储存,还有哪些试剂不能?
提示 因为玻璃的主要成分是SiO2,SiO2能和碱反应,因此碱溶液及水解呈碱性的盐溶液,如NaOH、KOH、Na2S、Na2SiO3等都不能用磨口玻璃塞的试剂瓶储存。
3.已知Cu2+、Fe2+、Fe3+完全水解时,溶液的pH分别为6.4、9.6、3.7。如何除去CuCl2溶液中的Fe3+、Fe2+?
提示 因Fe2+比Cu2+难水解,应先加入氧化剂(如H2O2)把Fe2+氧化为Fe3+,再加入CuO、Cu(OH)2、CuCO3或Cu2(OH)2CO3等,促进Fe3+水解生成Fe(OH)3沉淀而除去。
1.下列事实,其中与盐类的水解有关的是___________(填序号)。①NaHSO4溶液呈酸性②长期使用(NH4)2SO4化肥会使土壤酸性增大,发生板结③配制CuCl2溶液,用稀盐酸溶解CuCl2固体④实验室盛放纯碱溶液的试剂瓶不能用磨口玻璃塞⑤加热FeCl3·6H2O晶体,往往得不到FeCl3固体
2.将下列固体物质溶于水,再将其溶液加热、蒸发结晶,再灼烧,得到化学组成与原固体物质相同的是______(填序号)。①胆矾 ②氯化铝 ③硫酸铝 ④氯化铜 ⑤硫酸亚铁 ⑥碳酸钠 ⑦亚硫酸钠 ⑧NH4Cl ⑨KMnO4 ⑩Ca(HCO3)2
广义的盐类水解观认为就是某化合物与水发生复分解,化合物中显正价的离子结合OH-,显负价的离子结合H+。包括盐类水解和类盐水解,类盐虽然不是由酸碱中和后得到的生成物,但也具有盐的水解等性质的一类化合物。
2.中学阶段常见的类盐水解反应(1)金属氢化物NaH+H2O===_____________CaH2+2H2O===_______________(2)金属氮化物、磷化物Li3N +3H2O===_______________Ca3P2+6H2O===__________________AlP+3H2O===__________________
Ca(OH)2+2H2↑
3Ca(OH)2+2PH3↑
Al(OH)3↓+PH3↑
(3)金属碳化物CaC2+2H2O===________________Al4C3+12H2O===____________________Mg2C3+4H2O===___________________(4)卤素互化物IBr+H2O===___________IF5+3H2O===____________
Ca(OH)2+C2H2↑
4Al(OH)3↓+3CH4↑
2Mg(OH)2↓+C3H4↑
(5)非金属元素的卤化物NH2Cl + H2O ____________NCl3+3H2O===______________BCl3+3H2O===______________PCl3+3H2O===______________PCl5+4H2O===_____________SiCl4+4H2O===________________
H4SiO4↓+4HCl
1.(2022·郑州高二月考)广义的水解观认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述观点,下列说法错误的是A.BaO2的水解产物是Ba(OH)2和H2O2B.PCl3的水解产物是HClO和H3PO3C.Al4C3的水解产物是Al(OH)3和CH4D.CH3COCl的水解产物是两种酸
2.(2022·绵阳高二检测)实验室可利用SbCl3的水解反应制取Sb2O3:(1)SbCl3水解的化学方程式为_____________________________。(2)为得到较多较纯的Sb2O3,操作时将SbCl3徐徐加入大量水中,反应后期还要加入少量_____(填字母)。A.氨水 B.盐酸 C.醋酸
(3)SOCl2是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。①根据实验现象写出SOCl2和H2O反应的化学方程式:_______________________________。
===SO2↑+2HCl↑
②利用AlCl3·6H2O制备无水AlCl3时,可用SOCl2和AlCl3·6H2O混合共热,试解释原因:__________________________________________________________。
SOCl2和结晶水反应既能消耗水,生成的酸又能
题组一 盐类水解的应用1.化学在日常生活和生产中有着重要的应用。下列说法不正确的是A.某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为溶液中 的 发生水解B.明矾水解形成的Al(OH)3胶体能吸附水中的悬浮物,可用于水的净化C.将饱和FeCl3溶液滴入沸水中可制备Fe(OH)3胶体,利用的是盐类水解 原理D.配制FeCl3溶液时加入少量的盐酸,抑制Fe3+水解
pH=7的溶液中,Cu2+、S2-会发生反应生成沉淀,不能大量共存,故C错误;
题组二 盐溶液蒸干(灼烧)产物的判断4.在空气中直接蒸发下列盐的溶液:①Fe2(SO4)3;②Na2CO3;③KCl;④CuCl2;⑤NaHCO3。可以得到相应盐的晶体(可以含有结晶水)的是A.①②③ B.①③⑤C.②④ D.①③④⑤
5.为了得到比较纯净的物质,使用的方法恰当的是A.向Na2CO3饱和溶液中通入过量的CO2后,在加压、加热的条件下,蒸 发得到NaHCO3晶体B.Al2S3不能用复分解反应的方法在溶液中制取,而只能由S粉和Al粉混合 加热制得C.向FeBr2溶液中加入过量的氯水,加热蒸发得到FeCl3晶体D.向FeCl3溶液中加入过量的NaOH溶液,经过滤、洗涤沉淀,再充分灼 烧沉淀得到Fe3O4
6.下列物质的水溶液在空气中小心加热,蒸干至质量不再减少,能得到较纯净的原溶质的是①CuSO4 ②FeSO4 ③Ca(HCO3)2 ④NH4HCO3 ⑤KMnO4 ⑥FeCl3A.全部 B.仅①②C.仅①⑤ D.仅①
题组三 广义水解 7.(2022·辽宁省实验中学高二期中)海上作战经常使用化学烟雾弹,该烟雾弹通过水解反应产生大量烟雾。下列物质适合用作海上烟雾弹的是A.SiCl4 D.NaCl
8.CaC2、ZnC2、Al4C3、Mg2C3、Li2C2等都同属于离子型碳化物,判断下列水解反应中所得产物正确的是A.ZnC2水解生成乙烷(C2H6)B.Al4C3水解生成甲烷(CH4)C.Mg2C3水解生成丙烷(C3H8)D.Li2C2水解生成乙烯(C2H4)
9.已知BeCl2+Na2BeO2+2H2O===2NaCl+2Be(OH)2↓,下列说法正确的是A.BeCl2溶液的pH
相关课件
这是一份高中化学人教版 (2019)选择性必修1第三节 盐类的水解评优课ppt课件,文件包含第三章第三节第1课时盐类的水解pptx、第三章第三节第1课时盐类的水解专练docx、第三章第三节第1课时盐类的水解教师版docx、第三章第三节第1课时盐类的水解学习笔记docx、盐溶液的酸碱性mp4等5份课件配套教学资源,其中PPT共60页, 欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1实验活动3 盐类水解的应用课文配套课件ppt,共25页。PPT课件主要包含了CaCO3,CaO,蒸干并灼烧,如3NH4Cl,无固体,②③④⑤⑥等内容,欢迎下载使用。
这是一份化学选择性必修1第三节 盐类的水解课前预习课件ppt,共37页。PPT课件主要包含了盐类水解的应用,HXHYHZ,H2SO4,NH3·H2O,CH3COOH,NaOH+H2↑,LiOH+NH3↑,HIO+HBr,HIO3+5HF,NH3+HClO等内容,欢迎下载使用。










