

















初中化学课题3 溶液的浓度优质ppt课件
展开本讲PPT内嵌3个高清视频,点击按钮 即可播放,使用时可删除本页。
若软件版本太低,可能不兼容,导致视频无法正常播放。下载最新版OFFICE,或者WPS,即可正常播放。
实验9-7:三种浓稀不同的硫酸铜溶液实验9-8:配制两种质量分数不同的氯化钠溶液溶质的质量分数与化学方程式的综合计算
1.掌握溶液中溶质的质量分数的概念。2.学会计算有关溶质的质量分数。3.学会配制一定溶质质量分数的溶液。
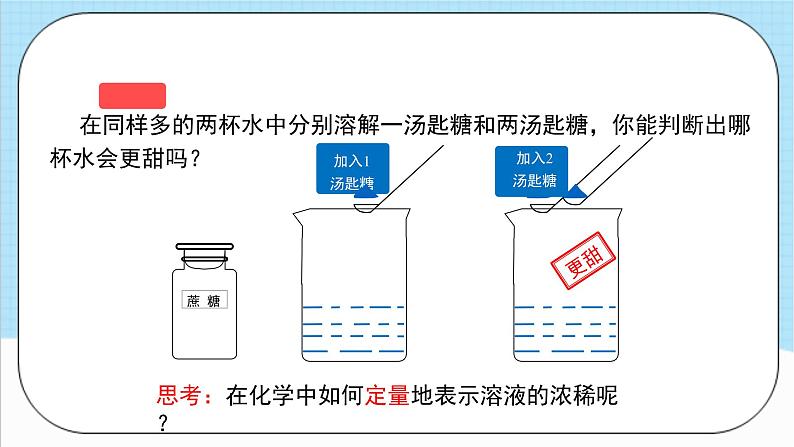
在同样多的两杯水中分别溶解一汤匙糖和两汤匙糖,你能判断出哪杯水会更甜吗?
思考:在化学中如何定量地表示溶液的浓稀呢?
实验9-7:三种浓稀不同的硫酸铜溶液
交流讨论:这三种溶液中,哪种溶液最浓?哪种溶液最稀?你的判断依据是什么?
根据三种溶液的颜色深浅。颜色深的溶液较浓,颜色浅的溶液较稀。
表示溶液浓度的方法很多,这里主要介绍 溶质的质量分数。
在实际应用中,常常要准确知道一定量的溶液里所含溶质的量,即溶液的浓度。
溶液中溶质的质量分数就是溶质质量与溶液质量之比。
溶质质量分数——定量表示溶液的浓度
实验9-8:配制两种质量分数不同的氯化钠溶液
交流讨论:根据溶质的质量分数的公式,能不能得到溶质和溶剂的质量?
溶质质量=溶液质量×溶质的质量分数
溶液质量=溶质质量+溶剂质量
溶剂质量=溶液质量-溶质质量
【例题1】在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150 kg的这种溶液,需要氯化钠和水的质量各是多少?
解:溶质质量=溶液质量×溶质的质量分数 =150 kg×16% =24 kg 溶剂质量=溶液质量-溶质质量 = 150 kg-24 kg = 126 kg答:配制150 kg质量分数为16%的氯化钠溶液需24 kg氯化钠和126 kg水。
【例题2】化学实验室现有质量分数98%的浓硫酸,但在实验中常需要用较稀的硫酸。要把50g上述浓硫酸稀释为质量分数为20%的硫酸,需要水的质量是多少?
解:设稀释后溶液的质量为x
50g ×98% = x×20%
答:需要水的质量195g。
需要水的质量= 245 g– 50g = 195g
【分析】稀释前溶质质量=稀释后溶质质量
练习:配制10%的硫酸溶液98g,需要98%的浓硫酸(密度为1.84g/mL)的体积是多少?
解:设需要98%的浓硫酸的体积为V。
V×1.84g/mL×98%=98g×10%
答:需要98%的浓硫酸的体积为5.4mL。
交流讨论:已知20℃时,氯化钠的溶解度是36g。有人说:“20℃时,氯化钠饱和溶液中溶质的质量分数为36%。”这种说法对吗?为什么?
100 g + 36 g
溶质质量分数与溶解度的关系
练习:在20℃时,Ca(OH)2的溶解度是0.17g,问此温度下将1g Ca(OH)2固体放入200g水中,充分溶解后,所得溶液的溶质质量分数是多少?
该温度下200g水中只能溶解0.34g Ca(OH)2固体,溶液即饱和。
答:所得溶液的溶质质量分数是0.17%。
【例题3】40g10%NaOH溶液跟多少克10%盐酸完全反应?反应后溶液的溶质的质量分数是多少?
解:设稀盐酸的质量为X,生成的NaCl的质量为Y
NaOH + HCl = NaCl + H2O
40g×10% X ×10% Y
40 36.5 58.5
反应后溶液的溶质的质量分数=
溶质的质量分数与化学方程式的综合计算
有关溶质的质量分数与化学方程式相结合的计算
解该类题时,一定要正确写出该反应的化学方程式。
有溶液参与的反应,只是溶液中的溶质参与了反应。
反应后溶液的质量=反应前的总质量-生成气体的质量- 生成沉淀的质量-不溶物的质量。
练习:100g某硫酸恰好与13g锌完全反应。试计算这种硫酸中溶质的质量分数。
解:设硫酸中溶质的质量为X
Zn + H2SO4 = ZnSO4 + H2↑
65 98
13g X
答:这种硫酸溶液中溶质的质量分数为19.6%。
实验演示——配制50g溶质质量分数为6%的氯化钠溶液
计算:配制50g溶质质量分数为6%的氯化钠溶液,需要氯化钠 g;水 g。
称量:用天平称量所需的氯化钠,放入烧杯中;
溶解:用玻璃棒搅拌,使氯化钠溶解。
量取:用量筒量取所需的水(水的密度近似看做1g/cm3),倒入盛有氯化钠的烧杯中。
实验室中配制一定溶质质量分数的溶液
思考:1.配置一定溶质质量分数的溶液需要用到哪些仪器?2.若所配溶液的溶质质量分数偏大或偏小,你认为可能的原因有哪些?
溶质质量与溶液质量之比
溶质质量分数的简单计算
一定溶质质量分数溶液的配制
1. 对“16%的食盐溶液”的含义解释错误的是( )A.100 g食盐溶液中溶解了l6 g食盐 B.将食盐与水按16﹕84的质量比配成的溶液C.将32 g食盐溶解于168 g水中所得到的溶液 D.100 g水中溶解了16 g食盐
2.现有一杯60℃的硝酸钾饱和溶液,下列操作会导致硝酸钾的质量分数减小的是( )
A. 升温至80℃ B. 恒温蒸发部分溶剂C. 加入一定量的硝酸钾D. 加入一定量的氯化钠
3.现需要将溶质质量分数为40%的氢氧化钠溶液稀释为40 g溶质质量分数为5%的氢氧化钠溶液。此时,需要水的体积为( )A.38 mL B.36 mL C.35 mL D.37 mL
化学九年级下册课题3 溶液的浓度评优课ppt课件: 这是一份化学九年级下册<a href="/hx/tb_c76882_t3/?tag_id=26" target="_blank">课题3 溶液的浓度评优课ppt课件</a>,共28页。PPT课件主要包含了溶液的浓度,20ml水,44%,09%,完全溶解,≈265%等内容,欢迎下载使用。
人教版九年级下册课题 1 金属材料获奖课件ppt: 这是一份人教版九年级下册<a href="/hx/tb_c9861_t3/?tag_id=26" target="_blank">课题 1 金属材料获奖课件ppt</a>,文件包含人教版化学九年级下册81《金属材料》课件pptx、人教版化学九年级下册81《金属材料》教案docx、人教版化学九年级下册81《金属材料》导学案原卷版docx、人教版化学九年级下册81《金属材料》分层作业原卷版docx、人教版化学九年级下册81《金属材料》分层作业解析版docx、人教版化学九年级下册81《金属材料》导学案解析版docx、1拿破仑加冕为什么要用铝制皇冠mp4、2实验8-1比较合金和纯金属的硬度mp4等8份课件配套教学资源,其中PPT共32页, 欢迎下载使用。
人教版课题3 溶液的浓度完整版课件ppt: 这是一份人教版课题3 溶液的浓度完整版课件ppt,文件包含93-2溶液的浓度第2课时pptx、93-2教学设计溶液的浓度第2课时docx、93-2练习·能力提升溶液的浓度第2课时docx、93-2练习·基础巩固溶液的浓度第2课时docx、93-2练习·素能拓展溶液的浓度第2课时docx、93-2预习导学溶液的浓度第2课时docx等6份课件配套教学资源,其中PPT共17页, 欢迎下载使用。













