



人教版 (2019)必修 第一册第三节 氧化还原反应评课ppt课件
展开1.通过具体实例识别氧化剂和还原剂。2.理解氧化反应、还原反应、氧化剂、还原剂、氧化性、还原性的概念。
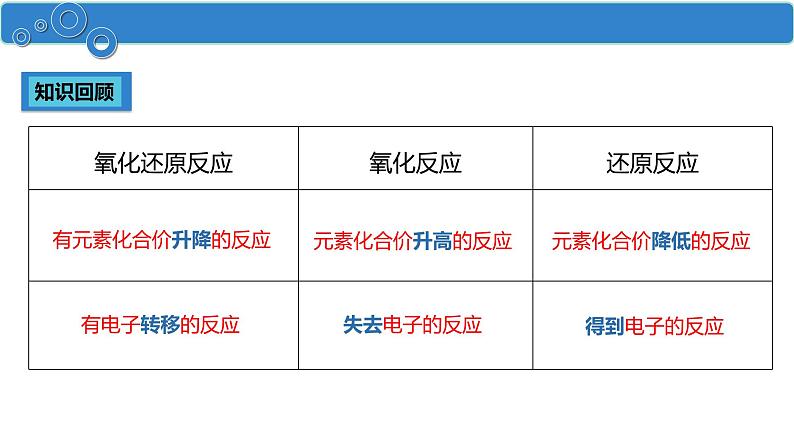
有元素化合价升降的反应
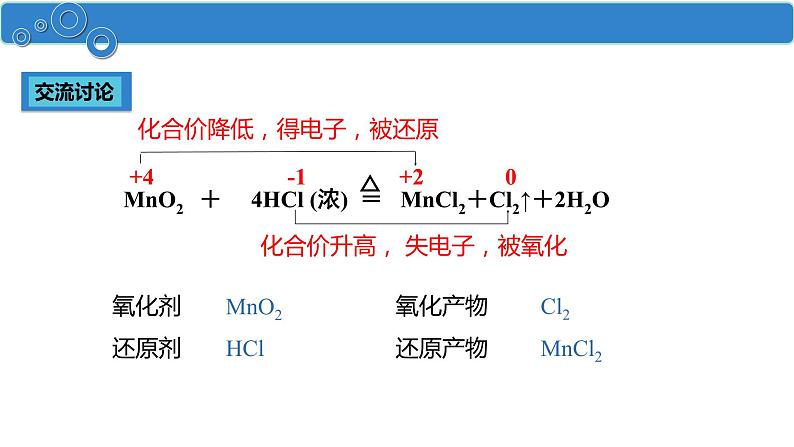
+4 -1 +2 0
化合价升高, 失电子,被氧化
化合价降低,得电子,被还原
还原剂:在氧化还原反应中,所含的某种元素的化合价升高的反应物。
氧化剂:在氧化还原反应中,所含的某种元素的化合价降低的反应物。
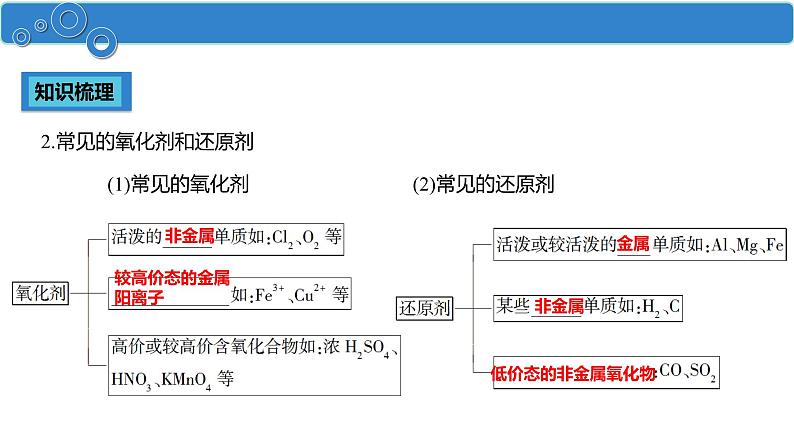
2.常见的氧化剂和还原剂
(2)与元素价态的关系
氧化性:氧化剂所表现出的得电子的性质。
还原性:还原剂所表现出的失电子的性质。
元素处于最高价态时只有氧化性;
元素处于最低价态时只有还原性;
元素处于中间价态时既有氧化性,也有还原性。
1.根据反应方程式来比较:
三、物质氧化性与还原性的比较
【典题例证】有A、B、C、D四种物质,已知它们能发生下列反应:
①A2++B=== B2++A ②A2++C===C2++A③B2++C=== C2++B ④C2++D===D2++C由此可推知,各物质的氧化性、还原性强弱顺序正确的是( )A.氧化性:A2+>B2+>C2+>D2+B.氧化性:D2+>C2+>B2+>A2+C.还原性:A>B>C>DD.还原性:D>C>B>A
2.根据金属活动顺序:
(3)元素处于中间价态,则既有氧化性又有还原性
(2)元素处于低价态具有还原性,价态越低,还原性越强
(1)元素处于高价态具有氧化性,价态越高, 氧化性越强
3.根据元素的化合价来判断:
从左到右,单质的还原性逐渐减弱;对应的阳离子的氧化性逐渐增强。
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
四、生产、生活中的氧化还原反应
1.在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是_________________,只有还原性的是_________________,既有氧化性又有还原性的是______________。
Fe3+、Mg2+、H+
2.在含有Cu(NO3)2、Mg(NO3)2、AgNO3的溶液中加入适量锌粉,首先置换出的是( )
A.Mg B.Cu C.Ag D.H2
3.已知下列三个离子反应方程式如下:
①X2++Y===X+Y2+②Y2++W===W2++Y③W2++Z===Z2++W则氧化性最弱的粒子是( )A.X2+B.Y2+ C.W2+D.Z2+
高中化学第三节 氧化还原反应课堂教学课件ppt: 这是一份高中化学<a href="/hx/tb_c161975_t3/?tag_id=26" target="_blank">第三节 氧化还原反应课堂教学课件ppt</a>,共30页。PPT课件主要包含了考纲要求,氧化剂和还原剂,1双线桥法,由反应物指向生成物,得到2×2e-,失去4e-,得到2×3e-,失去3×2e-,2单线桥法,元素化合价的判断等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第三节 氧化还原反应教学课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第三节 氧化还原反应教学课件ppt,共14页。PPT课件主要包含了素养发展目标,氧化剂,还原剂,氧化产物,还原产物,MnO2,HCl,MnCl2,Cl2,思考交流等内容,欢迎下载使用。
化学必修 第一册第三节 氧化还原反应背景图课件ppt: 这是一份化学必修 第一册第三节 氧化还原反应背景图课件ppt,共19页。PPT课件主要包含了维生素C,还原产物,氧化剂,归纳总结,练一练,FeCl3,FeCl2,Cl2,还原性,氧化性等内容,欢迎下载使用。













