







- 1.3《电解质的电离》课件+教案 课件 45 次下载
- 1.4《离子反应》课件+教案 课件 54 次下载
- 1.6《氧化剂和还原剂》课件+教案 课件 40 次下载
- 1.7《氧化还原反应的配平》课件+教案 课件 42 次下载
- 2.1《金属钠的性质和应用》课件+教案 课件 39 次下载
高中化学人教版 (2019)必修 第一册第一章 物质及其变化第三节 氧化还原反应评优课ppt课件
展开人教版化学科高一年必修一
《氧化还原反应》教学设计
课题 | 氧化还原反应(第一课时) | 课型 | 新授课 |
教学目标 | 1.能从化合价的变化,认识并建立氧化还原反应的概念。 | ||
2.能从典型化学反应的分析,理解氧化还原反应的本质是电子转移 | |||
3.通过对氧化还原反应概念的演变,学会科学探究学习化学的品质 | |||
教学重难点 | 重点:氧化还原反应的宏观特征 | ||
难点:氧化还原反应的微观本质 | |||
教学环节 | 教学过程 | ||
课堂导入 | 【导入】思考与讨论:根据初中所学知识,判断物质发生的是氧化反应还是还原反应? CO CO2 得氧 氧化反应 Fe2O3 Fe 失氧 还原反应 【总结】初中我们便是从物质得失氧来判断发生氧化或者还原反应的。 | ||
课
程
学
习
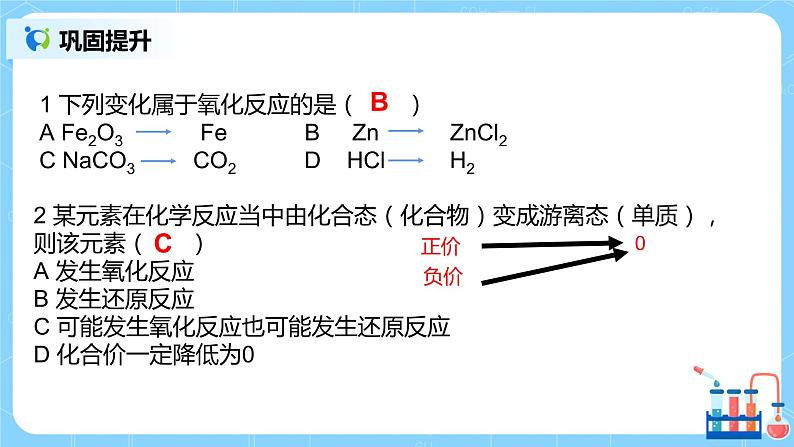
| 一、氧化还原反应 【思考与交流】根据你所学的知识,判断该反应属于哪种反应类型? 2FeCl3+Cu==2FeCl2+CuCl2 预设答案:不是置换反应、是离子反应、是氧化还原反应 【师】根据学生答案,进行对化学反应的分类归纳总结 1.思考:没有得氧失氧,为什么也属于氧化还原反应? 总结:氧化还原反应的特征:反应前后(同种)元素的化合价发生变化 2.氧化反应:有元素化合价升高的反应。 还原反应:有元素化合价降低的反应。 氧化反应和还原反应是在一个反应中同时发生的 3【巩固提升】1 下列变化属于氧化反应的是( ) A Fe2O3 Fe B Zn ZnCl2 C NaCO3 CO2 D HCl H2 2 某元素在化学反应当中由化合态(化合物)变成游离态(单质),则该元素( ) A 发生氧化反应 B 发生还原反应 C 可能发生氧化反应也可能发生还原反应 D 化合价一定降低为0
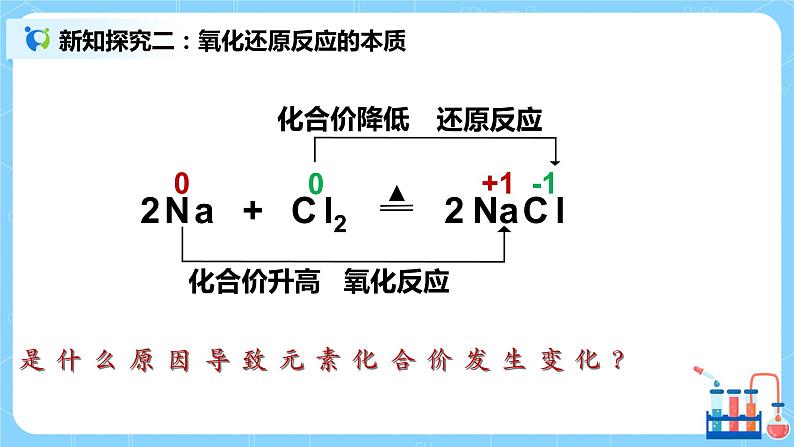
二、氧化还原反应的本质 1.2Na + Cl2 === 2NaCl 【思考】是什么原因导致元素化合价发生变化? 预设答案:电子的得失 2. H2 + Cl2 ==== 2HCl 【思考】还是得失电子导致元素化合价发生变化吗? 预设答案:共用电子对偏离氢,偏向氯;共用电子对偏移 3. 本质:电子的转移 ①电子的得失 ②电子对的偏移 【注意】氧化还原反应中,化合价有升必有降 升降总数必相等 电子有得必有失,得失电子总数相等 归纳口诀:升失氧 降得还 4.四种基本类型反应与氧化还原反应的关系 ①置换反应都是氧化还原反应; ②复分解反应都不是氧化还原反应; ③有单质参与的化合反应和分解反应都是氧化还原反应。 5.【巩固提升】有单质参与的化学反应,一定是氧化还原反应吗? 预设答案:不是,同素异形体的转化属于化学变化,但反应前后化合价不变,是非氧化还原反应。 四、课堂练习 1.下列属于氧化还原反应的是( ) A. B. C. D. 2.世界卫生组织()将列为A级高效安全灭菌消毒剂,中氯元素的化合价为( ) A.-1 B.0 C.+1 D.+2 3下列说法正确的是( ) A.氧化还原反应的本质是元素化合价发生变化 B.发生氧化反应的物质是得到电子的物质 C.氧化反应和还原反应同时发生 D.物质所含元素化合价升高的反应是还原反应 | ||
课堂 小结 | 氧化还原反应 1.特征:有元素化合价的变化 2.本质:发生电子的转移(得失/偏移) 3.四种基本反应类型和氧化还原反应的关系 | ||
板书设计 | 氧化还原反应 1.特征:有元素化合价的变化 2.本质:发生电子的转移(得失/偏移) 3.四种基本反应类型和氧化还原反应的关系 | ||
教学反思 | 氧化还原反应是高中化学概念的一个重要内容,也是高考考察的一个重点,是一个贯穿整个高中阶段的重难点内容,在教学过程中,应该重视学生对于概念的理解,并及时练习巩固强化。 | ||
高中人教版 (2019)第三节 氧化还原反应教学ppt课件: 这是一份高中人教版 (2019)第三节 氧化还原反应教学ppt课件,共35页。PPT课件主要包含了素养要求,思想在线,你会吗,思想点拨,学习小结,课堂检测等内容,欢迎下载使用。
氧化还原反应的有关计算: 这是一份氧化还原反应的有关计算,共28页。PPT课件主要包含了高考怎么考,浅蓝色至无色,75g等内容,欢迎下载使用。
人教版 (2019)必修 第一册第三节 氧化还原反应优秀ppt课件: 这是一份人教版 (2019)必修 第一册第三节 氧化还原反应优秀ppt课件,文件包含17《氧化还原反应的配平》课件pptx、17《氧化还原反应的配平》教案docx等2份课件配套教学资源,其中PPT共16页, 欢迎下载使用。














