




高中第一节 硫及其化合物教课ppt课件
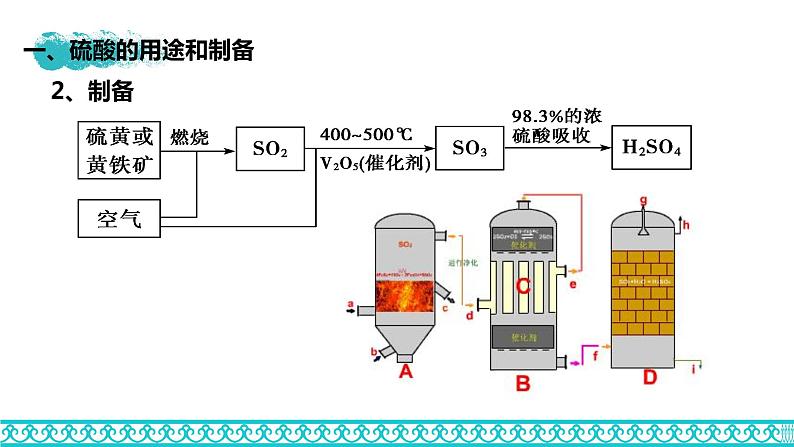
展开生 产 化 肥农 药 等
纯净的浓硫酸是一种无色黏稠的油状液体,溶于水时放出大量的热,稀释浓硫酸时应 。
将浓硫酸沿玻璃棒缓慢注入水中,并不断搅拌
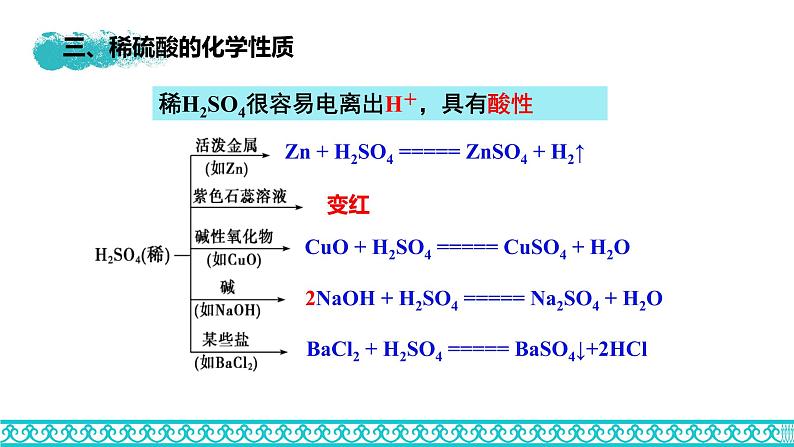
稀H2SO4很容易电离出H+,具有酸性
Zn + H2SO4 ===== ZnSO4 + H2↑
CuO + H2SO4 ===== CuSO4 + H2O
2NaOH + H2SO4 ===== Na2SO4 + H2O
BaCl2 + H2SO4 ===== BaSO4↓+2HCl
浓硫酸能吸收存在于周围环境中的水分,气体、液体中的水分子,故常用作 。是 性质。
浓硫酸能不能干燥所有气体?
还原性气体,如HBr、HI、H2S
浓硫酸能将蔗糖、纸张、棉布和木材等有机物中的氢元素和氧元素按 的组成比脱去。是 性质。
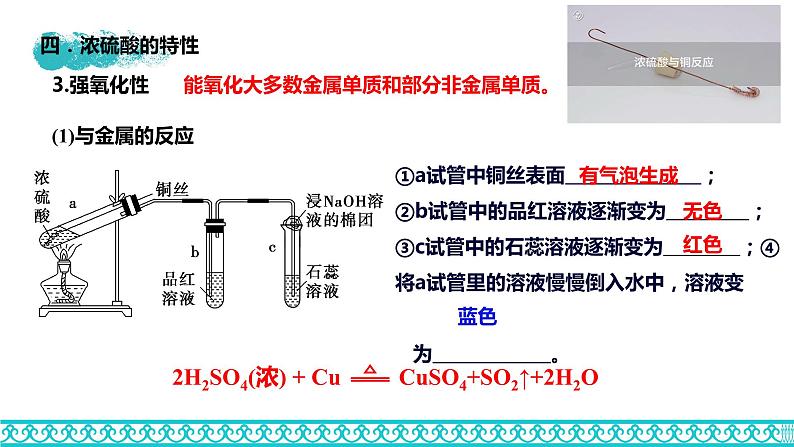
能氧化大多数金属单质和部分非金属单质。
①a试管中铜丝表面 ;②b试管中的品红溶液逐渐变为 ;③c试管中的石蕊溶液逐渐变为 ;④将a试管里的溶液慢慢倒入水中,溶液变 为 。
常温下铁和铝会和浓硫酸反应发生钝化,因此,常用铁制容器盛装浓硫酸
2.浓H2SO4和浓HNO3
在加热时,浓硫酸与木炭发生反应:
石膏 CaSO4∙2H2O
熟石膏 2CaSO4∙2H2O
胆矾 CuSO4∙5H2O
制作各种模型和医疗用的石膏绷带;调节水泥的硬化速率
检验水的存在;制作波尔多液
1.下列现象与用途和浓硫酸的脱水性有关的是( ) A.浓硫酸可作氯气的干燥剂 B.浓硫酸加到蔗糖中,蔗糖变黑 C.浓硫酸加到胆矾上,蓝色晶体变成白色粉末 D.浓硫酸与铜反应制取二氧化硫
3.实验室常用下图装置进行铜与浓硫酸反应的实验。下列有关实验现象的描述 或试剂的选用错误的是( ) A.甲试管内溶液变为蓝色 B.乙试管中品红溶液红色褪去 C.棉花上喷入的溶液可能为氢氧化钠溶液 D.棉花上喷入的溶液可能为饱和碳酸钠溶液
2.浓H2SO4在实现下列物质的转化过程中,既表现出氧化性,又表现出酸性的是( ) ①Cu→CuSO4 ②C→CO2 ③FeO→Fe2(SO4)3 ④Fe2O3→Fe2(SO4)3 A.①③ B.②④ C.①④ D.②③
(1)实验探究在三支试管中分别加入少量稀硫酸、Na2SO4溶液和Na2CO3溶液,然后各滴入几滴BaCl2溶液,观察现象。再分别加入少量稀盐酸,振荡,观察现象。
沉淀溶解,且有气泡生成
Q1:滴入BaCl2溶液有白色沉淀生成,能否证明有SO42-存在?
Q2:滴入BaCl2溶液有白色沉淀生成,还可能有哪些离子存在?
Q3:如何排除这些离子的干扰?
(2)实验结论 检验SO42-的正确操作方法如下:
发生反应的离子方程式为:
Ba2+ + SO42- ===== BaSO4↓
①被检液 → 加足量稀盐酸酸化
②取清液 → 滴加BaCl2溶液
1.下列检验试样中有无SO42-的操作及结论正确的是( ) A. 滴加BaCl2有白色沉淀生成,一定有SO42- B. 加盐酸酸化的BaCl2溶液有白色沉淀生成,一定有SO42- C. 滴加硝酸酸化的AgNO3溶液没有白色沉淀生成,一定没有SO42- D. 先加盐酸无明显现象,再加BaCl2溶液有白色沉淀生成,一定有SO42-
2.下列说法正确的是( ) A.浓H2SO4滴在湿润的蓝色石蕊试纸上,试纸先变红,然后褪色,最后变黑, 说明 浓H2SO4具有酸性、氧化性和吸水性 B. 样品 无明显现象 出现白色沉淀,说明样品中含SO42- C. 常温下浓 H2SO4能用铁制容器盛装,说明浓 H2SO4与Fe不反应 D. 样品 得到使澄清石灰水变浑浊的气体,说明样品中含SO32-或HSO3-
3.为了验证浓硫酸和木炭粉在加热条件下产生的气体产物,某同学选用了如图所 示的实验装置。下列说法错误的是( ) A.B装置用来检验产物中是否有水蒸气生成 B.C装置用来检验产物中是否有SO2生成 C.D装置中溴水褪色,则说明SO2具有漂白性 D.F装置用来检验产物中是否有CO2生成
4.某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。
实验中某同学将a g铜片和12 mL 18 ml·L-1的浓硫酸放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余。请回答:(1)请写出Cu与浓硫酸反应的化学方程式: 。
(2)①装置E中试管D内盛品红溶液,当C中气体收集满后,D中有可能观察到的现象是 。实验装置E中D有可能造成环境污染,试用最简单方法加以解决(实验用品自选) 。
用浸有NaOH溶液的棉花团塞在试管口
②装置B的作用是储存多余的气体。当D处有明显现象后,关闭旋塞K,移去酒精灯,但 由于余热的作用,A处仍有气体产生,此时B中现象是 。B中应放置的液体是________(填字母)。A.饱和Na2SO3溶液 B.酸性KMnO4溶液 C.浓溴水 D.饱和NaHSO3溶液
试剂瓶中液面下降,长颈漏斗中液面上升
高中化学人教版 (2019)必修 第二册第一节 硫及其化合物教学ppt课件: 这是一份高中化学人教版 (2019)必修 第二册第一节 硫及其化合物教学ppt课件,共33页。PPT课件主要包含了浓硫酸的物理性质,硫酸的化学性质,物理变化,化学变化,小试牛刀,SO2,浓硫酸具有强氧化性,物质中含有H2O,作干燥剂,常见的硫酸盐等内容,欢迎下载使用。
化学必修 第二册第一节 硫及其化合物课文内容ppt课件: 这是一份化学必修 第二册第一节 硫及其化合物课文内容ppt课件,共28页。PPT课件主要包含了考纲要求,硫酸的工业制备,硫酸的性质,实验探究,a与金属单质的反应,硫酸根离子的检验等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第二册第一节 硫及其化合物背景图ppt课件: 这是一份高中化学人教版 (2019)必修 第二册第一节 硫及其化合物背景图ppt课件,文件包含人教版高中化学必修第二册第5章第1节基础课时2硫酸硫酸根离子的检验课件ppt、人教版高中化学必修第二册第5章第1节基础课时2硫酸硫酸根离子的检验学案doc等2份课件配套教学资源,其中PPT共60页, 欢迎下载使用。













