






人教版 (2019)必修 第二册第三节 环境保护与绿色化学优质ppt课件
展开【考纲要求】1.硫酸的强酸性和浓硫酸三大特性。2.硫酸根离子的检验。
重点难点浓硫酸三大特性、硫酸根离子的检验。
1、纯H2SO4是 液体。沸点高,难挥发
应用:高沸点物质制取低沸点物质
(2016·上海高考)NaCl与浓H2SO4加热可制HCl,推测NaBr与浓H2SO4加热可制HBr
将浓H2SO4沿器壁慢慢注入水中,并用玻璃棒不断搅拌
2、能与水以 互溶,溶解时可放出大量的热。
浓H2SO4稀释的方法
常见的浓硫酸质量分数为98%,密度为1.84g/cm3,则 c=
(二)稀H2SO4具有酸的通性
硫酸是强电解质,在水溶液中的电离方程式为 H2SO4===2H++SO42-,能与指示剂、金属、碱性氧化物、碱、盐等物质发生反应。
蔗糖逐渐变黑,体积膨胀,形成疏松多孔的海绵状的炭。产生无色刺激性气味的气体
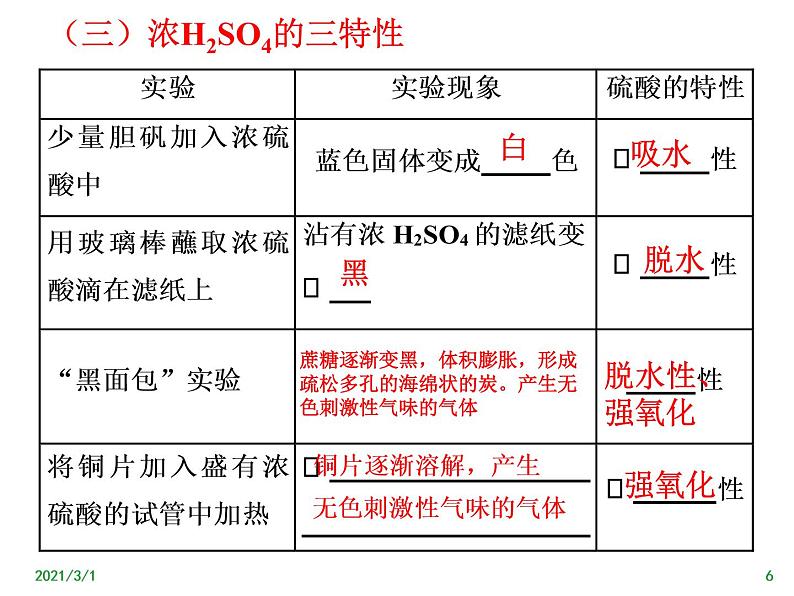
(三)浓H2SO4的三特性
1、吸水性利用浓H2SO4的吸水性,其常用作__________。
2、脱水性浓H2SO4能够将有机物里的氢、氧元素按原子个数2∶1的比例脱去。
[练习2] 将一定量的锌与100 mL 18.5 ml/L浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6 L(标准状况).将反应后的溶液稀释至1 L,测得溶液的pH=1,则下列叙述中错误的是 ( )A.气体A为SO2和H2的混合物B.气体A中SO2与H2的体积比为5∶1C.反应中共消耗Zn 97.5 gD.反应中共转移电子3 ml
②常温下,铁、铝遇浓H2SO4钝化,可用铝(或铁)槽车 运输浓硫酸。③浓硫酸还可与某些还原性化合物反应。
2HBr + H2SO4 = Br2 + SO2 ↑ + 2H2O
二、掌握SO42-、SO32-的检验方法
化学必修 第二册第一节 硫及其化合物课文内容ppt课件: 这是一份化学必修 第二册第一节 硫及其化合物课文内容ppt课件,共28页。PPT课件主要包含了考纲要求,硫酸的工业制备,硫酸的性质,实验探究,a与金属单质的反应,硫酸根离子的检验等内容,欢迎下载使用。
2020版高考化学一轮复习考点备考课件4.3.2硫酸硫酸根离子的检验 (含解析): 这是一份2020版高考化学一轮复习考点备考课件4.3.2硫酸硫酸根离子的检验 (含解析),共7页。PPT课件主要包含了速查速测,钝化现象,大量水,还可能存在Ag+,典例剖析,变稀后反应不再发生,反思归纳等内容,欢迎下载使用。
2023届高三化学高考备考一轮复习 硫酸 硫酸根离子的检验课件: 这是一份2023届高三化学高考备考一轮复习 硫酸 硫酸根离子的检验课件













