



- 第一章第3节氧化还原反应第3课时 课件—2021-2022学年人教版(2019版)高一化学必修(第一册) 课件 3 次下载
- 第一章第3节 氧化还原反应第2课时 课件—2021-2022学年人教版(2019版)高一化学必修(第一册) 课件 3 次下载
- 第一章第2节离子反应第2课时 课件—2021-2022学年人教版(2019版)高一化学必修(第一册) 课件 7 次下载
- 第一章第2节离子反应第1课时 课件—2021-2022学年人教版(2019版)高一化学必修(第一册) 课件 5 次下载
- 第二章第1节钠及其化合物第1课时 课件—2021-2022学年人教版(2019版)高一化学必修(第一册) 课件 2 次下载
人教版 (2019)必修 第一册第三节 氧化还原反应完整版课件ppt
展开世界是由物质构成的,目前人类发现和合成的物质已经超过1亿种。对于这么多的物质和更为丰富的化学变化,人们是怎样认识和研究的呢?
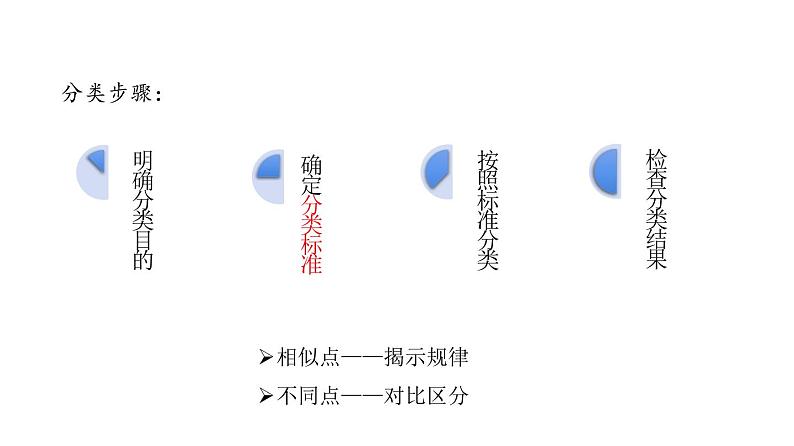
图书馆,书籍目录超市化学实验室药品柜电子购物网络信息垃圾分类其他…
相似点——揭示规律不同点——对比区分
(1)只由一种元素组成的物质一定是纯净物吗?
提示 只由一种元素组成的物质不一定是纯净物,例如氧元素的同素异形体O2和O3形成的混合气体,只由氧元素组成,不是纯净物。
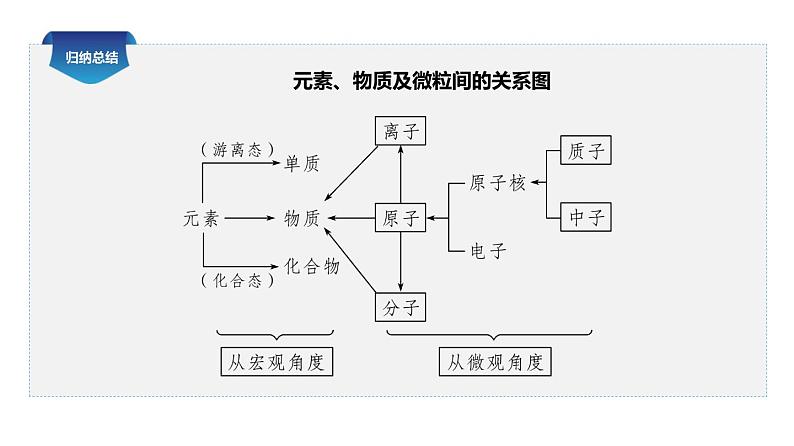
(2)从宏观上看物质由元素组成,从微观上看构成物质的微粒有哪些?
提示 构成物质的微粒有原子、分子或离子。如金刚石由原子构成;CO、CO2、H2、H2O等均由分子构成;NaCl、CaCO3等均由离子构成。
元素、物质及微粒间的关系图
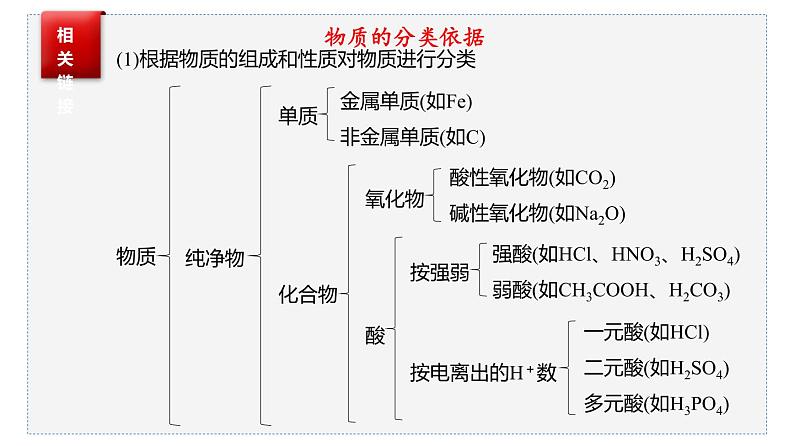
(1)根据物质的组成和性质对物质进行分类
金属单质(如Fe)非金属单质(如C)
酸性氧化物(如CO2)碱性氧化物(如Na2O)
强酸(如HCl、HNO3、H2SO4)弱酸(如CH3COOH、H2CO3)
一元酸(如HCl)二元酸(如H2SO4)多元酸(如H3PO4)
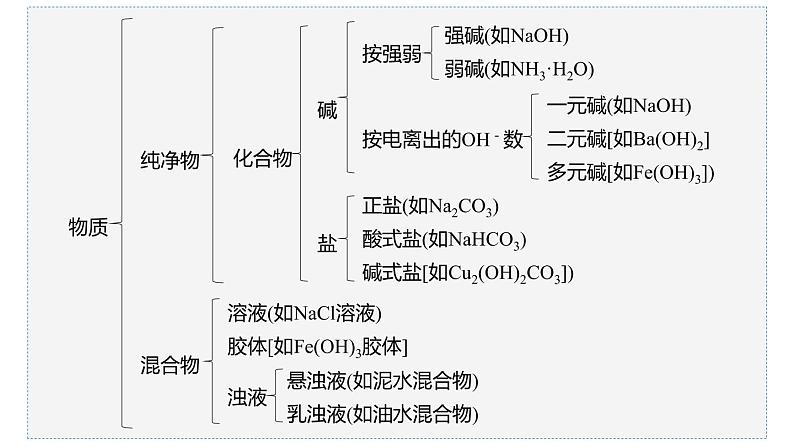
强碱(如NaOH)弱碱(如NH3·H2O)
一元碱(如NaOH)二元碱[如Ba(OH)2]多元碱[如Fe(OH)3])
正盐(如Na2CO3)酸式盐(如NaHCO3)碱式盐[如Cu2(OH)2CO3])
溶液(如NaCl溶液)胶体[如Fe(OH)3胶体]
悬浊液(如泥水混合物)乳浊液(如油水混合物)
(2)分类的标准不同,同一物质可以属于不同的类别:如NaHSO4可以属于纯净物、钠盐、硫酸氢盐、酸式盐、含氧酸盐、水溶性盐等。
物质的分类依据--------树状分类法
指出右图中序号所示物质的分类依据:①_____________________;②_____________________;③___________;④_________________;⑤_____________。
物质的分类依据--------交叉分类法
物质的分类依据------氧化物的分类
(1)氧化物的分类方法
(2)各类氧化物之间的关系
(1)①酸、②碱、③盐、④氧化物四类物质的组成一定含有氧元素的是②④( )(2)纯碱是碱( )(3)CuSO4·5H2O属于混合物( )(4)H2SO4既属于含氧酸又属于二元酸,这种分类方法是树状分类法( )
(1)非金属氧化物一定是酸性氧化物吗?酸性氧化物一定是非金属氧化物吗?
提示 非金属氧化物不一定是酸性氧化物,如CO、NO。酸性氧化物不一定是非金属氧化物,如Mn2O7。
(2)金属氧化物一定是碱性氧化物吗?碱性氧化物一定是金属氧化物吗?
提示 金属氧化物不一定是碱性氧化物,如Mn2O7。碱性氧化物一定是金属氧化物。
(3)碳元素的物质家族如下表所示,请指出各物质的常见类别及碳元素的化合价:
(1)分类是根据研究对象的共同点和差异点,将它们区分为不同种类和层次的科学方法。(2)物质的分类标准不同,其分类方式不同。对物质及其变化既可以从物质的组成和性质等宏观的角度进行分类,也可从物质的构成和参加化学反应的粒子等微观的角度分类。
常见两种分类法——树状分类法
对同一分类进行再分类,系统性强,适合层次包含关系。
常见两种分类法——交叉分类法
至少同时运用两种分类标准,弥补单一标准的不足。
任务一:物质分类的依据
探究“单质-氧化物-酸(碱)-盐”之间的转化规律【任务】将初中所学代表性物质进行分类。以Ca、CaO、Ca(OH)2、CaCO3为例探究金属单质、碱性氧化物、碱、盐之间的转化规律;以C、CO2、H2CO3、CaCO3为例探究非金属单质、酸性氧化物、酸、盐之间的转化规律。
2Ca+O2===2CaO CaO+H2O===Ca(OH)2 Ca(OH)2+CO2===CaCO3↓+H2O
CO2+H2O===H2CO3Ca(OH)2+H2CO3===CaCO3↓+2H2O
[微点拨]CO2是酸性氧化物,CO不是酸性氧化物,二者都属于非金属氧化物。
解析: 题干中三种物质均是纯净物且是化合物,而B项中O2为单质;C项为CO和H2的混合物;D项为混合物。
回顾初中所学的溶液、悬浊液、乳浊液,混合物如何分类?
这些混合物都是由一种物质分散到另一种物质中形成的。
二、分散系 1、概念: 一种(或多种)物质分散到另一种(或多种)物质中所形成的混合物,叫做分散系。
分散系中被分散的物质。
分散系中容纳分散质的物质。
3.分散系的分类及其依据(1)按分散质和分散剂的状态不同,共有____种分散系。
(2)当分散剂是水或者其他液体时,根据分散质粒子直径的大小,分散系可分为三类:①分散质粒子直径小于1 nm的分散系是______;②分散质粒子直径大于100 nm的分散系是______;③分散质粒子直径在1~100 nm之间的分散系是______。
根据分散质粒子直径的大小,分散系可分为三类:①分散质粒子直径小于1 nm的分散系是______;②分散质粒子直径大于100 nm的分散系是______;③分散质粒子直径在1~100 nm之间的分散系是______。
(2)按分散质粒子直径大小
常见的胶体有:云、烟、雾、豆浆、牛奶、墨汁、碳素墨水、有色玻璃、淀粉溶液、蛋白质溶液等。
(1)分散系的组合方式及其实例
4.氢氧化铁胶体的制备和性质(1)氢氧化铁胶体的制备①制备实验:在小烧杯中加入40 mL_______,加热至_____,向沸水中慢慢滴入5~6滴FeCl3______溶液,继续煮沸至溶液呈_____色,停止加热。即可得到氢氧化铁胶体。②反应的化学方程式为____________________________________。
实验:把盛有硫酸铜溶液和氢氧化铁胶体的烧杯置于暗处,分别用红色激光笔照射烧杯中的液体,在与光束垂直的方向进行观察,记录现象。
丁达尔效应:当光束通过胶体时,会形成一条光亮的“通路”。
丁达尔效应的应用:区分胶体和溶液
将泥沙、淀粉溶胶和氯化钠溶液的混合物分离。原理和操作?
利用半透膜把胶体中混有的离子或分子从胶体溶液里分离的操作,叫做渗析。
如何证明淀粉未透过半透膜?如何证明离子透过半透膜?如何证明两者已完全分离?
概念:当可见光束通过胶体时,在入射光侧面可观察到________ _______原因:胶体中分散质微粒对可见光产生_____应用:可用于鉴别______和_____
概念:在一定条件下胶体形成沉淀析出的现象
加入酸、碱和盐等加热或搅拌加含有相反电荷胶粒的胶体
应用:胶体净水原理、黄河三角洲的形成等
概念:在外加电场的作用下,带电胶体微粒发生定向移动原因:胶体微粒有巨大的比表面积,能较强地吸附带有某种电荷的 离子而形成带电微粒应用:电泳电镀、电泳除尘等
(1)根据丁达尔效应将分散系分为溶液、浊液和胶体( )(2)直径介于1~100 nm之间的粒子称为胶体( )(3)Fe(OH)3胶体聚沉生成沉淀,发生了化学变化( )
(1)溶液、浊液、胶体三种分散系的本质区别是什么?
提示 溶液、浊液、胶体三种分散系本质的区别是分散质粒子的大小不同。
(2)可用过滤的方法除去氢氧化铁胶体中的泥沙吗?
提示 可以,胶体中的分散质粒子能透过滤纸孔隙,而泥沙不能透过,故可以用过滤的方法除去氢氧化铁胶体中的泥沙。
(3)下列事实与胶体性质有关的是__________(填序号)。①水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染②一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路③往Fe(OH)3胶体中滴入稀硫酸,先看到红褐色沉淀生成,而后沉淀溶解④医院里用血液透析的方法治疗肾功能衰竭等疾病引起的血液中毒⑤FeCl3溶液和烧碱溶液混合会产生红褐色沉淀
1、溶液、胶体、浊液三类分散系的比较
2、图解胶体的制备与性质
随堂演练 知识落实
1.(2020·吉林高一检测)某气体经过检验只含有一种元素,则该气体是( )A.一种单质B.一种化合物C.单质与化合物的混合物D.可能是一种单质,也可能是几种单质的混合物
解析 只含有一种元素的物质可能是纯净物单质(如O2),也可能是混合物(如O2和O3的混合气体)。
2.在“加碘食盐”“含氟牙膏”“补钙保健品”“缺铁性贫血”中,“碘、氟、钙、铁”是指( )A.单质 B.元素 C.化合物 D.物质
解析 这些元素均以化合态形式存在,化合物不只是由一种元素组成。
3.国家质检部门检出人们端午节包粽子的“返青粽叶”多以胆矾(化学式为CuSO4·5H2O)为添加剂,长期食用有害健康,请问胆矾是一种( )A.氧化物 B.盐 C.碱 D.酸
解析 胆矾、绿矾(FeSO4·7H2O)等结晶水合物都属于盐、纯净物。
4.根据某种共性,可将CO2、SO2归为一类氧化物,下列物质中与它们属于同一类的是( )A.CaCO3 B.P2O5 C.CuO D.KMnO4
解析 CO2、SO2属于酸性氧化物,CaCO3、KMnO4属于盐,CuO属于碱性氧化物。
5.氯化铁溶液与氢氧化铁胶体具有的共同性质是( )A.分散质粒子直径在1~100 nm之间 B.都是混合物C.都是无色、透明的溶液 D.都呈红褐色
解析 氯化铁溶液与氢氧化铁胶体两种分散系,都属于混合物;氯化铁溶液为棕黄色,其分散质粒子直径小于1 nm;氢氧化铁胶体为红褐色,其分散质粒子直径在1~100 nm之间。
6.我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10-9 m)恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中正确的是( )A.其分子直径比氯离子小B.在水中形成的分散系属于悬浊液C.在水中形成的分散系具有丁达尔效应D.“钴酞菁”分子不能透过滤纸
解析 分散质“钴酞菁”分子的直径(1.3×10-9 m)介于1~100 nm之间(大于氯离子的直径),为胶体粒子,其分散系为胶体,能透过滤纸,具有丁达尔效应。
人教版 (2019)必修 第一册第一节 物质的分类及转化教学课件ppt: 这是一份人教版 (2019)必修 第一册第一节 物质的分类及转化教学课件ppt,共25页。PPT课件主要包含了分门别类,物质的分类及转化,第一节,物质的分类,研读课本,教辅资料或学科等等,交叉分类,树状分类,如物质的分类可分为,纯净物等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第一节 物质的分类及转化课堂教学课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第一节 物质的分类及转化课堂教学课件ppt,共22页。PPT课件主要包含了纯净物,混合物,化合物,金属单质,有机物,无机物,氧化物,悬浊液乳浊液,新概念,分散系等内容,欢迎下载使用。
化学必修 第一册第一章 物质及其变化第二节 离子反应教学课件ppt: 这是一份化学必修 第一册第一章 物质及其变化第二节 离子反应教学课件ppt,共26页。PPT课件主要包含了Na+,Cl﹣,归纳总结,随堂练习等内容,欢迎下载使用。













