



还剩26页未读,
继续阅读
初中化学课题 1 质量守恒定律教案配套课件ppt
展开
这是一份初中化学课题 1 质量守恒定律教案配套课件ppt,共34页。PPT课件主要包含了P2O5,在密闭容器中,知识链接等内容,欢迎下载使用。
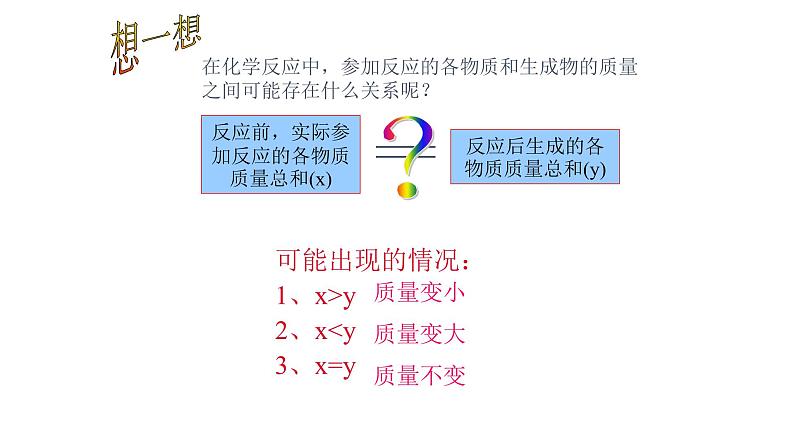
可能出现的情况:1、x>y2、x质量变小质量变大质量不变
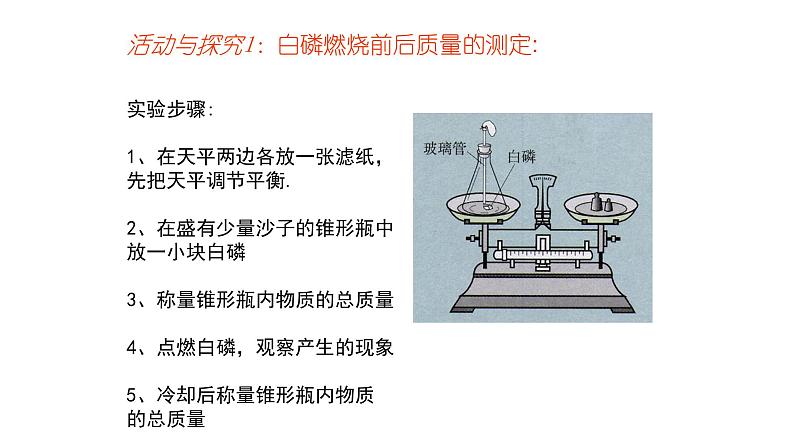
活动与探究1:白磷燃烧前后质量的测定:
实验步骤:1、在天平两边各放一张滤纸,先把天平调节平衡. 2、在盛有少量沙子的锥形瓶中放一小块白磷3、称量锥形瓶内物质的总质量4、点燃白磷,观察产生的现象5、冷却后称量锥形瓶内物质的总质量
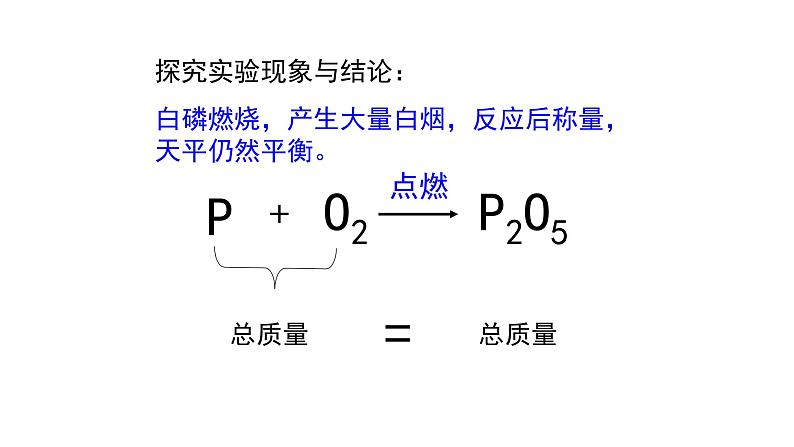
探究实验现象与结论:白磷燃烧,产生大量白烟,反应后称量,天平仍然平衡。
实验步骤:1、在天平两边各放一张滤纸,先把天平调节平衡2、反应前称量: 把装有硫酸铜溶液的小烧杯和铁钉一同放在天平左盘称量,称得总质量m1; 3、把铁钉加入到装有硫酸铜溶液的小烧杯中。(砝码不动) 4、反应后的称量:等到反应一段时间后,称得总质量m2,比较m1和m2的大小。
活动与探究2 铁钉与硫酸铜溶液反应前后质量的测定
硫酸铜 + 铁 → 硫酸亚铁 + 铜
M1 = M2
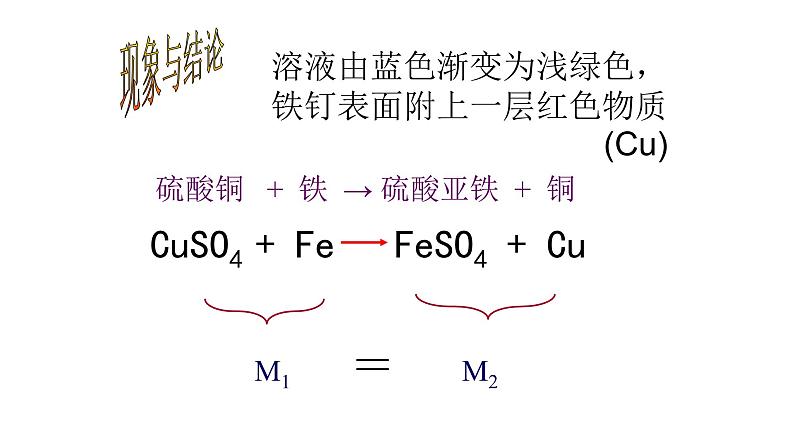
溶液由蓝色渐变为浅绿色,铁钉表面附上一层红色物质 (Cu)
CuSO4 + Fe FeSO4 + Cu
通过实验我们得到的结论是:
化学反应前后物质的总质量____
一 质量守恒定律。 参加化学反应的各物质的质量总和, 等于反应后生成的各物质的质量总和。
2. 6克碳与一定量的氧气恰好完全反应, 生成二氧化碳22克,有______克氧气 参加了反应。
是否存在违背质量守恒定律的化学反应呢?
固体粉末溶解,有大量的气泡产生;
天平指针向右倾斜(变轻)
思考:1、该实验的现象是什么?
发出耀眼的白光、放出大量的热,生成白色固体,同时还有白烟产生
思考:2、该反应的原理是什么?
在开放容器中:盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳
M1 > M2
盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳 M1 = M2
1、根据上面两个实验,讨论为什么会出现这样的实验结果。2、如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么实验结果?
之所以会出现这样的结果,是由于反应有气体参加或生成的缘故。
如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会发现天平保持平衡。
小结:若选择有气体参加或有气体生成的化学反应来证明质量守恒定律,则反应一定要在密闭容器内进行。
理解质量守恒定律的定义时要注意:
1.质量守恒定律是关于化学反应的普遍规律,其运用范围是化学变化。一切化学反应都遵循质量守恒定律。物理变化不属此范围。
2.质量守恒定律的“守恒”指的是质量守恒,不能任意扩展到其它物理量。如体积等不一定守恒。
3.注意定律中的几个关键之处:①“参加反应的各物质”,没有参加反应的物质不包括在内;②“生成的各物质的质量总和”,应当包括生成的各种物质,如沉淀、气体等。
在化学反应前后物质的质量总和为什么会守恒?
水 氢气 + 氧气
分析讨论:①化学反应前后,分子种类变了吗?②化学反应前后,原子种类变了吗?③化学反应过程的实质是什么?
H2O H2 + O2
宏观:反应前后元素种类不变。
成语“点石成金”,本意为古代术士的一种法术,即能使石头变成黄金;现比喻能化腐朽为神奇。有人说他能把石灰石变成黄金,请你用化学知识说明石灰石不能变成黄金的道理。
答:在化学反应中元素的种类不变。石灰石 的主要成分是碳酸钙,它是由钙元素、 碳元素、氧元素组成的。黄金是由金元 素组成的,因此石灰石不可能变成黄金。
链接:基训P42 14题、15题
某物质M燃烧后生成了水和二氧化碳,则它肯定含有哪些元素? A、C H B、 C C、C H O D、H O
链接:基训P44 2题、4题 基训P45 10题
在 A + B —— C + D 的反应中,5克A和4克B完全反应,生成 3克C,求生成的D的质量。
m D =5克 + 4克 –3 克 =6克
链接:基训P44 1、3、5、6、7题
在化学反应2XY2+Y2=2Z中Z的化学式为( ) A、X2Y3 B、XY3 C、X2Y6 D、 X2Y4
链接:导学案 P27 5题
用化学式表示化学反应的式子,叫化学方程式。(左反右生,等号连接)
(用化学式来表示反应的式子)
化学反应中各物质的质量比
反应物:S、O2。生成物:SO2。条件:点燃
表示反应物.生成物及反应条件
32 :16×2 :32+16×2
32 : 32 : 64
1 : 1 : 1
(2)化学方程式的读法
1)本质:硫和氧气在点燃条件下反应生成二氧化硫。
2)质量方面:每32份质量的硫和32份质量的氧气在点燃条件下完全反应生成64份质量的二氧化硫。
3)粒子个数方面:每1个硫原子和1个氧分子反应生成1个二氧化硫分子。
可能出现的情况:1、x>y2、x
活动与探究1:白磷燃烧前后质量的测定:
实验步骤:1、在天平两边各放一张滤纸,先把天平调节平衡. 2、在盛有少量沙子的锥形瓶中放一小块白磷3、称量锥形瓶内物质的总质量4、点燃白磷,观察产生的现象5、冷却后称量锥形瓶内物质的总质量
探究实验现象与结论:白磷燃烧,产生大量白烟,反应后称量,天平仍然平衡。
实验步骤:1、在天平两边各放一张滤纸,先把天平调节平衡2、反应前称量: 把装有硫酸铜溶液的小烧杯和铁钉一同放在天平左盘称量,称得总质量m1; 3、把铁钉加入到装有硫酸铜溶液的小烧杯中。(砝码不动) 4、反应后的称量:等到反应一段时间后,称得总质量m2,比较m1和m2的大小。
活动与探究2 铁钉与硫酸铜溶液反应前后质量的测定
硫酸铜 + 铁 → 硫酸亚铁 + 铜
M1 = M2
溶液由蓝色渐变为浅绿色,铁钉表面附上一层红色物质 (Cu)
CuSO4 + Fe FeSO4 + Cu
通过实验我们得到的结论是:
化学反应前后物质的总质量____
一 质量守恒定律。 参加化学反应的各物质的质量总和, 等于反应后生成的各物质的质量总和。
2. 6克碳与一定量的氧气恰好完全反应, 生成二氧化碳22克,有______克氧气 参加了反应。
是否存在违背质量守恒定律的化学反应呢?
固体粉末溶解,有大量的气泡产生;
天平指针向右倾斜(变轻)
思考:1、该实验的现象是什么?
发出耀眼的白光、放出大量的热,生成白色固体,同时还有白烟产生
思考:2、该反应的原理是什么?
在开放容器中:盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳
M1 > M2
盐酸 + 碳酸钠 → 氯化钠 + 水 +二氧化碳 M1 = M2
1、根据上面两个实验,讨论为什么会出现这样的实验结果。2、如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会出现什么实验结果?
之所以会出现这样的结果,是由于反应有气体参加或生成的缘故。
如果在燃着的镁条上方罩上罩,使生成物全部收集起来称量,会发现天平保持平衡。
小结:若选择有气体参加或有气体生成的化学反应来证明质量守恒定律,则反应一定要在密闭容器内进行。
理解质量守恒定律的定义时要注意:
1.质量守恒定律是关于化学反应的普遍规律,其运用范围是化学变化。一切化学反应都遵循质量守恒定律。物理变化不属此范围。
2.质量守恒定律的“守恒”指的是质量守恒,不能任意扩展到其它物理量。如体积等不一定守恒。
3.注意定律中的几个关键之处:①“参加反应的各物质”,没有参加反应的物质不包括在内;②“生成的各物质的质量总和”,应当包括生成的各种物质,如沉淀、气体等。
在化学反应前后物质的质量总和为什么会守恒?
水 氢气 + 氧气
分析讨论:①化学反应前后,分子种类变了吗?②化学反应前后,原子种类变了吗?③化学反应过程的实质是什么?
H2O H2 + O2
宏观:反应前后元素种类不变。
成语“点石成金”,本意为古代术士的一种法术,即能使石头变成黄金;现比喻能化腐朽为神奇。有人说他能把石灰石变成黄金,请你用化学知识说明石灰石不能变成黄金的道理。
答:在化学反应中元素的种类不变。石灰石 的主要成分是碳酸钙,它是由钙元素、 碳元素、氧元素组成的。黄金是由金元 素组成的,因此石灰石不可能变成黄金。
链接:基训P42 14题、15题
某物质M燃烧后生成了水和二氧化碳,则它肯定含有哪些元素? A、C H B、 C C、C H O D、H O
链接:基训P44 2题、4题 基训P45 10题
在 A + B —— C + D 的反应中,5克A和4克B完全反应,生成 3克C,求生成的D的质量。
m D =5克 + 4克 –3 克 =6克
链接:基训P44 1、3、5、6、7题
在化学反应2XY2+Y2=2Z中Z的化学式为( ) A、X2Y3 B、XY3 C、X2Y6 D、 X2Y4
链接:导学案 P27 5题
用化学式表示化学反应的式子,叫化学方程式。(左反右生,等号连接)
(用化学式来表示反应的式子)
化学反应中各物质的质量比
反应物:S、O2。生成物:SO2。条件:点燃
表示反应物.生成物及反应条件
32 :16×2 :32+16×2
32 : 32 : 64
1 : 1 : 1
(2)化学方程式的读法
1)本质:硫和氧气在点燃条件下反应生成二氧化硫。
2)质量方面:每32份质量的硫和32份质量的氧气在点燃条件下完全反应生成64份质量的二氧化硫。
3)粒子个数方面:每1个硫原子和1个氧分子反应生成1个二氧化硫分子。














