


人教版九年级上册课题 1 质量守恒定律优质ppt课件
展开【重点】了解什么叫化学方程式。
【难点】掌握化学方程式的意义。
1.了解化学方程式的含义及其表示的意义;2.会从质、量、数等方面读化学方程式,并能利用化学方程式求出化学反应中各物质的质量比。
请同学们写出碳在氧气中燃烧的反应文字表达式,这个文字表达式能给我们什么信息?
该式子确实能表示反应物、生成物及反应条件;但书写不方便、国际上不通用且不能体现质量守恒定律。
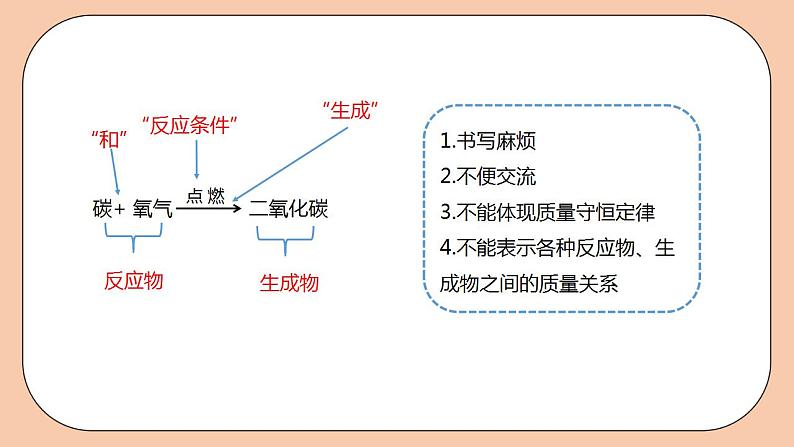
碳+ 氧气 二氧化碳
1.书写麻烦 2.不便交流 3.不能体现质量守恒定律 4.不能表示各种反应物、生成物之间的质量关系
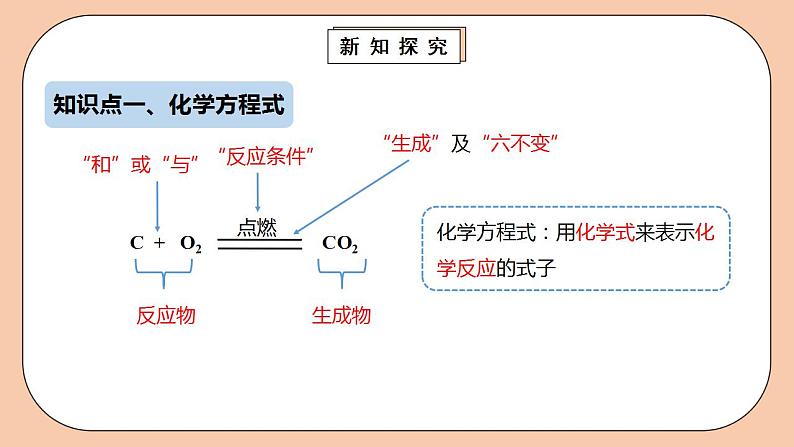
化学方程式:用化学式来表示化学反应的式子
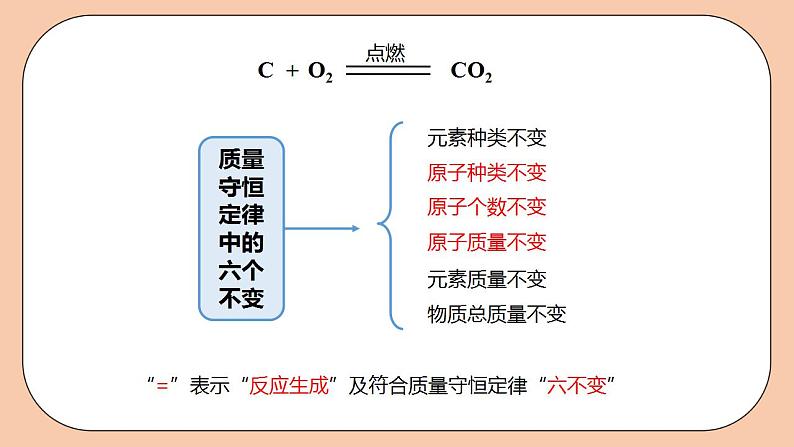
“=”表示“反应生成”及符合质量守恒定律“六不变”
质量守恒定律中的六个不变
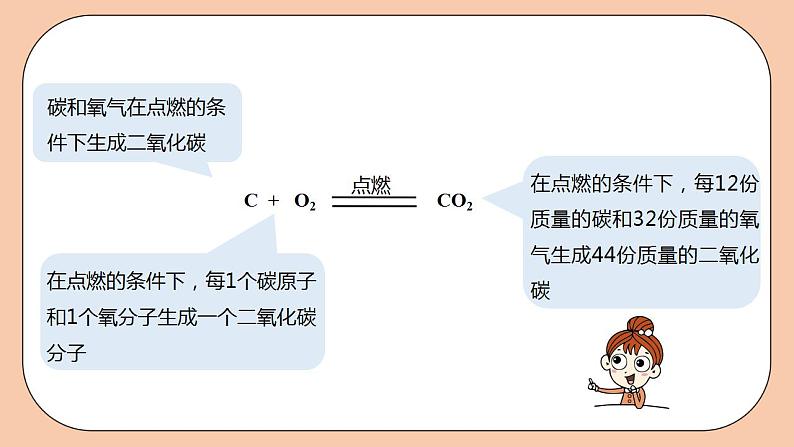
碳和氧气在点燃的条件下生成二氧化碳
在点燃的条件下,每1个碳原子和1个氧分子生成一个二氧化碳分子
在点燃的条件下,每12份质量的碳和32份质量的氧气生成44份质量的二氧化碳
氢气和氧气在点燃的条件下生成水
在点燃的条件下,每2个氢分子和1个氧分子生成2个水分子
在点燃的条件下,每4份质量的氢气和32份质量的氧气生成36份质量的水
表示反应物、生成物之间的粒子个数比
4P + 5O2 2P2O54×31 5×32 2×142
1、表示磷和氧气参加反应,反应生成五氧化二磷。
3、表示反应物中磷原子、氧分子和生成物中五氧化二磷分子的个数比为4∶5∶2。
4、表示每124份质量的磷与160份质量的氧气反应生成284份质量的五氧化二磷,质量比为31∶40∶71。
2、表示反应在点燃条件下进行。
1、化学计量数是指化学方程式中每种物质化学式前面的数字,如上述的反应中P的化学计量数为4,O2的化学计量数为5。
2、如果反应物(或生成物)都是气体,化学方程式还能表示它们在反应时的体积比,体积比等于化学计量数之比。如水通电分解生成氢气和氧气的体积比为2:1。
宏观读法: 碳和氧气在点燃条件下反应生成二氧化碳微观读法:在点燃条件下,每一个碳原子和一个氧气分子反应生成一个二氧化碳分子质量读法:在点燃条件下,每12份质量的碳和32份质量氧气反应生成44份质量的二氧化碳
1、宏观读法:氢气和氧气在点燃条件下反应生成水2、微观读法:在点燃条件下,每2个氢气分子和1个氧气分子反应生成2个水分子3、质量读法:在点燃条件下,每4份质量的氢气和32份质量的氧气反应生成36份质量的水
方法点拨:通过化学方程式,可得到的信息有:反应物、生成物、反应条件;反应中各物质的质量关系;反应中各粒子的数量关系。不能获知化学反应的快慢。
根据化学方程式,不能获得的信息是( )
A.反应中的反应物和生成物B.反应发生所需要的条件C.化学反应的快慢D.反应中各物质的质量关系
化学方程式:S+O2 SO2 所表示的意义是( )
①硫和氧气在点燃的条件下反应,生成二氧化硫②每1个硫原子和1个氧分子反应生成1个二氧化硫分子③每32份质量的硫和32份质量的氧气完全反应生成64份质量的二氧化硫④硫加氧气在点燃的条件下等于二氧化硫
A.①③④ B.①②③C.②③④ D.①②④
解析:①从质的方面描述了该化学方程式的意义;②从微观方面描述了该化学方程式的意义;③从量的方面描述了该化学方程式的意义。
用化学式来表示化学反应的式子
质的意义:表示反应物、生成物和反应条件
量的意义:1.表示反应物和生成物间的质量比2.表示参加反应和生成的各粒子的数量关系
宏观读法、微观读法、质量读法
先将8g A和10g B混合加热,恰好完全反应后生成6g C和一定质量的D,则下列说法错误的是( )A.参加反应的A和D的质量比是8∶6B.D的质量是12gC.4g A完全反应后生成3g CD.每8份质量的A和10份质量的B完全反应后生成6份质量的C
在一个密闭容器中放入X、Y、Z、W,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。则关于此反应的认识错误的是( )
A. 物质Z可能是该反应的催化剂B.待测值为15C.物质Y一定是单质D.反应中Y、W的质量比为6∶5
解析:由质量守恒定律可知,待测值为(20+5+2+37)-(35+2+12)=15,因为反应后X的质量减少,所以X是反应物;W的质量减少了37g-12g=25g,故W是反应物;Y的质量增加了35g-5g=30g,故Y是生成物。该变化可表示为X+W→Y,故Y一定是化合物;反应中Y、W的质量比为30g∶25g=6∶5;Z的反应前后质量不变,可能是该反应的催化剂,也可能是没有参加反应的物质。
在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t1、t2时各物质质量如图所示。下列说法中不正确的是( )
A.该反应为化合反应B.丙可能为该反应的催化剂C.该反应中,乙、丁的质量变化之比为7∶5 D.该反应中,甲、乙的质量变化之比为1∶4
解析:由反应前后的质量关系可知,该反应可表示为甲+丁→乙,属于化合反应;丙可能是该反应的催化剂,也可能是未参加反应的杂质;该反应中,乙和丁的质量变化之比为28 g∶20 g=7∶5;甲和乙的质量变化之比为8 g∶28 g=2∶7。
在化学反应 中,下列说法正确的是( )
A.碳加氧气等于二氧化碳B.反应前后分子的种类和数目不变C.反应前后元素的数目不变D.反应前后原子的种类和数目不变
解析:化学方程式中“+”是“和”的含义,“ ”是“生成”的含义;在该反应中,分子的种类和数目都发生了改变;元素只讲种类,不讲个数,在化学反应中元素的种类不变。
在2CO+O2 2CO2的反应中,CO、O2、CO2的质量比为 ( )
A.2∶1∶2 B.7∶4∶11C.7∶8∶11 D.14∶4∶11
九年级上册课题 1 质量守恒定律优质ppt课件: 这是一份九年级上册课题 1 质量守恒定律优质ppt课件,共30页。PPT课件主要包含了广而告之,两位科学家的“争论”,密闭装置,敞口装置,实验注意事项,质量守恒定律,天平不平衡,氧化镁,化学反应的实质,质量守恒的原因等内容,欢迎下载使用。
人教版九年级上册课题 1 质量守恒定律示范课ppt课件: 这是一份人教版九年级上册课题 1 质量守恒定律示范课ppt课件PPT课件主要包含了第1课时,狄仁杰的迷惑,提出问题,猜想假设,设计实验,称量结果,m前=1570g,m后=1570g,防止集气瓶底部炸裂,m前=1975g等内容,欢迎下载使用。
初中第四章 生命之源——水4.3 质量守恒定律集体备课课件ppt: 这是一份初中第四章 生命之源——水4.3 质量守恒定律集体备课课件ppt,共27页。PPT课件主要包含了质量守恒定律,课本114页习题4,想一想,水分子,化学反应前后,可能改变,在密闭容器中等内容,欢迎下载使用。













