





所属成套资源:2026届高考化学一轮总复习
2026届高考化学一轮总复习第8章水溶液中的离子反应与平衡第39讲盐类的水解课件
展开 这是一份2026届高考化学一轮总复习第8章水溶液中的离子反应与平衡第39讲盐类的水解课件,共60页。PPT课件主要包含了第39讲盐类的水解,考点二,考点一,盐类的水解,pH=7,pH7,答案C,答案10,盐的性质,颜色变浅等内容,欢迎下载使用。
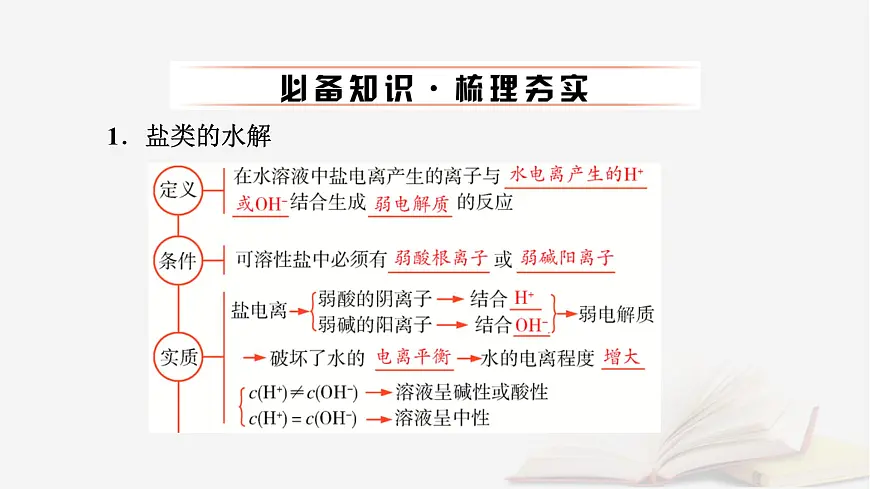
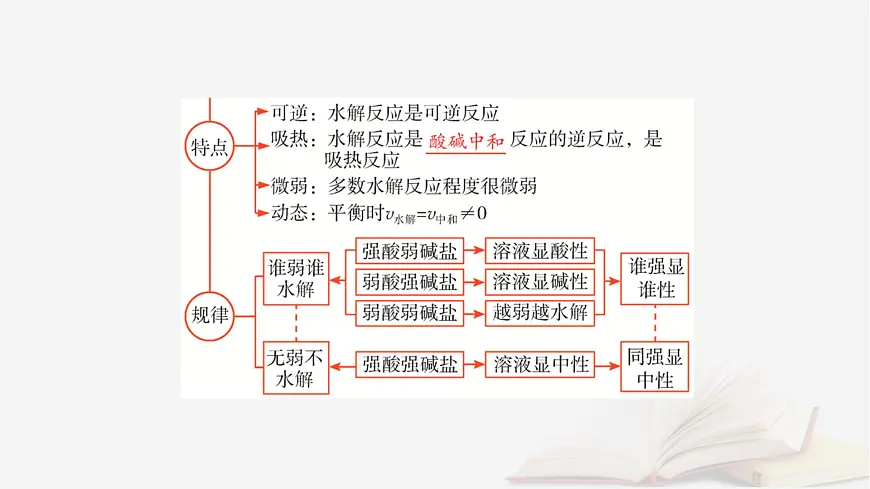
考点一 盐类的水解原理及规律
NH3·H2O+H+
(2)三种类型的盐水解离子方程式的书写①多元弱酸盐水解:分步进行,以第一步为主,一般只写第一步水解方程式。如Na2CO3水解的离子方程式为:第一步水解__________________________________;第二步水解__________________________________。
(3)实例探究分析盐类水解规律
【正误辨析】(1)常温下,pH=11的CH3COONa溶液与pH=3的CH3COOH溶液,水的电离程度相同。( )[提示] × CH3COONa促进水的电离,CH3COOH抑制水的电离。(2)相同温度时,浓度均为0.2 ml·L-1的NaHCO3和Na2CO3溶液中,存在的粒子种类相同。( )[提示] √ NaHCO3和Na2CO3溶液中,存在的粒子种类相同。
(3)某盐的溶液呈酸性,该盐一定发生了水解反应。( )
(4)已知酸性:HF>CH3COOH,所以等浓度的CH3COONa溶液的碱性强于NaF溶液。( )[提示] √ 根据越弱越水解可知,CH3COO-的水解程度大于F-的水解程度,所以CH3COONa溶液的碱性更强。(5)向AlCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成。( )[提示] √ 两种物质相互促进水解,水解彻底,有沉淀和气体生成。
(9)水解平衡右移,盐离子的水解程度可能增大,也可能减小。( )[提示] √ 若是加入能水解的该盐固体,平衡右移,盐离子的水解程度会减小,若是加水稀释,平衡右移,水解程度是增大的。
(10)稀溶液中,盐的浓度越小,水解程度越大,其溶液酸性(或碱性)也越强。( )[提示] × 溶液越稀,水解程度越大,水解产生的H+或OH-的物质的量越大,但稀释后H+或OH-的浓度越小,所以溶液酸性(或碱性)会越弱。
1.(2025·北京海淀检测)已知HClO、CH3COOH在常温下的电离常数分别为4.0×10-8、1.8×10-5。常温下,物质的量浓度均为0.1 ml·L-1的六种溶液:①(NH4)2SO4溶液;②KNO3溶液;③NH4HSO4溶液;④NH4Cl溶液;⑤NaClO溶液;⑥CH3COONa溶液,则上述六种溶液的pH由小到大的顺序是( )A.③①④②⑤⑥ B.③①④②⑥⑤C.③②①⑥④⑤ D.⑤⑥②④①③[答案] B
微考点1 盐类水解的实质及规律
2.(2025·武汉模拟)如图是某离子M的水解过程示意图,M可能是( )
3.室温下,0.1 ml·L-1的NH4CN溶液的pH等于9.32,下列说法错误的是( )A.上述溶液能使甲基橙试剂变黄色B.室温下,NH3·H2O是比HCN更弱的电解质C.上述溶液中CN-的水解程度大于NH的水解程度D.室温下,0.1 ml·L-1 NaCN溶液中,CN-的水解程度小于上述溶液中CN-的水解程度[答案] B
弱酸弱碱盐阴、阳离子都水解,其溶液的酸碱性取决于弱酸阴离子和弱碱阳离子水解程度的相对强弱。当K酸=K碱(K为电离常数)时,溶液显中性,如CH3COONH4;当K酸>K碱时,溶液显酸性,如HCOONH4;当K酸c(CH3COO-)>c(OH-)[答案] B
[解析] ①盐酸pHc(CH3COO-)>c(OH-),故D正确。
6.(2025·湖南长沙检测)物质与水发生的复分解反应称为水解反应。例如:Mg3N2+6H2O===3Mg(OH)2↓+2NH3↑。在一定条件下,BrCl、CuCl2、Mg2C3和K3P均可以发生水解。根据上述观点,下列说法不正确的是( )A.BrCl的水解产物是HBrO和HClB.K3P的水解产物是KOH和H3PO4C.Mg2C3的水解产物是Mg(OH)2和C3H4D.CuCl2的水解产物是Cu(OH)2和HCl[答案] B
溶液酸碱性强弱比较 盐溶液的酸碱性
比较相同浓度的溶液pH大小的方法(1)先按酸性、中性、碱性分类,再按电离和水解规律排序。(2)酸性:强酸强碱弱酸盐。
书写盐类水解离子方程式的注意事项
微考点3 利用电离常数计算水解常数
[答案] (1)1×10-12 增大 (2)2.4×10-5
考点二 盐类水解的影响因素及应用
生成红褐色沉 淀,放出气体
【正误辨析】(1)水解平衡右移,盐的离子的水解程度一定增大。( )[提示] × 水解平衡右移,盐的离子的水解程度也可能是在减小,如增大盐的浓度。(2)在CH3COONa溶液中加入冰醋酸,能抑制CH3COO-水解。( )[提示] √ 醋酸分子浓度增加,抑制CH3COO-的水解。(3)将Fe2(SO4)3溶液加热蒸干并灼烧,最后得到Fe2O3。( )[提示] × 将Fe2(SO4)3溶液加热蒸干并灼烧,最后得到Fe2(SO4)3。
(6)碳酸钠溶液可以用于除去油污。( )[提示] √ 碳酸钠溶液水解显碱性,油污在碱性条件下水解,生成可溶于水的物质,起到去污效果。(7)NH4F溶液存放在玻璃试剂瓶中。( )[提示] × NH4F溶液中F-水解生成HF会与玻璃中的SiO2反应。(8)可溶性铁盐可以用于净水。( )[提示] √ 可溶性铁盐如Fe2(SO4)3水解可以生成Fe(OH)3胶体,胶体具有吸附作用,可用于净水。
(13)明矾作为净水剂,可以杀菌、消毒。( )[提示] × 明矾溶于水后,Al3+的水解产物Al(OH)3胶体具有吸附作用,可以净水,但不能杀菌消毒。(14)配制FeSO4溶液时,应加入铁粉防止Fe2+被氧化,并加入盐酸抑制Fe2+水解。( )[提示] × 应加入硫酸抑制Fe2+水解。
1.利用传感技术测定一定浓度碳酸钠溶液的pH与温度(T)的关系,曲线如图,下列分析错误的是( )
微考点1 外界条件对盐类水解的影响
A.碳酸钠水解是吸热反应B.ab段说明水解平衡正向移动C.bc段说明水解平衡逆向移动D.水的电离平衡也对pH产生影响
[解析] 分析图像,碳酸钠溶液中碳酸根离子水解,升温pH增大,说明水解是吸热反应,故A正确;碳酸钠是弱酸强碱盐,水解使溶液显碱性,而升高温度使平衡正向移动,溶液的碱性增强,故B正确;水解是吸热的,温度不断升高只会导致平衡不断正向移动,此时溶液pH却出现反常下降,这是由于水本身也存在电离,温度改变对水的电离平衡造成了影响,故C错误;水本身也存在着一个电离平衡,温度改变平衡移动,因此对溶液的pH产生影响,故D正确。
[名师点拨] 理解盐类水解影响因素的常见误区误区一:误认为水解平衡向正向移动,离子的水解程度一定增大。如向FeCl3溶液中,加入少量FeCl3固体,平衡向水解方向移动,但Fe3+的水解程度减小。误区二:误认为弱酸强碱盐都因水解而显碱性。如NaHSO3溶液显酸性。误区三:误认为可水解的盐溶液在蒸干后都得不到原溶质。例如:对于水解程度不大且水解产物不离开平衡体系的情况[如Al2(SO4)3]来说,溶液蒸干仍得原溶质。
3.实验测得0.5 ml·L-1 CH3COONa溶液、0.5 ml·L-1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是( )
A.随温度升高,纯水中c(H+)>c(OH-)B.随温度升高,CH3COONa溶液的c(OH-)减小C.随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果D.随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO-、Cu2+水解平衡移动方向不同
[答案] C[解析] 升高温度,促进水的电离,但纯水中的c(H+)=c(OH-),A错误;升高温度既促进水的电离,又促进醋酸钠的水解,使溶液中c(OH-)增大,B错误;升高温度既促进水的电离,Kw增大,又促进铜离子的水解,使其水解平衡正向移动,这相当于促进了氢氧根离子与铜离子结合,故c(H+)增大,导致pH减小,C正确;盐类的水解是吸热反应,随着温度升高,CH3COO-、Cu2+的水解平衡均正向移动,水解平衡移动方向相同,D错误。
4.(2024·河北保定高三检测)下列有关问题与盐的水解有关的是( )①NH4Cl与ZnCl2溶液可作焊接金属时的除锈剂 ②NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂③草木灰与铵态氮肥不能混合施用 ④实验室中盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞 ⑤加热蒸干CuCl2溶液得到Cu(OH)2固体 ⑥要除去FeCl3溶液中混有的Fe2+,可先通入氧化剂Cl2,再调节溶液的pHA.①②③ B.②③④C.①④⑤ D.①②③④⑤[答案] D
微考点2 盐类水解在生产和生活中的应用
5.下列物质的应用中,利用了水解平衡的是( )A.用NaHCO3固体制备纯碱B.用明矾[KAl(SO4)2·12H2O]处理污水C.用盐酸去除铁锈(主要成分Fe2O3·xH2O)D.用双氧水杀灭细菌[答案] B[解析] NaHCO3固体加热分解得到纯碱(碳酸钠),A不符合题意;明矾[KAl(SO4)2·12H2O]电离出的Al3+水解生成Al(OH)3胶体,有吸附性,B符合题意;氧化铁能与盐酸反应生成可溶性氯化铁和水,C不符合题意;双氧水有较强的氧化性,用于杀灭细菌,D不符合题意。
6.请回答下列问题。(1)把AlCl3溶液蒸干灼烧,最后得到的主要固体是________,原因是________________________________________________________________________________________________________________________________________________________________________________________(用化学方程式表示并配以必要的文字说明),如何操作溶质不变?__________________________________________________________________________________________________________________________。
(2)Mg粉可溶解在NH4Cl溶液中,原因是_______________________ _______________________________________________________________________________________________________________________________________________________________________________________。
1.(2024·安徽卷,13,3分)环境保护工程师研究利用Na2S、FeS和H2S处理水样中的Cd2+。已知25 ℃时,H2S饱和溶液浓度约为0.1 ml·L-1,Ka1(H2S)=10-6.97,Ka2(H2S)=10-12.90,Ksp(FeS)=10-17.20,Ksp(CdS)=10-26.10。下列说法错误的是( )A.Na2S溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+2c(S2-)B.0.01 ml·L-1 Na2S溶液中:c(Na+)>c(S2-)>c(OH-)>c(HS-)C.向c(Cd2+)=0.01 ml·L-1的溶液中加入FeS,可使c(Cd2+)c(Cd2+)
2.(2023·北京卷,3,3分)下列过程与水解反应无关的是( )A.热的纯碱溶液去除油脂B.重油在高温、高压和催化剂作用下转化为小分子烃C.蛋白质在酶的作用下转化为氨基酸D.向沸水中滴入饱和FeCl3溶液制备Fe(OH)3胶体[答案] B[解析] 用热的纯碱溶液去油污,是因为纯碱在热水中水解程度增大,溶液碱性增强,可促进油脂水解;重油在高温、高压和催化剂作用下生成小分子烃,属于分解反应;蛋白质在酶的作用下发生水解反应转化为氨基酸;向沸水中滴入饱和FeCl3溶液,Fe3+发生水解反应生成Fe(OH)3胶体;综上所述可知选B。
3.(2023·重庆卷,11,3分)(NH4)2SO4溶解度随温度变化的曲线如图所示,关于各点对应的溶液,下列说法正确的是( )
4.(2023·海南卷,14,1分)25 ℃下,Na2CO3水溶液的pH随其浓度的变化关系如图所示。下列说法正确的是( )
A.c(Na2CO3)=0.6 ml·L-1时,溶液中c(OH-)
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 

.png)




