





所属成套资源:高一化学课件(苏教版2019)
专题5 微观结构与物质的多样性第二单元 第1课时 离子键高一化学课件(苏教版2019)
展开 这是一份专题5 微观结构与物质的多样性第二单元 第1课时 离子键高一化学课件(苏教版2019),共60页。
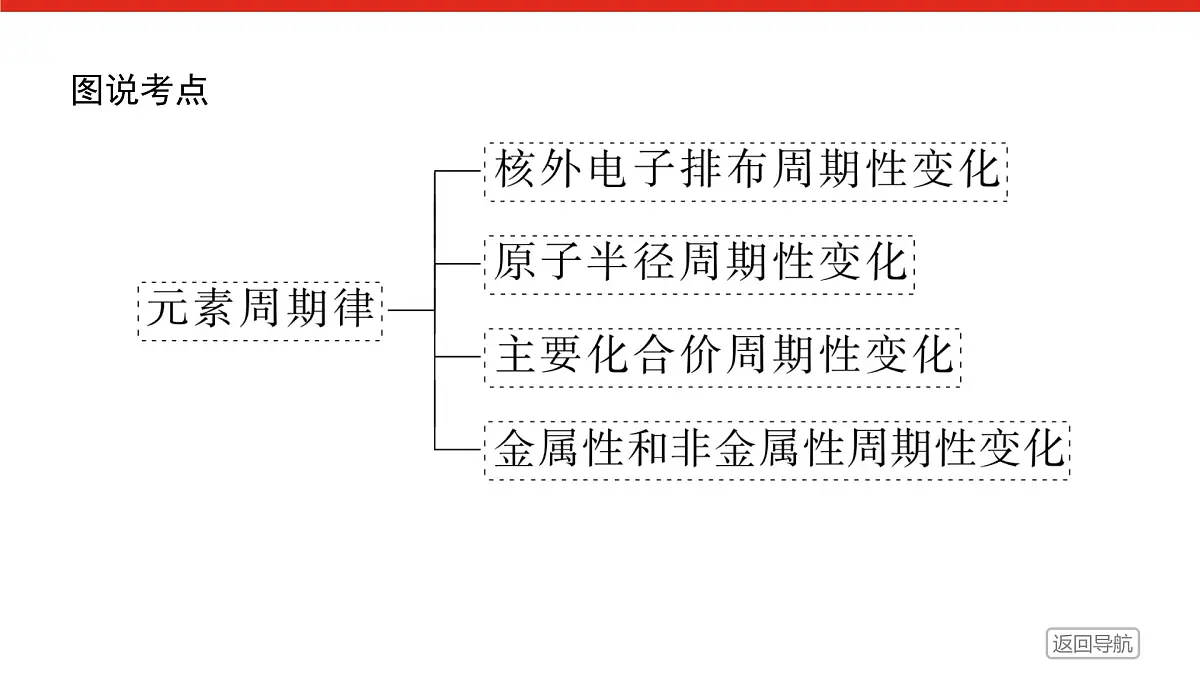
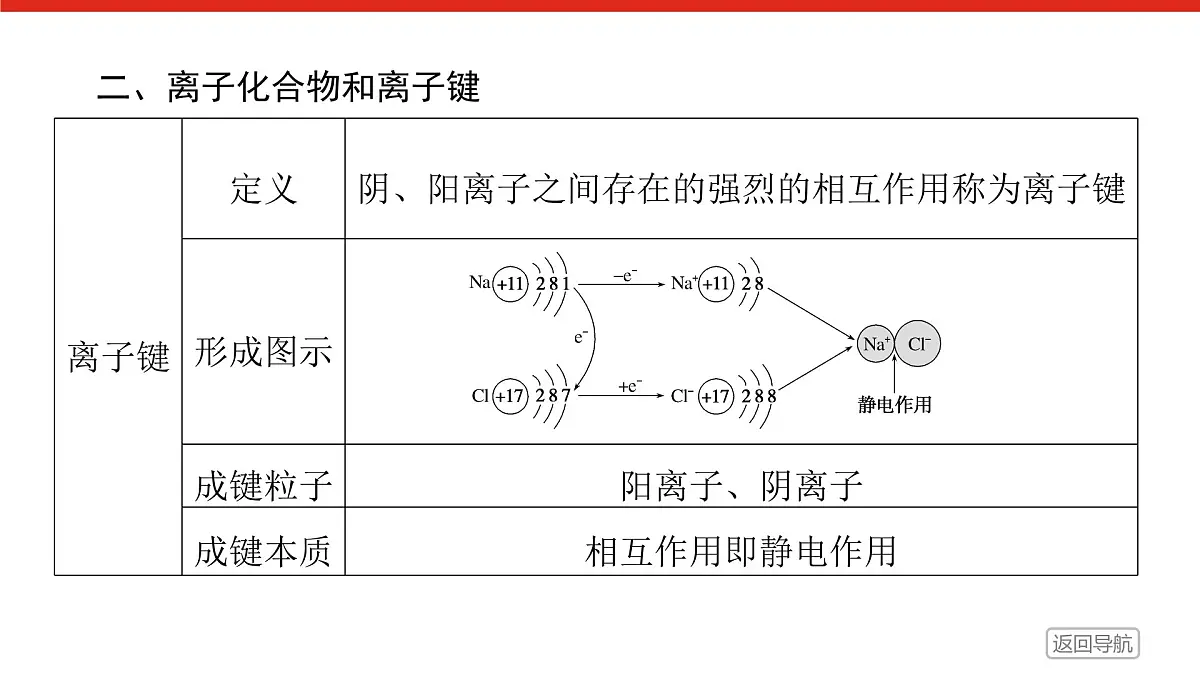
第1课时 离子键课程目标1. 认识化学键的含义。2.知道离子键的概念及其形成。3.能用电子式表示离子化合物的组成和形成过程。图说考点01.学业基础——自学·思记·尝试02.核心素养——合作·探究·分享03.学考评价——夯实·测控·演练04.课时作业(二十五)内容索引01.学业基础——自学·思记·尝试学业基础——自学·思记·尝试[新知预习]一、化学键1.化学键:物质中直接相邻的________________________相互作用。2.分类:__________________。3.构成物质的基本微粒原子或离子之间存在的强烈的离子键、共价键特别提醒 并不是所有的物质中都存在化学键,如稀有气体中不存在化学键。二、离子化合物和离子键续表阴、阳三、电子式最外层电子Na×Na+[即时自测] 1.判断正误,正确的打“√”,错误的打“×”(1)化学键只存在于分子之间。( )(2)化学键只存在于离子之间。( )(3)化学键是相邻原子或离子之间的强烈的静电吸引力。( )(4)MgCl2的电子式为: ( )(5)离子化合物是由阴、阳离子通过离子键构成的化合物。( )××××√2.下列物质中含有离子键的是( )A.H2 B.CO2C.NH3 D.NaCl答案:D3.下列电子式中书写正确的是( )答案:C02.核心素养——合作·探究·分享核心素养——合作·探究·分享提升点1离子键与离子化合物例1 下列说法正确的是( )A.阴、阳离子通过静电吸引形成的强烈相互作用称为离子键B.第ⅠA族元素原子和第ⅦA族元素原子之间都形成离子键C.金属元素与非金属元素化合时,不一定形成离子键D.只有活泼金属元素与活泼非金属元素之间才能形成离子键答案:C解析:离子键是阴、阳离子通过静电作用形成的,静电作用包括引力和斥力,A项错误;第ⅦA族元素都是活泼的非金属元素,第ⅠA族元素大都是活泼的金属元素,但氢是非金属元素,HF、HCl、HBr、HI等化合物中的化学键都不是离子键,B项错误;某些不活泼金属与非金属元素之间形成共价键,如AlCl3,C项正确;形成离子键的也可以是带电荷的原子团,如(NH4)2SO4等,D项错误。[提升1] 小亮的纠错笔记中有两道题未分析,请帮他分析。(1)下列说法正确的是( )A.阴、阳离子通过静电引力形成离子键B.阴、阳离子间通过离子键一定能形成离子化合物C.离子化合物一定能导电D.离子化合物中只含离子键,不含共价键答案:B 解析:A项,离子键是指阴、阳离子间的静电作用,包括引力和斥力;B项,离子键形成的只能是离子化合物;C项,离子化合物在熔融状态或水溶液里才能导电;离子化合物也可能含有共价键,如NaOH,D错误。(2)下列属于离子化合物的是( )A.CaCl2 B.HClC.Na D.H2O关键能力答案:A解析:Na是金属单质;HCl、H2O分子中均无易失电子的原子,不是离子化合物;Ca是活泼金属,Cl是活泼非金属,两种原子分别失、得电子形成Ca2+、Cl-,故CaCl2是离子化合物。1.离子键的三个“一定”和两个“不一定”(1)三个“一定”①离子化合物中一定含有离子键。②含有离子键的化合物一定是离子化合物。③离子化合物中一定含有阴离子和阳离子。(2)两个“不一定”①离子化合物中不一定含有金属元素,如NH4Cl、NH4NO3等。②含有金属元素的化合物不一定是离子化合物,如AlCl3。 提升点2 用电子式表示离子化合物例2 下列电子式书写正确的是________。答案:EFH解析:氯原子最外层电子数为7,A错;最外层电子数应在原子的元素符号上、下、左、右四个方向对称分布,应为[提升2] 判断下列用电子式表示的离子化合物的形成过程是否正确?若错误,请说明理由。错误。①将“―→”写成了“===”;②阴离子(Cl-)的电子式未加[ ]表示。正确的写法是错误。生成的离子化合物不能将两个氟离子写在一起。正确的写法是正确。解析:此题考查了电子式的书写。用电子式表示离子化合物的形成过程时,离子化合物中阴、阳离子的表示要正确。状元随笔 电子式书写中的“6个”易错点:①将离子化合物与共价化合物电子式混淆;②将书写电子式与用电子式表示物质形成过程混淆;③将阳离子电子式与阴离子电子式混淆;④漏写原子最外层未成对电子;⑤合并同类离子;⑥漏掉离子所带电荷数等。关键能力电子式的书写方法1.原子的电子式书写原子的电子式时,一般将原子的最外层电子写在元素符号的上、下、左、右四个位置上。例如:2.简单阳离子的电子式简单阳离子是原子失去最外层电子后形成的,其电子式就是简单阳离子的离子符号,如Na+、Mg2+等。3.简单阴离子的电子式4.复杂阴离子、阳离子的电子式复杂阴离子、阳离子要标明电子,要用“[ ]”括起来,并在“[ ]”右上角标明“+”“-”及其电荷数。5.离子化合物电子式的书写(原则上把阳离子和阴离子的电子式按比例组合)6.用电子式表示离子化合物的形成过程例如氯化镁的形成:在左边写出镁原子、氯原子的电子式,右边写出离子化合物氯化镁的电子式,中间用“―→”,而不用“===”连接,如:03.学考评价——夯实·测控·演练学考评价——夯实·测控·演练1.以下是四位同学关于化学键概念理解的对话,其中错误的是( )答案:C2.全球热播影片《阿凡达》在中国内地上映,影片中出现了一种潘多拉星球的宇宙飞船。如表是元素周期表中的一部分,表中所列字母分别表示一种元素(选项中的物质都由下表中的元素组成)。由以上信息可推断下列说法正确的是( ) 答案:C 3.下列物质中不含离子键的是( )①NH4HCO3 ②NH3 ③BaSO4④CH3COONa ⑤Ba(OH)2 ⑥H2SO4A.①④⑥ B.②③⑤C.④⑤ D.②⑥答案:D解析:①NH4HCO3中铵根离子和碳酸氢根离子之间以离子键相结合;②NH3中N和H之间以共价键相结合,不含离子键;③BaSO4中钡离子和硫酸根离子之间以离子键相结合;④CH3COONa中醋酸根离子和钠离子之间以离子键相结合;⑤Ba(OH)2中钡离子和氢氧根离子之间以离子键相结合;⑥H2SO4中S和H、O之间以共价键相结合,不含离子键。因此不含有离子键的是②⑥。4.下列说法正确的是( )A.含有金属元素的化合物一定是离子化合物B.第ⅠA族和第ⅦA族原子化合形成的化合物一定是离子化合物C. 在离子化合物CaCl2中,两个氯离子间也存在离子键D.钠原子与氯气反应生成食盐后,其结构的稳定性增强答案:D解析:AlCl3晶体中不含有离子键,故AlCl3不是离子化合物,A错误;第ⅠA族中氢原子和第ⅦA族的原子化合形成的化合物不是离子化合物,B错;离子键是使阴、阳离子结合成化合物的静电作用,C错;钠原子失去最外层1个电子,而氯原子得到1个电子后都变成最外层8电子的稳定结构,D正确。5.下列离子化合物电子式不正确的是( )答案:C解析:离子化合物的电子式由阴离子电子式和阳离子电子式构成,原子失去电子成为阳离子,阳离子的电子式和离子符号相同,原子失去几个电子就带几个单位正电荷。阳离子没有方括号(阳离子的原子团除外)。阴离子是原子获得电子,使外层电子达到8个电子的稳定结构(K层为2个电子),用方括号把电子都围在内部,例如氯原子获得一个电子,成为带一个负电荷的离子 ,在硫化钠中有两个Na+和一个硫离子,但是两个阳离子不能写在一起,阳离子要挨着阴离子,阴离子要挨着阳离子,整个电子式呈电中性。因而A、B、D电子式都对。Na2O2是离子化合物,阴离子没有用方括号括住,没有标出负电荷的电荷数,C错,其正确的书写为:6.(1)写出下列物质的电子式。①Ca________,Si________,S________,F________;②NaH____________,溴化钾_________,MgO_____________;③氢氧化钠__________,过氧化钙____________。(2)用电子式表示下列离子化合物的形成过程。①氧化钠:_________________________________________________;②氯化镁:________________________________________________。Na+[∶H]-7.A、B、C 3种短周期元素,原子序数依次增大,3种元素原子序数之和为35,A、C同主族,B+核外有10个电子,则:(1)A、B、C 3种元素分别是_____、______、______。(填元素名称)(2)A、B、C 3种元素两两之间能形成多种化合物,其中属于离子化合物的化学式分别为________、________、________。(3)用电子式表示B和C形成离子化合物的过程________________________________。氧钠硫Na2ONa2O2Na2S解析:由B+核外有10个电子可推知B为钠元素,设A的原子序数为x,由A、C同主族知C的原子序数为x+8,即x+11+x+8=35,则x=8,故A为氧元素,C为硫元素。练后感悟电子式书写的三大错因04.课时作业(二十五)一、选择题(每小题只有一个选项符合题意,每小题3分,共33分)1.下图形象地表示了氯化钠的形成过程。下列相关叙述中不正确的是( )A.钠原子易失去一个电子,氯原子易得到一个电子B.钠离子与钠原子有相似的化学性质C.钠原子与氯原子作用生成NaCl后,其结构的稳定性增强D.氯化钠是离子化合物答案:B 答案:B3.下列各组原子序数所表示的两种元素能形成AB2型离子化合物的是( )A.6和8 B.11和13C.11和16 D.12和17答案:D解析:A项,可以是CO2,B项,Na和Al不能形成化合物,C项,可以是Na2S,D项,为MgCl2,符合题意的只有D项。A项CO2是共价化合物。4.关于化学键的下列说法中,正确的是( )A.物质中任何原子间的相互作用都属于化学键B.任何分子中都含有化学键C.物质溶于水时一定发生了化学键的断裂D.化学变化必定包含旧化学键断裂和新化学键生成两个过程答案:D5.以下叙述中,错误的是( )A.钠原子和氯原子作用生成NaCl后,其结构的稳定性增强B.在氯化钠中,除氯离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用C.任何离子键在形成的过程中必定有电子的得与失D.金属钠与氯气反应生成氯化钠后,体系能量降低答案:C解析:活泼的金属原子和活泼的非金属原子之间形成离子化合物,阳离子和阴离子均达到稳定结构,这样体系的能量降低,其结构的稳定性增强,故A、D正确,B也正确。离子键的形成只是阴、阳离子间的静电作用并不一定发生电子的得失,如Na+与OH-结合成NaOH,故C错误。6.下列哪一组元素的原子间反应不易形成离子键( ) A. a与f B.a与gC.b与g D.d与g答案:D7.下列电子式书写正确的是( )A.①③⑤ B.②④⑥C.①③④ D.③⑥答案:D解析:①中Cl-电子式书写错误,应写为8.下列物质的形成过程表示正确的是( )答案:D解析:在原子与离子化合物间应用“―→”号连接,不能用“===”,且NaCl电子式应写为 ,A项错误;Na+、Br-没有标出其所带电荷,B项错误;两个氟离子不能放在一起,应放在Mg2+两侧,C项错误。9. 某离子化合物中阳离子和阴离子的电子层结构均与氖原子电子层结构相同则此离子化合物的化学式为( )A.MgCl2 B.NaF C.MgS D.K2S答案:B10.下列叙述正确的是( ) A.阳离子一定是金属离子阴离子一定只含非金属元素 B.某金属元素的阳离子和某非金属元素的阴离子组成的物质一定是纯净物 C.阴、阳离子相互作用后不一定形成离子化合物 D.离子化合物一定都溶于水 答案:C 11.下列指定微粒的个数比为2∶1的是 ( )A.NaHSO4固体中的阳离子和阴离子B.Na2O2中阳离子和阴离子C.H-离子中质子数和电子数D.BaH2固体中阳离子和阴离子答案:B 二、非选择题(共27分)12.(5分)氮化钠(Na3N)是科学家制备的一种重要的化合物它与水作用可产生NH3请回答下列问题:(1)比较Na3N中两种微粒的半径r(Na+) _______(填“>”“r(O)>r(H)解析:已知A、C最外层电子数相等,则A、C同主族;C是金属元素,则A可能是氢或硼;设原子序数aA、bB、cC、dD,则c+d=3(a+b),若a=1,则c=11;若a=5,则c=13;而a
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 


.png)




