



人教版 (新课标)选修4 化学反应原理第一节 原电池一等奖ppt课件
展开第四章 电化学基础
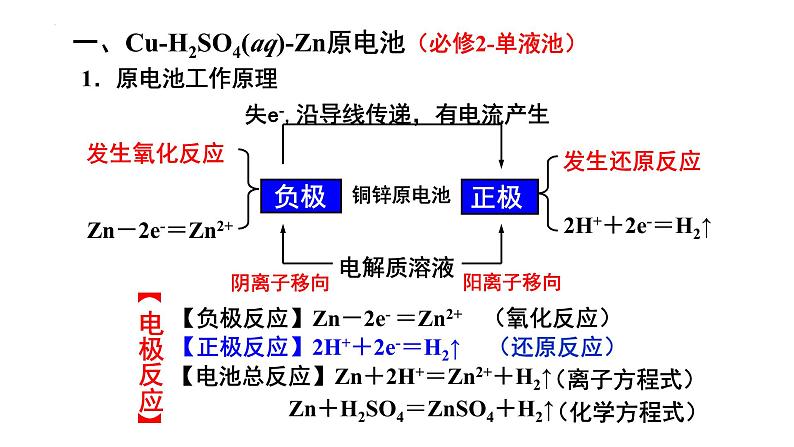
Zn-2e-=Zn2+
失e-,沿导线传递,有电流产生
2H++2e-=H2↑
【正极反应】2H++2e-=H2↑
【负极反应】Zn-2e- =Zn2+
【电池总反应】Zn+2H+=Zn2++H2↑
Zn+H2SO4=ZnSO4+H2↑
一、Cu-H2SO4(aq)-Zn原电池(必修2-单液池)
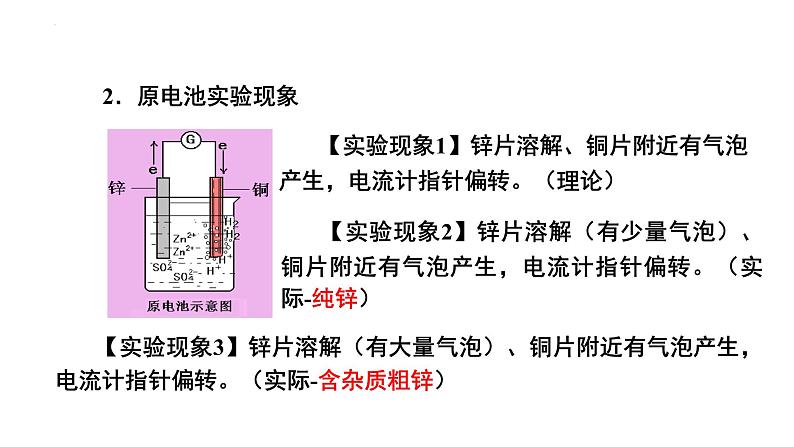
【实验现象1】锌片溶解、铜片附近有气泡产生,电流计指针偏转。(理论)
【实验现象2】锌片溶解(有少量气泡)、铜片附近有气泡产生,电流计指针偏转。(实际-纯锌)
【实验现象3】锌片溶解(有大量气泡)、铜片附近有气泡产生,电流计指针偏转。(实际-含杂质粗锌)
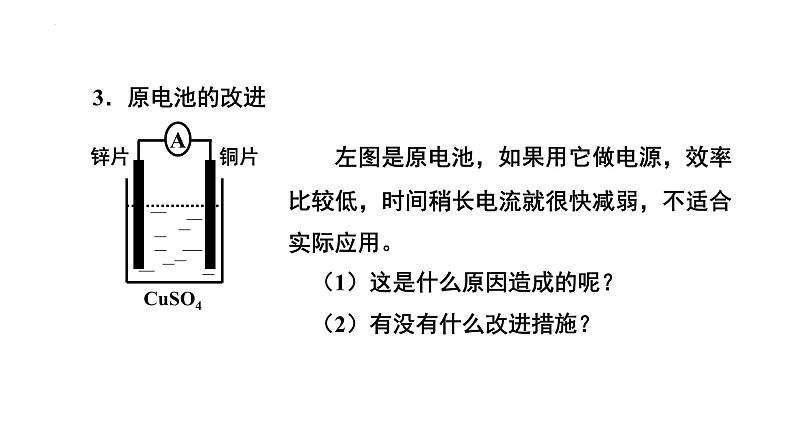
左图是原电池,如果用它做电源,效率比较低,时间稍长电流就很快减弱,不适合实际应用。 (1)这是什么原因造成的呢? (2)有没有什么改进措施?
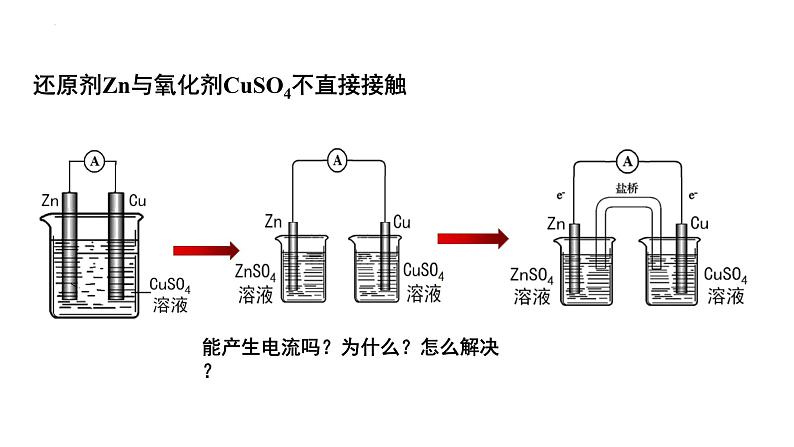
还原剂Zn与氧化剂CuSO4不直接接触
能产生电流吗?为什么?怎么解决?
(1)盐桥的成分:饱和的KCl溶液和琼脂(2)盐桥的作用: ①可使由它连接的两溶液保持电中性。 ②保障整个电路闭合,维持反应进行。 ③转移离子,沟通内电路。
【实验4-1】装置如图4-1所示,用一个充满电解质溶液的盐桥,装置有锌片的ZnSO4溶液和铜片用导线连接,并在中间串联一个电流表,观察有什么现象发生。取出盐桥,又发生了什么现象?
相同点:氧化还原反应原理;两个电极;都能产生电流;外电路均 是电子的定向移动, 内电路均是离子的定向移动。不同点:1.两个半反应在同一区域进行,电流不稳定。 2.两个半反应在不同区域进行,电流持续、稳定。
二、(盐桥)双液原电池的工作原理
(1)把氧化反应和还原反应分开在不同区域进行
(2)原电池的正负极的判断
(3)电解质溶液和电极材料的选择
烧杯中的电解质溶液应与电极材料具有相同的阳离子
较不活泼金属(非金属)
(3) 外电路中的电子从______________电极流向______________电极。
判断右边原电池的正、负极,并写出电极反应式。
负极: Cu-2e-=Cu2+正极: 2Fe3+ +2e-=2Fe2+
Cu+2FeCl3=CuCl2+2FeCl2
Cu+2Fe3+=Cu2++2Fe2+
根据化合价升降判断正负极
1.简单原电池电极方程式的写法
负极:2Al-6e- =2Al3+
2Al3++8OH-=2AlO2-+4H2O
负极总反应: 2Al+8OH- -6e- =2AlO2-+4H2O
正极:总反应-负极反应
6H2O+6e-=6OH—+ 3H2↑
2Al+2OH- +2H2O=2AlO2-+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2.复杂原电池电极方程式的书写
1、根据氧化还原反应电子转移判断电极反应2、根据电极反应确定合适的电极材料和电解质溶液
利用Fe+Cu2+=Fe2++Cu,设计一个原电池
【科学探究】原电池的设计
利用反应Zn+2FeCl3=2FeCl2+ZnCl2 设计出原电池,并写出电极反应
负极:Zn-2e-=Zn2+(氧化反应)正极:2Fe3++2e-=2Fe2+(还原反应)
1.利用原电池原理设计新型化学电池
2.改变化学反应速率,如实验室用粗锌与硫酸反应制取氢气
3.进行金属活动性强弱比较
4.保护金属不受腐蚀,即将金属作为原电池的正极而受到保护
2.把a、b、c、d四块金属浸泡在稀硫酸中,用导线两两相连可以组成各种原电池.若a、b相连时,a为负极;c、d相连时,c为负极;a、c相连时,c为正极;b、d相连时,b为正极.则这四种金属的活动性顺序由大到小为( ) A.a>b>c>d B.a>c>d>b C.c>a>b>d D.b>d>c>a
3.(2021·安徽·高二月考)NO2是大气的主要污染物之一,某研究小组设计如图所示的装置对NO2进行回收利用,装置中a、b均为多孔石墨电极。下列说法错误的是( ) A.a为电池的负极,发生氧化反应 B.电子流向a电极→用电器→b电极→溶液→a电极 C.一段时间后,a极附近HNO3浓度增大 D.电池总反应为4NO2+O2+2H2O=4HNO3
人教版 (新课标)选修4 化学反应原理第四节 化学反应进行的方向优秀ppt课件: 这是一份人教版 (新课标)选修4 化学反应原理<a href="/hx/tb_c22167_t3/?tag_id=26" target="_blank">第四节 化学反应进行的方向优秀ppt课件</a>,共20页。PPT课件主要包含了组织建设,ΔG=ΔH-TΔS,课堂小结等内容,欢迎下载使用。
高中化学人教版 (新课标)选修4 化学反应原理第一节 化学反应速率获奖课件ppt: 这是一份高中化学人教版 (新课标)选修4 化学反应原理<a href="/hx/tb_c22164_t3/?tag_id=26" target="_blank">第一节 化学反应速率获奖课件ppt</a>,共25页。PPT课件主要包含了●炸药爆炸,●金属锈蚀,●食物腐败,●离子反应,●塑料老化,●溶洞形成,组织建设,第一节化学反应速率,计算式为单位,化学反应速率等内容,欢迎下载使用。
高中化学人教版 (新课标)选修4 化学反应原理第三节 化学反应热的计算优质课件ppt: 这是一份高中化学人教版 (新课标)选修4 化学反应原理<a href="/hx/tb_c22161_t3/?tag_id=26" target="_blank">第三节 化学反应热的计算优质课件ppt</a>,共25页。PPT课件主要包含了组织建设,盖斯定律,△H2>0,△H1<0,S始态,L终态,△H1+△H2≡0,②×2-①得,盖斯定律的应用,反应热的计算等内容,欢迎下载使用。













