



人教版 (新课标)选修4 化学反应原理第一节 弱电解质的电离精品ppt课件
展开三、电解质的电离方程式
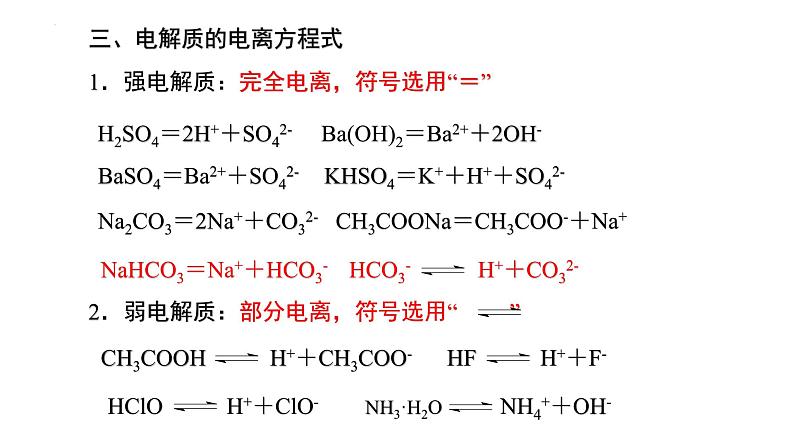
1.强电解质:完全电离,符号选用“=”
H2SO4=2H++SO42- Ba(OH)2=Ba2++2OH-
BaSO4=Ba2++SO42- KHSO4=K++H++SO42-
Na2CO3=2Na++CO32- CH3COONa=CH3COO-+Na+
【小试牛刀】写出下列各物质的电离方程式:Ca(OH)2、CaCO3、NaHSO3、NaHSO4、HI、H2S、Fe(OH)2、Na2SiO3、H2O2、H2C2O4、H2SO3、H2O
【再来一刀】醋酸的下列性质中,可以证明它是弱电解质的是( ) ①1 ml·L-1的CH3COOH溶液中c(H+)=10-2 ml·L-1;②CH3COOH以任意比与H2O互溶;③在相同条件下,CH3COOH溶液的导电性比盐酸弱;④10mL1ml·L-1的CH3COOH溶液恰好与10mL1ml·L-1的NaOH溶液完全反应;⑤同浓度同体积的CH3COOH溶液和HCl溶液与Fe反应时,CH3COOH溶液中放出H2的速率慢;⑥CH3COOH溶液中CH3COOH、CH3COO-、H+同时存在 A.①③⑤⑥ B.②③④⑤ C.①④⑤⑥ D.③⑤⑥
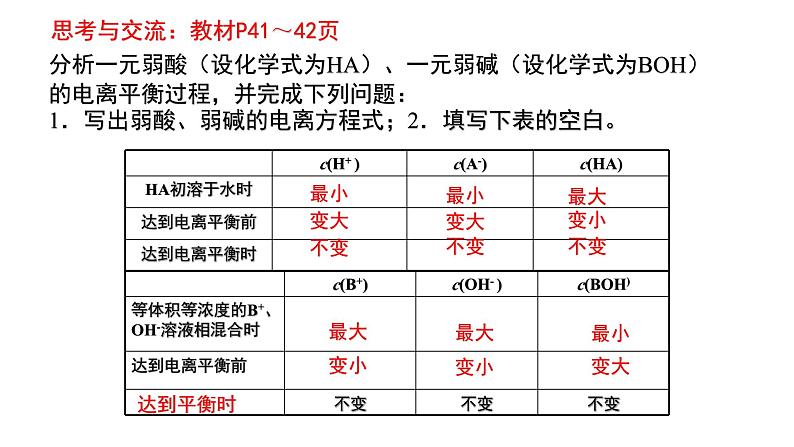
分析一元弱酸(设化学式为HA)、一元弱碱(设化学式为BOH)的电离平衡过程,并完成下列问题:1.写出弱酸、弱碱的电离方程式;2.填写下表的空白。
思考与交流:教材P41~42页
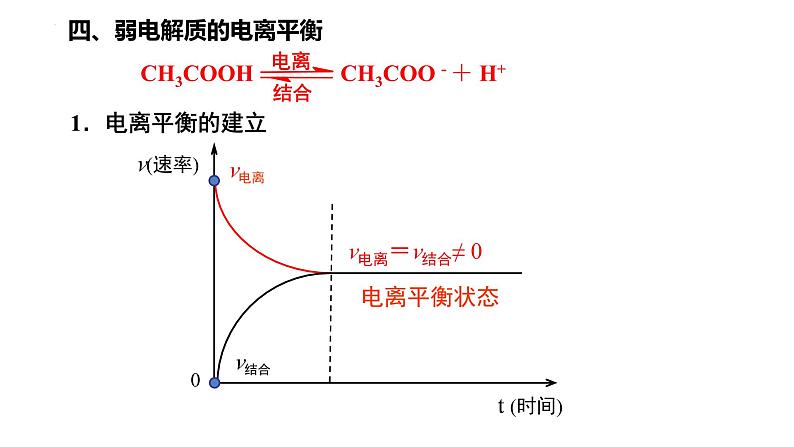
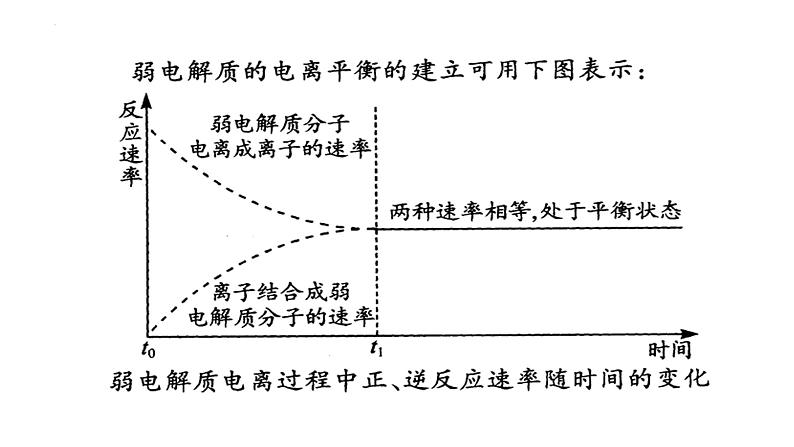
四、弱电解质的电离平衡
v电离=v结合≠ 0
2.电离平衡:在一定条件(如温度、浓度)下,当弱电解质分子电离成离子的速率和离子结合成弱电解质分子的速率相等时,电离过程就达到了电离平衡状态。
(1)研究对象:弱电解质的电离
(2)特征(点):动、定、等、变、吸
吸:电离过程为吸热过程(△H>O)。
3.影响电离平衡的因素
(1)内因:电解质的本性。通常电解质越弱,电离程度越小。
(2)外因(外界条件):浓度、温度等。
① 温度:升高温度,电离平衡向电离方向(正方向)移动,弱电解质的电离程度将增大。
②浓度:增大电解质分子的浓度或减少相应离子的浓度,都会使电离平衡向电离方向移动。加水稀释弱电解质溶液,电离平衡正向移动,电离程度增大(越稀越电离)。
③同离子效应:在弱电解质溶液中加入同弱电解质具有相同离子的强电解质时,电离平衡向逆反应方向移动。
④化学反应:在弱电解质溶液中加入能与弱电解质电离产生的某种离子反应的物质时,可使平衡向电离的方向移动。
【再来一刀】相同温度下0.1ml/L的醋酸溶液与0.01ml/L的醋酸,两者的电离度和氢离子浓度下列叙述正确的是( ) A.电离度前者大,氢离子浓度后者小 B.电离度前者小,氢离子浓度后者小 C.电离度前者小,氢离子浓度后者大 D.电离度前者大,氢离子浓度后者大
【思考】在CH3COOH水溶液中存在哪些微粒?离子浓度的关系? H2S水溶液中存在哪些微粒?离子浓度的关系?
【再来一刀】比较H2S溶液中的微粒浓度大小(H2O除外)
【小试牛刀】已知氢氟酸(HF)是弱酸,在物质的量浓度为0.1ml/L的HF溶液中, 下列排序正确的是( ) A.c(F-)>c(H+)>c(HF)>c(OH-) B.c(HF)>c(H+)>c(F-)>c(OH-) C.c(H+)>c(F-)>c(HF)>c(OH-) D.c(HF)>c(F-)>c(H+)>c(OH-)
【再来一刀】下列对氨水溶液中存在的电离平衡:NH3·H2O NH4++OH- 叙述正确的是( )A.加水后,溶液中n(OH-)增大 B.加入少量浓盐酸,溶液中c(OH-)增大C.加入少量浓NaOH溶液,电离平衡正向移动D.加入少量NH4Cl固体,溶液中c(NH4 +)减少
在醋酸溶液中存在的平衡有
分析改变下列条件对醋酸电离平衡的影响,填写下表:
1.在100 mL 0.1ml·L-1的醋酸溶液中,欲使醋酸的电离程度增大,H+浓度减小,可采用的方法是( )A.加热 B.加入100 mL 0.1 ml·L-1的醋酸溶液C.加入少量的0.5 ml·L-1的硫酸 D.加入少量的1 ml· L-1的NaOH溶液
2.从植物花中可提取一种简写为HIn的有机物,在水溶液中因存在以下电离平衡,故可用作酸碱指示剂。HIn(aq) (红色) H+ (aq) +In-(aq)(黄色)在浓度为0.02 ml·L-1的下列各溶液中加入该指示剂,(1)HCl (2)NaOH (3)NaCl(aq) (4)NaHSO4(aq) (5) Na2CO3(aq) (6)氨水 其中能使指示剂显黄色的是( )A.(1)(4)(5) B.(2)(6) C.(1)(4) D.(2)(5)(6)
3.常温下,有pH相同、体积相同的醋酸和盐酸两种溶液,分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( ) A. B. C. D.
人教版 (新课标)选修4 化学反应原理第四节 化学反应进行的方向优秀ppt课件: 这是一份人教版 (新课标)选修4 化学反应原理<a href="/hx/tb_c22167_t3/?tag_id=26" target="_blank">第四节 化学反应进行的方向优秀ppt课件</a>,共20页。PPT课件主要包含了组织建设,ΔG=ΔH-TΔS,课堂小结等内容,欢迎下载使用。
高中化学人教版 (新课标)选修4 化学反应原理第一节 化学反应速率获奖课件ppt: 这是一份高中化学人教版 (新课标)选修4 化学反应原理<a href="/hx/tb_c22164_t3/?tag_id=26" target="_blank">第一节 化学反应速率获奖课件ppt</a>,共25页。PPT课件主要包含了●炸药爆炸,●金属锈蚀,●食物腐败,●离子反应,●塑料老化,●溶洞形成,组织建设,第一节化学反应速率,计算式为单位,化学反应速率等内容,欢迎下载使用。
2020-2021学年第二节 水的电离和溶液的酸碱性备课课件ppt: 这是一份2020-2021学年第二节 水的电离和溶液的酸碱性备课课件ppt,共33页。PPT课件主要包含了探究一,探究二等内容,欢迎下载使用。













