高中化学人教版 (新课标)选修4 化学反应原理第一节 弱电解质的电离同步测试题
展开1.关于强弱电解质及非电解质的组合完全正确的是( )
2.在0.1ml·L-1CH3COOH溶液中存在如下电离平衡:对于该平衡,下列叙述正确的是( )
A.加入水时,平衡向逆方向移动
B.加入少量NaOH固体,平衡向正方向移动
C.加入少量0.1ml·L-1HCl溶液,溶液中c(H+)不变
D.加入少量CH3COONa固体,平衡向正方向移动
·L-1的某一元弱酸溶液,在100℃和20℃时相比,其c(H+)前者比后者( )
A.大B.小
C.相等D.不能肯定
4.下列物质容易导电的是( )
A.熔融的氯化钠B.硝酸钾溶液
C.硫酸铜晶体D.无水乙醇
5.根据酸碱质子理论,凡是能给出质子(即H+)的分子或离子都是酸,凡是能结合质子的分子或离子都是碱。按照这种理论,下列粒子属于两性物质的是( )
A.OH-B.H2OC.H2POeq \\al(-,4)D.NaCl
6.根据下表数据(均在同温、同压下测定),可得出弱电解质强弱顺序正确的是( )
A.HX>HY>HZB.HZ>HY>HX
C.HY>HZ>HXD.HZ>HX>HY
7.在相同温度时100mL0.01ml·L-1的醋酸溶液与10mL0.1ml·L-1的醋酸溶液相比较,下列数值前者大于后者的是( )
A.中和时所需NaOH的量
B.电离程度
C.H+的物质的量
D.CH3COOH的物质的量
8.证明碳酸钙是强电解质的实验事实是( )
A.碳酸钙属于盐类
B.碳酸钙与盐酸反应是离子反应
C.碳酸钙溶于水的部分是完全电离的
D.碳酸钙在一定条件下能电离出Ca2+和COeq \\al(2-,3)
9.现有浓度均为0.1ml·L-1的盐酸、硫酸、醋酸三种溶液,回答下列问题:
(1)等体积的以上三种酸分别与过量的NaOH溶液反应,若生成的盐的物质的量依次为b1ml、b2ml、b3ml,则它们的大小关系为____________________。
(2)分别用以上三种酸中和一定量的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、V3,其大小关系为______________________________。
(3)分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为____________________。
能力提升
10.将大小、形状相同,质量相等的镁条,放入下列溶液中,反应速率按由大到小的顺序排列正确的是( )
①2ml·L-1H3PO4 ②2ml·L-1醋酸 ③2ml·L-1的醋酸中加入少量的CH3COONa固体 ④2ml·L-1的盐酸
A.①③②④B.④①②③
C.④②①③D.①④③②
11.化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂。
向HIn的水溶液中分别滴入浓度为0.02ml·L-1的下列各溶液:
①盐酸 ②石灰水 ③NaCl溶液 ④NaHSO4溶液 ⑤NaHCO3溶液 ⑥氯水
其中能使该水溶液变红色的是( )
A.①④⑤B.②⑤⑥C.①④D.②③⑥
12.在25℃时,用蒸馏水稀释1ml·L-1的醋酸溶液至0.01ml·L-1,随溶液的稀释,下列各项中始终保持增大趋势的是( )
AB.
C. D.
·L-1H2S水溶液加水稀释为0.01ml·L-1时,下列各粒子的浓度减小最多的是( )
A.H2SB.HS-C.H+D.S2-
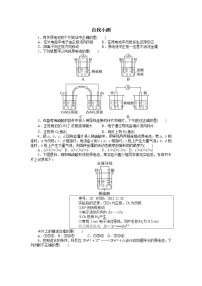
14.如图所示图像是在一定温度下,向不同电解质溶液中加入新物质时的溶液的导电性(其电流强度I随加入量m)的变化曲线。其中与A变化趋势一致的是__________,与B变化趋势一致的是__________,与C变化趋势一致的是__________。(填序号)
①Ba(OH)2溶液中滴入H2SO4溶液至过量 ②醋酸溶液中滴入NH3·H2O溶液至过量 ③澄清石灰水中通入CO2至过量 ④NH4Cl溶液中逐渐加入适量NaOH固体 ⑤盐酸中通入适量氨气 ⑥氢氧化钠溶液中通入适量Cl2
拓展探究
15.双氧水(H2O2)和水都是极弱电解质,但H2O2显极弱的酸性。
(1)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:____________________。
(2)鉴于H2O2显弱酸性,它能同强碱作用形成“正盐”,在一定条件下也可形成“酸式盐”。请写出H2O2与Ba(OH)2作用形成的“正盐”的化学方程式:____________________。
(3)水电离生成H3O+和OH-叫做水的自偶电离。同水一样,H2O2也有极微弱的自偶电离,其自偶电离的方程式为______________________________。
参考答案
1解析:在A组中Cl2是单质,不在电解质与非电解质之列;B组中BaSO4虽难溶,但溶解的部分完全电离,是强电解质,非弱电解质;CaCO3、HNO3都是强电解质,HClO、CH3COOH都是弱电解质,C2H5OH、SO2都是非电解质,C、D两组正确。
答案:CD
2解析:A项,加水,有利于弱电解质的电离,虽离子浓度减小,但离子数目增加;B项,加碱与弱酸电离的H+反应使电离平衡正向移动,但H+浓度减小;C项,加强酸提供H+,抑制弱酸电离,但H+浓度增大,溶液酸性增强;D项,加相同阴离子的强电解质,同名离子抑制弱酸电离,平衡逆向移动。
答案:B
3解析:升高温度促进弱电解质的电离。
答案:A
4解析:电解质在水溶液中或熔融状态下才能离解为自由移动的离子,在此状况下才能导电,而非电解质在上述两种条件下均不能电离。导电粒子一种是自由电子,另一种是自由的阴、阳离子。A、B具有自由的阴、阳离子;C中虽有阴、阳离子,但不能自由移动;无水乙醇为非电解质。
答案:AB
5解析:OH-能结合H+:OH-+H+===H2O,生成弱电解质H2O,则OH-是碱,H2O能电离出H+,就是能给出质子,H2O是酸;H2O又能结合H+,就是能结合质子,即H2O+H+===H3O+,H2O又是碱,所以H2O属于两性物质。H2POeq \\al(-,4)能电离出H+:,,它又能结合质子:,所以H2POeq \\al(-,4)属于两性物质。NaCl===Na++Cl-,Na+和Cl-不能结合H+和OH-,NaCl既不是酸,又不是碱。应选B、C。
答案:BC
6解析:电离平衡常数的大小可表明弱电解质的相对强弱,电离平衡常数越大,弱电解质的电离程度越大。
答案:A
7解析:两溶液中CH3COOH的物质的量都是0.001ml,中和时所需NaOH的量相等;浓度越大,电离程度越小,其电离出的H+的物质的量浓度也就越小。
答案:BC
8解析:判断强弱电解质的标准是在溶于水时能否完全电离。
答案:C
9答案:(1)b1=b2=b3 (2)V1=V3=2V2 (3)v2>v1>v3
10解析:反应速率的快慢取决于溶液中c(H+)的大小。②、③相比较,由于③中加入了CH3COONa固体,从而抑制了醋酸的电离,故③中c(H+)要比②中c(H+)略小。
答案:B
11解析:由电离平衡看出,若使指示剂显红色必须使平衡左移,而使平衡左移的条件是向溶液中加入H+。在给出的试剂中只有①和④溶于水后能电离出大量的H+。氯水有漂白性,会使溶液褪色。
答案:C
12解析:醋酸是弱酸,加水稀释,醋酸的电离平衡右移,n(H+)和n(CH3COO-)增大,n(CH3COOH)与c(H+)和c(CH3COO-)减小;A、B、C项中,分子分母同乘溶液体积,浓度比等于其物质的量之比。A中随加水比值增大;B中,随加水比值几乎不变;C中,随加水比值减小;D中比值是平衡常数K表达式,K是不随浓度而改变的常数,故加水,其比值不变。
答案:A
13解析:弱电解质溶液在加水稀释过程中,存在两个效应:一是稀释效应,二是电离效应。对离子而言是在浓度减小(稀释导致)的基础上略有增大(电离平衡右移导致),而对弱电解质分子而言两种效应的作用都使其浓度变小。
答案:A
14解析:电流强度I与离子浓度成正比。
答案:② ①③ ④⑤⑥
15解析:(1)若把H2O2看成二元弱酸,则其存在二级电离,其电离方程式为:
(2)因可把H2O2看做二元弱酸,故当它和碱反应生成“正盐”时,应生成过氧化物。所以H2O2和Ba(OH)2反应生成“正盐”的化学方程式为:H2O2+Ba(OH)2===BaO2+H2O。
(3)类比水的自偶电离,不难书写出H2O2的自偶电离方程式。
答案:(1)
(2)H2O2+Ba(OH)2===BaO2+2H2O
(3)
A
B
C
D
强电解质
NaCl
H2SO4
CaCO3
HNO3
弱电解质
HF
BaSO4
HClO
CH3COOH
非电解质
Cl2
CS2
C2H5OH
SO2
酸
HX
HY
HZ
物质的量浓度/ml·L-1
0.1
0.2
0.3
电离平衡常数
7.2×10-4
1.8×10-4
1.8×10-5
高中化学人教版 (新课标)选修4 化学反应原理第一节 化学反应与能量变化课后练习题: 这是一份高中化学人教版 (新课标)选修4 化学反应原理第一节 化学反应与能量变化课后练习题,共7页。试卷主要包含了6 ℃时变成硫蒸气S2,2C ΔH=-221,6 kJ 的热量, 是吸热反应,则CO是,已知,有如下三个热化学方程式等内容,欢迎下载使用。
高中化学人教版 (新课标)选修4 化学反应原理第二章 化学反应速率和化学平衡第一节 化学反应速率课时训练: 这是一份高中化学人教版 (新课标)选修4 化学反应原理第二章 化学反应速率和化学平衡第一节 化学反应速率课时训练,共4页。
化学选修4 化学反应原理第二章 化学反应速率和化学平衡第一节 化学反应速率当堂达标检测题: 这是一份化学选修4 化学反应原理第二章 化学反应速率和化学平衡第一节 化学反应速率当堂达标检测题,共7页。试卷主要包含了反应,经2minB的浓度减少0,8ml·L-1·s-1,将5,把0,已知反应等内容,欢迎下载使用。