



人教版 (新课标)选修4 化学反应原理第一节 弱电解质的电离教课内容ppt课件
展开变 —— 条件改变,平衡移动
定 —— 溶液中离子浓度和分子浓度保持不变
逆 —— 离子化与分子化的过程可逆
等 —— v(电离)___v(结合)___0
2、电离平衡的定义: 一定条件下,弱电解质分子电离成离子的速率和离子重新 结合成弱电解质分子的速率相等时的状态叫电离平衡
(1)向溶液中加入与弱电解质电离有相同离子的强电解质, 使电离平衡向逆方向移动。
(二)影响电离平衡的因素
2、浓度:(1)增大弱电解质溶液浓度,电离平衡向电离方向移动, 溶液中电解质分子和电离生成的离子浓度都增大。
1、温度:升高溶液温度,电离平衡向电离方向移动。
内因:弱电解质本身的性质
(因电离过程是破坏化学键的吸热过程。)
(2) 通常,减小弱电解质溶液浓度,即加水稀释弱电解质 溶液时,电离平衡向电离方向移动,
电解质分子和电离生成的离子浓度都减小。
(勒夏特列原理也适用于电离平衡)
(2)加入与弱电解质电离出的离子反应的离子,电离平衡 正向移动。
:弱电解质在溶液里达到电离平衡时,溶液中已经电离的电解质分子数占原来分子总数的百分数。
了解:电离程度的定量表示方法
注意:在相同条件下,电离度越大,电解质越强。
讨论:常温时,1ml/L的CH3COOH溶液和0.1ml/L的CH3COOH溶液,其c(H+) 之比为( ) A . 1:1 B. 10:1 C. <10:1 D. >10:1
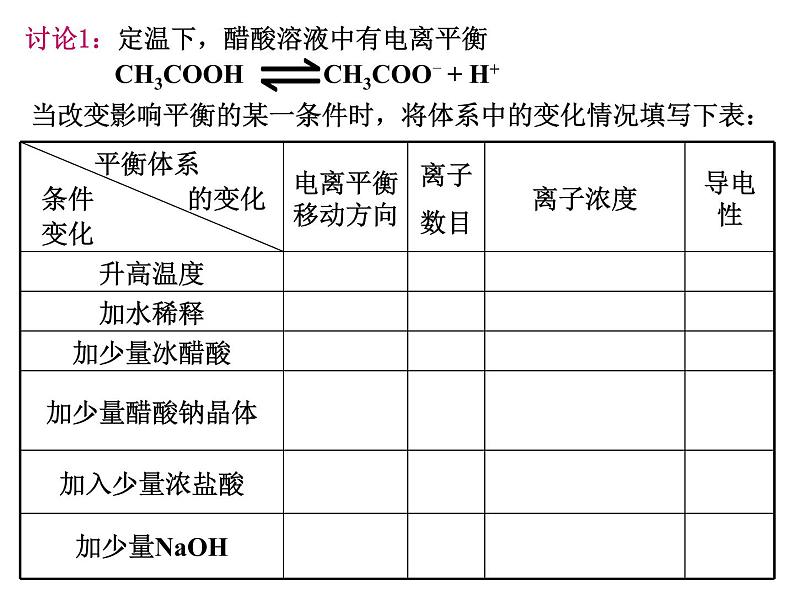
当改变影响平衡的某一条件时,将体系中的变化情况填写下表:
讨论1:定温下,醋酸溶液中有电离平衡
CH3COOH CH3COO- + H+
讨论2:为何多元弱酸电离以一级电离为主,逐级渐难?
1、某一元强酸X和某一元弱酸Y的水溶液中,c(H+)均为1×10-2ml·L-1,各取这两种溶液10mL分别与足量金属镁反应。下列叙述中正确的是( ) A、产生H2量:X>Y B、反应消耗镁的量:X
2、把0.05ml NaOH固体分别加入100ml下列液体中,溶液的 导电能力变化不大的是 ( ) A.蒸馏水 ·L-1 的盐酸 ·L-1 的 醋酸 D. 0.5ml·L-1 的 NH4Cl 溶液
4、石灰乳悬浊液中存在下列平衡向一定量的此悬浊液中加入少量生石灰,维持温度不变,下列说法中正确的是( ) A、溶液中Ca2+数目减少 B、c(Ca2+)增大 C、溶液中c(OH-)不变 D、溶液中OH-数目不变
高中化学人教版 (新课标)选修4 化学反应原理第一节 弱电解质的电离教学演示课件ppt: 这是一份高中化学人教版 (新课标)选修4 化学反应原理第一节 弱电解质的电离教学演示课件ppt,共9页。PPT课件主要包含了知识回顾,强弱电解质,只有水合离子,电离方程式用“”,共价化合物溶于水,纯净物,混合物,化合物,物质的分类,易溶强电解质等内容,欢迎下载使用。
化学选修4 化学反应原理第一节 弱电解质的电离教课内容课件ppt: 这是一份化学选修4 化学反应原理第一节 弱电解质的电离教课内容课件ppt,共38页。PPT课件主要包含了灯泡亮,相关知识复习,电解质与非电解质,灯泡越亮,导电性越强,弱电解质,化合物,非电解质,电解质,强电解质等内容,欢迎下载使用。
人教版 (新课标)选修4 化学反应原理第一节 弱电解质的电离评课课件ppt: 这是一份人教版 (新课标)选修4 化学反应原理第一节 弱电解质的电离评课课件ppt,共34页。PPT课件主要包含了二强弱电解质,课堂练习,记住A,思考与讨论,第二课时,六知识拓展,强酸与弱酸的比较,思考与练习等内容,欢迎下载使用。














