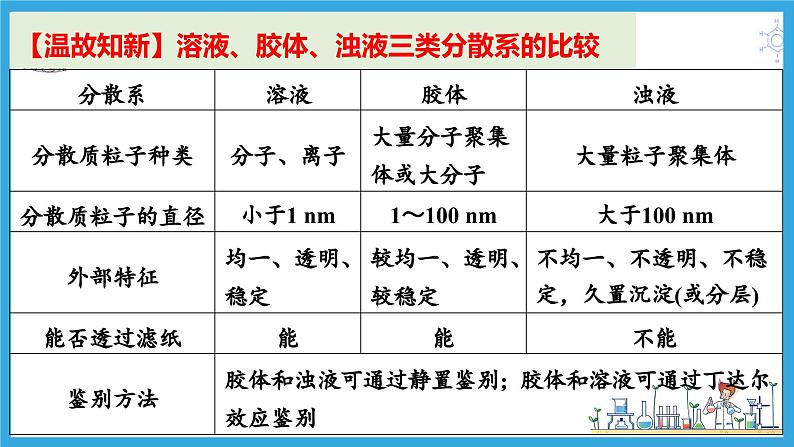





- 1.1.1 简单分类法及其应用(教学课件) 课件 0 次下载
- 1.1.2 分散系及其分类(教学课件) 课件 0 次下载
- 1.2.1 电解质的电离(教学课件) 课件 0 次下载
- 1.2.2 离子反应(教学课件) 课件 0 次下载
- 1.2.3 离子反应的应用(教学课件) 课件 0 次下载
高中化学人教版 (2019)必修 第一册第一节 物质的分类及转化教学ppt课件
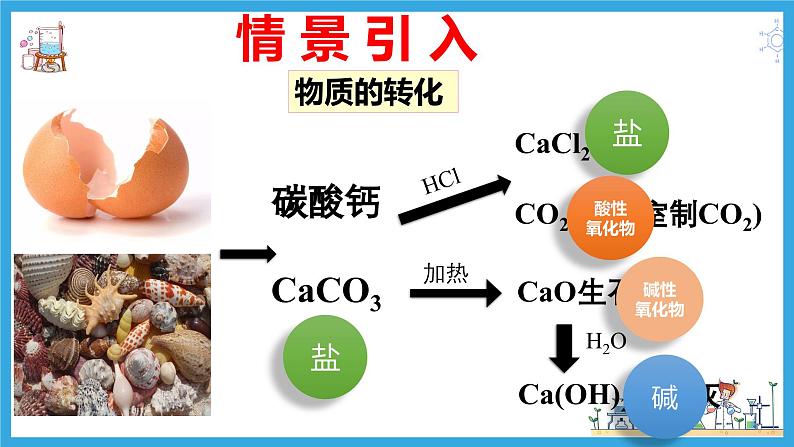
展开1.1 物质的分类及转化第三课时 物质的转化
1.能根据物质的微观结构预测物质在特定条件下可能具有的性质和可能发生的变化,并能解释其原因。2.同类物质具有相似的性质,一定条件下各类物质可以相互转化。
CaCl2CO2(实验室制CO2)
CuO+H2SO4===CuSO4+H2O
从微观角度来看,不同的酸溶液中都含有______。
Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
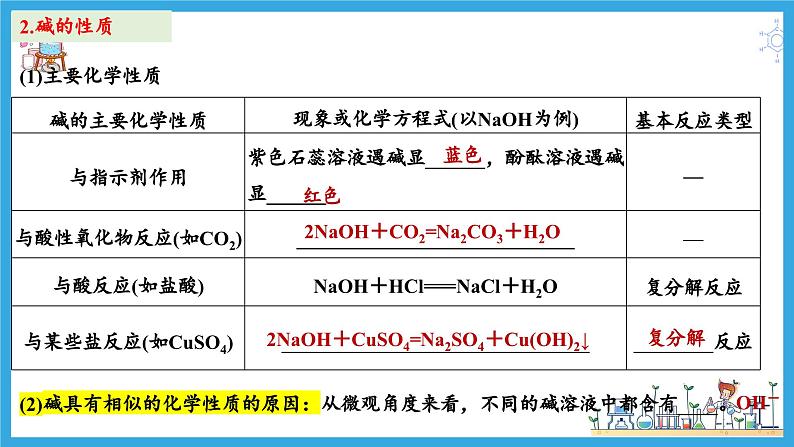
2NaOH+CO2=Na2CO3+H2O
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
(2)碱具有相似的化学性质的原因:从微观角度来看,不同的碱溶液中都含有____。
(2)写出上述物质中能与氢氧化钙反应的化学方程式并注明反应类型:① , ;② , ;③ , ;④ , 。
Ca(OH)2+2HNO3===Ca(NO3)2+2H2O
Ca(OH)2+CO2===CaCO3↓+H2O
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
Ca(OH)2+CuCl2===Cu(OH)2↓+CaCl2
【思想在线】(1)指出表中各物质的类别:
(2)同一类盐具有相似的化学性质的原因: 从微观角度来看,组成上含有相同的________________。
Fe+CuSO4 = FeSO4+Cu
Na2CO3+2HCl=2NaCl+H2O+CO2↑
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
CuSO4+Ba(NO3)2=BaSO4↓+Cu(NO3)2
CaO+H2O = Ca(OH)2
Zn+H2SO4 = ZnSO4+H2↑
2HCl+CaCO3 = CaCl2+H2O+CO2↑
为什么不同的酸、碱或碳酸盐具有相似的化学性质?
HClH2SO4HNO3
NaOHKOHBa(OH)2
Na2CO3 K2CO3(NH4)2CO3
为什么酸、碱、碳酸正盐都各自具有相似的化学性质?
1.(2022·安阳五一中学高一月考)向下列物质的溶液中滴加稀硫酸或氯化镁溶液时,均有白色沉淀生成的是( )A.BaCl2 B.Ba(OH)2C.Na2CO3 D.KOH
2.在一定条件下,能跟某些酸、碱、盐发生反应的物质是( )
A.Na2CO3 B.CuOC.CaCO3 D.CO2
【题后归纳】(1)认识物质的通性既要注意一般情况,也要注意特殊情况。 如金属+酸→盐+氢气, 但铜与盐酸不反应,与其他酸反应也不产生氢气。(2)盐和盐反应、盐和碱反应是复分解反应,反应物都必须是可溶性的。
在化学变化过程中,______是不会改变的。即化学反应中______守恒。
【实例1】以钙为例,用化学方程式表示钙及其化合物之间的转化关系并指明反应类型。
①____________________________,__________;②____________________________________,__________;③________________________________,__________;④___________________________________________,____________;⑤__________________________________________,____________;⑥___________________________________________,____________。
2Ca+O2===2CaO
CaO+H2O===Ca(OH)2
CaO+CO2===CaCO3
Ca(OH)2+2HCl===CaCl2+2H2O
CaCO3+2HCl===CaCl2+CO2↑+H2O
【举一反三】以钙、氧化钙、氢氧化钙、硫酸钙为例认识金属元素的相关类型物质转化关系:
【实例2】碳及其化合物之间的转化关系如图所示:
写出图中序号所示转化所需反应物的化学式:①______;②________;③________________;④________;⑤________________ (答案合理即可)。
【举一反三】以碳、二氧化碳、碳酸、碳酸钠为例认识非金属元素的相关类型物质转化关系:
2.研究物质的思维路径
基于上述转化关系,从物质分类的角度,寻找从单质到盐的转化规律。
3.物质转化的应用——物质制备方法的选择
(1)确定物质制备方法的依据 ①物质的组成和性质; ②物质之间的转化关系。(2)工业生产中最适当方法的选择
3. 意义 根据物质的组成和性质,以及物质之间的转化关系,我们可以确定制取某类物质的可能方法。 例如,要想制取某种碱,通常可以采取两种方法: 碱性氧化物与水发生反应; 盐与另一种碱发生反应。
【实例】:工业上制取NaOH①不采用Na2O与H2O反应的原因:__________________________________。②主要采用的方法:________________。③过去曾采用的方法:Ca(OH)2+Na2CO3===__________________________。
Na2O作为原料,来源少、成本高
CaCO3↓+2NaOH
1.利用下列流程制取烧碱,在整个流程中没有涉及的化学反应类型是( )
A.化合反应 B.置换反应C.复分解反应 D.分解反应
单质、氧化物、酸、碱、盐之间的转化关系
1.一同学设计了两种由CuO→Cu的实验方案:
大家认为方案二优于方案一,理由是:①节约能源;②Cu产率高;③产品纯净;④操作安全。其中,评价正确的是( )A.①②③ B.①②④ C.①③④ D.②③
2.模型认知是建立宏观与微观联系的思维方法。工业上制硝酸的主要反应之一是氨的催化氧化,该反应的微观示意图如图。下列说法正确的是( )
A.该反应属于复分解反应B.反应前后分子种类没有发生变化C.反应物、生成物中共有三种氧化物D.甲的相对分子质量为17
3.(2021·昆明八中高一月考)下列物质间的转化不能一步实现的是( )A.CaO―→Ca(OH)2―→CaSO4B.Fe2O3―→FeCl3―→Fe(OH)3C.C―→CO―→CaCO3D.Cu―→CuO―→CuSO4
下列说法正确的是( )A.铜绿属于碱 B.乙为氧化铜C.④为复分解反应 D.⑤为分解反应
5.铜器久置于空气中会和空气中的水蒸气、二氧化碳、氧气作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”(碱式碳酸铜),“铜绿”能跟酸反应生成铜盐、二氧化碳和水。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。
6.甲、乙、丙、丁分别是Na2CO3、AgNO3、BaCl2、盐酸四种无色溶液中的一种,它们两两反应后的现象如下:甲+乙―→沉淀;甲+丙―→沉淀;乙+丙―→沉淀;丙+丁―→沉淀;乙+丁―→无色无味气体。则甲、乙、丙、丁四种溶液依次是( )A.BaCl2 Na2CO3 AgNO3 盐酸B.BaCl2 Na2CO3 盐酸 AgNO3C.Na2CO3 盐酸 AgNO3 BaCl2D.AgNO3 盐酸 BaCl2 Na2CO3
高中化学人教版 (2019)必修 第一册第一节 物质的分类及转化教学ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第一节 物质的分类及转化教学ppt课件,文件包含第1课时初步认识比热容pptx、加热水和煤油mp4、比较水沙石的比热容mp4、比较金属的比热熔冰mp4、水和煤油的吸热能力对比mp4、水和煤油的吸热能力对比swf等6份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
化学必修 第一册第一节 物质的分类及转化教学课件ppt: 这是一份化学必修 第一册第一节 物质的分类及转化教学课件ppt,共22页。PPT课件主要包含了学习目标,第3课时物质的转化,碳酸钙CaCO3等内容,欢迎下载使用。
高中人教版 (2019)第一节 物质的分类及转化教案配套课件ppt: 这是一份高中人教版 (2019)第一节 物质的分类及转化教案配套课件ppt,共24页。PPT课件主要包含了物质的转化,酸的化学通性,紫色石蕊试液遇酸变红,盐+H2↑,置换反应,盐+水,复分解反应,新盐+新酸,碱的化学通性,盐的化学通性等内容,欢迎下载使用。













