





高中化学人教版 (2019)必修 第一册第一章 物质及其变化第三节 氧化还原反应授课课件ppt
展开用双线桥法表示下列方程式电子转移的方向和数目
+4 -1 +2 0
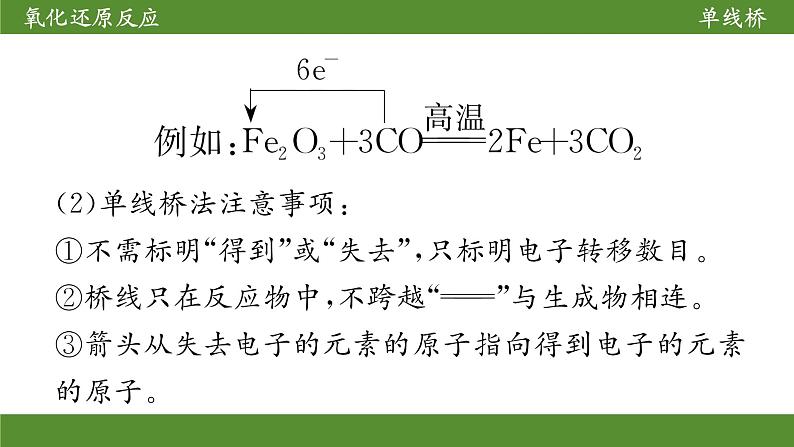
该反应中,只有一部分氯原子化合价发生变化,还有一部分氯原子价态不变,故失去电子数为2×e-,而不是4 ×e-。
甲醛(HCHO)是室内空气污染的主要污染物之一,活性高锰酸钾球是以高锰酸钾为原料,以活性氧化铝为载体,经过二次深加工的一种产品,可用于空气净化除甲醛。其反应原理是:5HCHO+4KMnO4+6H2SO4===5CO2↑+K2SO4+4MnSO4+11H2O请分析该反应是否属于氧化还原反应?
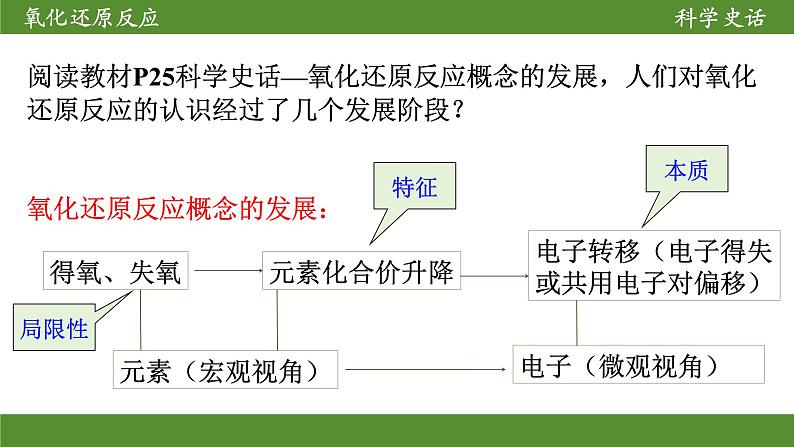
氧化还原反应概念的发展:
电子转移(电子得失或共用电子对偏移)
阅读教材P25科学史话—氧化还原反应概念的发展,人们对氧化还原反应的认识经过了几个发展阶段?
思考:1.有单质参加或生成的化学反应一定是氧化还原反应吗?
2.当反应中一种元素被氧化时,一定有另一种元素被还原吗?
3.某元素从游离态到化合态,该元素一定被氧化吗?
得电子,化合价降低,被还原
失电子,化合价升高,被氧化
氧化性:物质得电子性质,氧化剂具有氧化性。 且物质得电子越容易氧化性越强
还原性:物质失电子性质,还原剂具有还原性。 且物质失电子越容易还原性越强
物质氧化性还原性的强弱和其得失电子的能力有关。与得失电子的数目无关。
(1)2H2+O2===2H2O(2)4P+5O2===2P2O5(3)Fe+H2SO4===FeSO4+H2↑(4)2HgO===2Hg+O2↑
1、分析下列氧化还原反应中元素化合价的变化情况,指出氧化剂和还原剂。
易错警示 (1)并非价态越高氧化性越强,在HClO中氯元素化合价为+1价,在HClO4中氯元素的化合价为+7价,但HClO的氧化性比HClO4强。(2)由于有些氧化还原反应中,氧化剂或还原剂并没有全部发生氧化还原反应,因此在求氧化剂或还原剂的质量或两者的比例时要格外注意。
MnO2+4HCl(浓 ) == MnCl2+2H2O+Cl2↑
氧化剂和还原剂的比例为1:2其中HCl既体现出还原性也体现出酸性。
易错警示 (3)元素由化合态变为游离态时,该元素不一定被还原。如:Cu2+→Cu时,铜元素被还原,Cl-→Cl2时, 氯元素被氧化。(4)同一种氧化剂(或还原剂)所对应的还原产物(或氧化产物)不是一成不变的,取决于还原剂(或氧化剂)的性质、反应条件、反应物的浓度、反应介质的酸碱性等多种因素。如KMnO4在酸性溶液中的还原产物一般是Mn2+;在中性或碱性溶液中还原产物一般是锰的较高价态化合物,如MnO2、K2MnO4等。
从化合价角度预测物质的氧化性、还原性
活动1、预测下列物质的性质(氧化性、还原性)
可变为-2、-1价,氧化性
化合价的角度考虑氧化性、还原性
高中化学人教版 (2019)必修 第一册第一章 物质及其变化第三节 氧化还原反应教学课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第一章 物质及其变化第三节 氧化还原反应教学课件ppt,文件包含第1课时初步认识比热容pptx、加热水和煤油mp4、比较水沙石的比热容mp4、比较金属的比热熔冰mp4、水和煤油的吸热能力对比mp4、水和煤油的吸热能力对比swf等6份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
高中化学人教版 (2019)必修 第一册第三节 氧化还原反应教学课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第三节 氧化还原反应教学课件ppt,共14页。PPT课件主要包含了素养发展目标,氧化剂,还原剂,氧化产物,还原产物,MnO2,HCl,MnCl2,Cl2,思考交流等内容,欢迎下载使用。
化学必修 第一册第三节 氧化还原反应背景图课件ppt: 这是一份化学必修 第一册第三节 氧化还原反应背景图课件ppt,共19页。PPT课件主要包含了维生素C,还原产物,氧化剂,归纳总结,练一练,FeCl3,FeCl2,Cl2,还原性,氧化性等内容,欢迎下载使用。













