





初中化学鲁教版 (五四制)九年级全册3 海水“制碱”背景图ppt课件
展开1.知道工业制取纯碱的化学反应原理2.知道氨碱法制取纯碱的流程及注意事项,了解侯氏制碱法的历史及优点,树立探究精神。3.了解纯碱在日常生活或工农业生产中的应用
为什么加了碱面的面团蒸出的馒头没有酸味且疏松多孔呢?
在工业上以氯化钠为主要原料,制取碳酸钠。
纯碱(Na2CO3)
1862年,比利时化学家索尔维实现了氨碱法的工业化。这种方法能连续生产,产量大,质量高,省劳动力,成本低廉。掌握氨碱法的资本家为了独享此项技术成果,他们采取了严密的保密措施,使外人对此新技术一无所知。一些技术专家想探索此项技术秘密,大都以失败告终。不料这一秘密竟被一个中国人运用智慧摸索出来了。 这个中国人就是侯德榜
1921年10月侯德榜接受了永利碱业公司的聘请,毅然从美国启程回国,决心自己开发制碱新工艺。经过600多次研究实验,分析了2000多个样品,历时5年,于1942年发明并创立了举世闻名的“侯氏制碱法”。
如果要你来制备纯碱,你会考虑哪些方面?
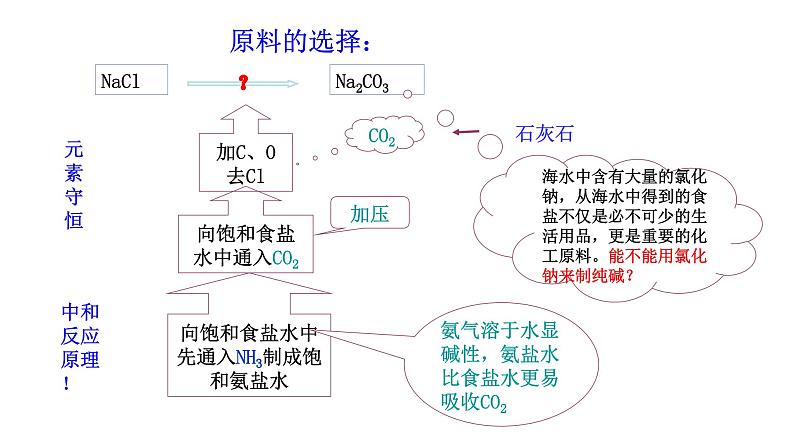
向饱和食盐水中通入CO2
向饱和食盐水中先通入NH3制成饱和氨盐水
氨气溶于水显碱性,氨盐水比食盐水更易吸收CO2
海水中含有大量的氯化钠,从海水中得到的食盐不仅是必不可少的生活用品,更是重要的化工原料。能不能用氯化钠来制纯碱?
海水“制碱”的原料: 饱和食盐水、石灰石、氨气
↓ ↓ NaCl 、H2O CO2
↓使CO2更易被食盐水吸收
NaCl +H2O + NH3+CO2 ==== NaHCO3+ NH4Cl
2NaHCO3 Na2CO3+CO2↑+ H2O
在相同的温度下,NaHCO3溶解度比NH4Cl小,先析出晶体。
3、氨盐水吸收二氧化碳后生成的碳酸 氢 钠和氯化铵,那种物质首先析出?为什么?(提示:根据课本15页溶解度曲线)
2、在生产过程中为什么要先通入氨气得到饱和的氨盐水后再通入二氧化碳?
使溶液显碱性,吸收更多的 CO2以生成更多的碳酸氢钠。
NaHCO3,在同一温度下NaHCO3溶解度小
1、为什么采用饱和的食盐水?
提出方案 ——流程分析
↑CaCO3 = CaO+CO2 CaO+H2O=Ca(OH)2 Ca(OH)2+2NH4C1=CaC12+2NH3↑+2H2O
海水“制碱”工业生产的实际流程
实验室制纯碱-Na2CO3 氨碱法(侯氏制碱法)
1.析出NaHCO3后的溶液中是否含有NaHCO3?
2.析出NaHCO3后的溶液是NaHCO3的饱和溶液吗?
3.析出NaHCO3后的溶液中除了含有NaHCO3外,主要还含有什么物质?
阅读课本44页多识一点,了解索尔维的氨碱法制纯碱的优缺点和侯德榜的侯氏制碱法的优点,并通过看微课,感悟侯德榜的爱国精神和科学素养。
Ca(OH)2+2NH4CI=CaCI2+2NH3↑+2H2O
氨碱法(索尔维制碱法)
两者原理相同,区别在与对过滤出NaHCO3后的母液的处理方法:侯氏制碱法向滤出NaHCO3晶体后的NH4Cl溶液中加入食盐,使其中的NH4Cl单独结晶析出,用作氮肥, NaCl溶液则可循环使用。
联合制碱法(侯氏制碱法)
碳酸钠的物理性质和用途
(1)碳酸钠在生活中的用途
白色粉末,易溶于水(其水溶液呈碱性。纯碱不是碱,是盐)
【典例1】家庭或企业加工馒头、面包和饼干等食品时,常在面粉中加入膨松剂(如碳酸氢钠),蒸制或烘焙食品中产生大量气体,使面团疏松、多孔,制作的食品松软或酥脆,易于消化吸收。阅读上面信息后,回答:(1)信息中提供的膨松剂是 (填化学式);(2)碳酸氢钠是一种 性的化合物(填“可溶”或“不溶”);(3)碳酸氢钠能使蒸制或烘焙的食品疏松多孔,原理是(用化学方程式解释) 。
知识点一、NaHCO3的性质
【典例2】(2021·梧州中考)1926年,我国化工专家侯德榜创造出的“侯氏制碱法”,结束了由美、英、法等国垄断世界纯碱市场的时代。其基本工业流程如图:已知:常温下,氨气的溶解度很大,CO2的溶解度很小。回答下列问题:(1)纯碱的化学式为 。(2)“侯氏制碱法”的反应温度一般控制为30﹣35℃,因为在此温度时,NaHCO3的溶解度较____(填“大”或“小”)。(3)若向饱和食盐水中先通入CO2,会导致NaHCO3产量减少,原因是 。 (4)写出步骤①、②发生的总反应方程式 。 (5)“侯氏制碱法”中能循环利用的物质有NaCl、H2O和 。
知识点二、氨碱法制纯碱
二氧化碳溶解度小,不利于碳酸氢根的形成
NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl
1.侯德榜是我国制碱工业的先驱。侯氏制碱法中的“碱”是指其化学式为( )A.Na2CO3B.NaHCO3C.NaOHD.NaCl2. 下列物质俗名对应正确的是( )A. NaOH—苛性钠B. Ca(OH)2—生石灰C. Na2CO3—烧碱D. NaHCO3—苏打
3.下列溶液分别能跟硫酸铜、盐酸、碳酸钠溶液反应,并产生不同现象的是( )A.AgNO3 B.Ca(OH)2 C.H2SO4 D.NaOH4.妈妈在洗碗筷时,经常在水中加入一种物质,很快就能将“油乎乎”的菜盘洗得干干净净。妈妈在水中加入的物质可能是( )A.汽油 B.烧碱 C.纯碱 D.食盐水
5.判断下列反应能否进行:
AgNO3+ FeCl3=====AgCl+ NaNO3CaCO3+ NaOHNa2SO4+ HCl Fe(OH)3+ H2SO4====
3AgCl +Fe(NO3)3
不反应,盐和盐反应时须均可溶
不反应,碱和盐反应时须均可溶
不反应,生成物中无气体、沉淀或水
Fe2(SO4)3 + H2O
6、氯化钠是必不可少的生活用品,更是重要的化工原料。(1)“烧干海水变银山”是郭沫若对海南莺歌海盐场的赞美诗作。海水“晒盐”是通过 (填“蒸发结晶”或“降温结晶”)的方法获取食盐。(2)抗日战争期间,我国著名制碱专家侯德榜打破西方国家对制碱技术的垄断,创立“侯氏制碱法”,促进了世界制碱技术的发展。其生产原理示意图如图:①制碱过程中,可以循环利用的物质是 ,产物中可作氮肥的是 ;②产物中 NaHCO3比NH4Cl先结晶析出。请结合生产原理及如图解释其原因: 。
同温下碳酸氢钠的溶解度比氯化铵小,且反应时生成碳酸氢钠的质量比氯化铵大
氨碱法制纯碱
NaCl+NH3+CO2+H2O===NaHCO3+NH4Cl
初中化学鲁教版 (五四制)九年级全册3 海水“制碱”多媒体教学课件ppt: 这是一份初中化学鲁教版 (五四制)九年级全册3 海水“制碱”多媒体教学课件ppt,文件包含第2课时纯碱的性质ppt、复分解反应wmv、复分解反应发生的条件mp4、碳酸钠碳酸氢钠分别与稀盐酸的反应wmv、碳酸钠溶液与澄清石灰水反应wmv等5份课件配套教学资源,其中PPT共39页, 欢迎下载使用。
鲁教版 (五四制)1 溶液的形成教课课件ppt: 这是一份鲁教版 (五四制)1 溶液的形成教课课件ppt,文件包含第1课时溶解的过程乳化现象ppt、什么是溶液mp4、溶解时的吸热与放热mp4、肥皂为什么能去污mp4等4份课件配套教学资源,其中PPT共31页, 欢迎下载使用。
鲁教版 (五四制)九年级全册第六单元 化学与社会发展2 化学与材料研制优秀ppt课件: 这是一份鲁教版 (五四制)九年级全册第六单元 化学与社会发展2 化学与材料研制优秀ppt课件,文件包含第二节化学与材料研制ppt、塑料mp4、复合材料mp4、白色污染mp4等4份课件配套教学资源,其中PPT共39页, 欢迎下载使用。













