



高中化学人教版 (2019)必修 第一册第三节 氧化还原反应课文内容课件ppt
展开1.认识氧化还原反应的本质是电子的转移。2.能举例说明生产、生活中常见的氧化还原反应。3.熟记常见物质的化合价,并能通过化合价的升降,判断氧化还原反应。
建立用微粒观认识氧化还原反应,形成宏观辨识与微观探析的化学学科核心素养。
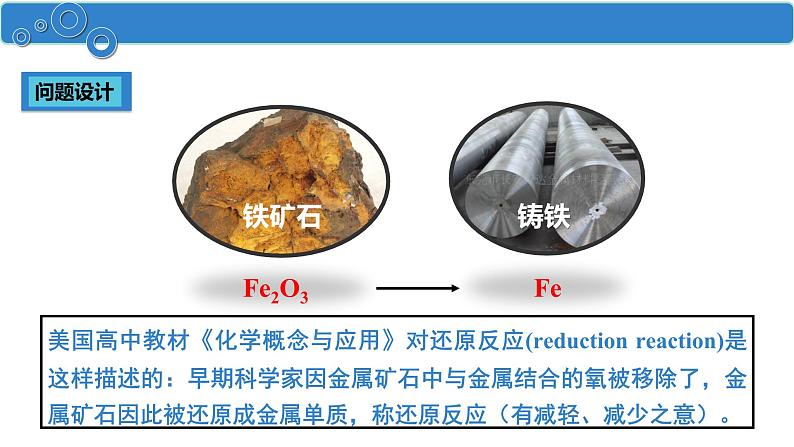
美国高中教材《化学概念与应用》对还原反应(reductin reactin)是这样描述的:早期科学家因金属矿石中与金属结合的氧被移除了,金属矿石因此被还原成金属单质,称还原反应(有减轻、减少之意)。
氧化反应和还原反应是同时进行的,这样的反应称为氧化还原反应。
从得氧失氧角度分析氧化还原反应
完成下列反应的方程式,并思考问题:
2.标出以上反应中各元素的化合价,你能发现什么规律?
1.判断哪些物质发生氧化反应、那些发生还原反应?
(1)一氧化碳还原氧化铜(2)氢气还原氧化铜(3)碳与水高温下的反应
氧化反应:物质所含元素化合价升高的反应
还原反应:物质所含元素化合价降低的反应
凡是有元素化合价升降的化学反应
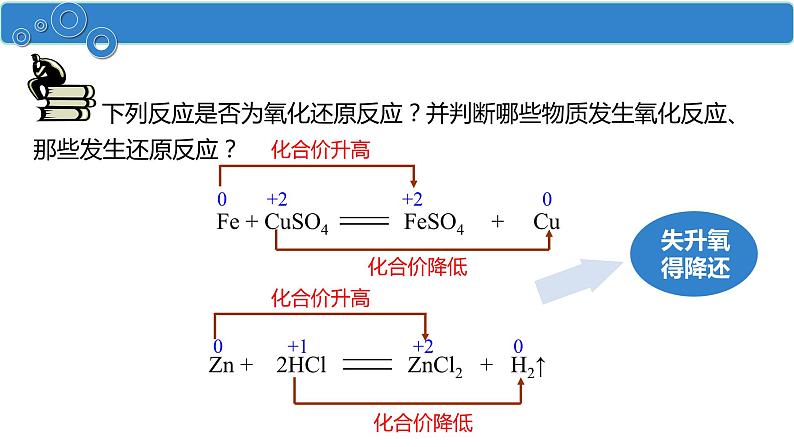
下列反应是否为氧化还原反应?并判断哪些物质发生氧化反应、那些发生还原反应?
0 +2 +2 0
0 +1 +2 0
判断下列反应是否是氧化还原反应:
氧化还原反应中元素化合价变化的原因:
1.该反应中发生反应的微粒是什么?
2.NaCl中存在的微粒是什么?
3.它们是如何转化的?
失去2×e-电子,化合价升高,被氧化
2Na + Cl2 ==== 2NaCl
0 0 +1 -1
得到2×e-电子,化合价降低,被还原
H Cl
氧化还原的实质是电子的转移
2. 氧化还原反应的实质
电子的转移(电子的得失和电子对的偏移)
氧化还原反应与四种基本反应类型的关系:
1.下列反应属于氧化还原反应的是( )
A.CaCO3+2HCl === CaCl2+H2O+CO2↑B.2NaHCO3 === Na2CO3+H2O+CO2↑C.Cl2+2NaOH === NaCl+NaClO+H2OD.NaBr+AgNO3 === AgBr↓+NaNO3
2. 下列变化中,属于还原反应的是( )
A.Cl-→Cl2 B.FeCl2→FeCl3C.C→CO2 D.KMnO4→MnO2
3.下列说法正确的是( )
A.化合价升高的反应是还原反应B.氧化还原反应一定有氧元素参加C.氧化反应与还原反应同时发生D.反应物要么发生氧化反应,要么发生还原反应
4.已知CaH2中Ca为+2 价,对于CaH2+2H2O===Ca(OH)2 +2H2↑,下列说法正确的是( )
A.H2都是还原产物 B.H2都是氧化产物C.CaH2中的氢元素既被氧化又被还原D.氧化产物与还原产物的质量比为1∶1
高中化学人教版 (2019)必修 第一册第一章 物质及其变化第三节 氧化还原反应精品ppt课件: 这是一份高中化学人教版 (2019)必修 第一册<a href="/hx/tb_c161975_t3/?tag_id=26" target="_blank">第一章 物质及其变化第三节 氧化还原反应精品ppt课件</a>,共33页。PPT课件主要包含了考纲要求,认识氧化还原反应,氧化反应,Fe2O3,还原反应,一个反应,氧化还原反应,氧化还原反应的特征,氯化钠的形成,氯化氢的形成等内容,欢迎下载使用。
化学必修 第一册第三节 氧化还原反应教学课件ppt: 这是一份化学必修 第一册第三节 氧化还原反应教学课件ppt,共26页。PPT课件主要包含了生活中的氧化还原反应,学习目标,升失氧,降得还等内容,欢迎下载使用。
化学人教版 (2019)第三节 氧化还原反应优质课ppt课件: 这是一份化学人教版 (2019)第三节 氧化还原反应优质课ppt课件,共21页。PPT课件主要包含了用途广泛的铁,铁矿石等内容,欢迎下载使用。













