






人教版九年级下册课题1 生活中常见的盐课前预习课件ppt
展开写出下列反应的化学方程式(1)氢氧化钠与硫酸(2)碳酸钠与盐酸(3)碳酸氢钠与盐酸(4)碳酸钙与盐酸(5)碳酸钠与澄清石灰水
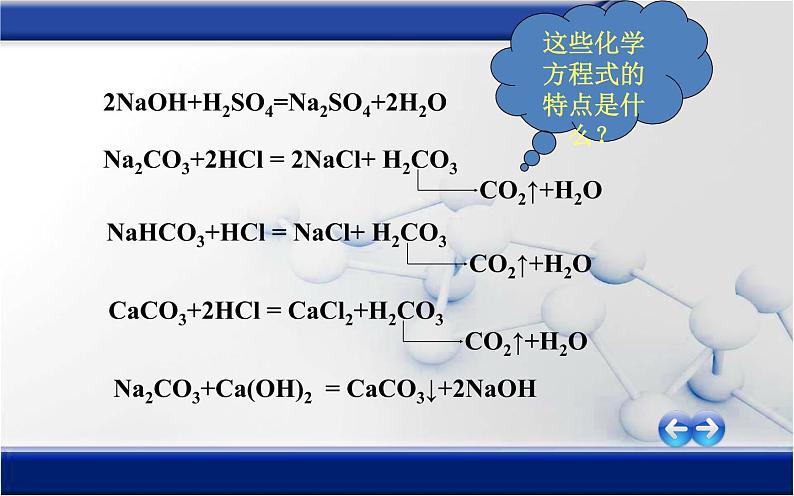
2NaOH+H2SO4=Na2SO4+2H2O
Na2CO3+2HCl = 2NaCl+ H2CO3
NaHCO3+HCl = NaCl+ H2CO3
CaCO3+2HCl = CaCl2+H2CO3
Na2CO3+Ca(OH)2 = CaCO3↓+2NaOH
这些化学方程式的特点是什么?
1.定义:两种化合物相互交换成分,生成另外两种化合物的反应
关键词:两种化合物 、交换成分
CuSO4+NaOH=Na2SO4+Cu(OH)2 ↓
上述两个反应是否属于复分解反应?观察到的现象有什么共同之处?
酸碱中和反应是否也属于复分解反应?生成物中相同的物质是什么?
如:2NaOH+H2SO4 = Na2SO4+2H2O
碳酸盐与盐酸发生复分解反应时,可观察到的共同现象是什么?
如:CaCO3+2HCl = CaCl2+2H2O+CO2 ↑
2. 复分解反应发生的条件
(1)反应一般在溶液中
产生气泡,该气体能使澄清石灰水变浑浊
稀H2SO4与K2CO3溶液发生了反应
稀H2SO4与Ba(NO3)2溶液发生了反应
判断下列各组物质能否发生复分解反应,能,请写出化学方程式。(1)碳酸钠溶液与氯化钙溶液 (2)氯化镁溶液与硫酸铜溶液(3)氢氧化钠溶液与氯化镁溶液
Na2CO3 + CaCl2 = 2NaCl + CaCO3↓
2NaOH + MgCl2 = 2NaCl + Mg(OH)2↓
(4)氢氧化钾与稀盐酸(5)碳酸钾与稀硫酸 (6)氯化钠溶液与硝酸钾溶液
KOH + HCl = KCl + H2O
K2CO3 + H2SO4 = K2SO4 + H2O + CO2↑
除去食盐中的氯化镁、氯化钙杂质的方法?写出有关的化学方程式。
2NaOH+MgCl2 = 2NaCl +Mg(OH)2 ↓ Na2CO3+CaCl2 = CaCO3↓+2NaCl
化合反应:A+B→AB
分解反应:AB→A+B
置换反应:A+BC→AC+B
复分解反应:AB+CD→AD+CB
CaO+H2O = Ca(OH)2
H2CO3= H2O+CO2 ↑
Fe+CuSO4 = FeSO4+Cu
CuSO4+BaCl2 = BaSO4↓+CuCl2
1.你知道什么样的反应为复分解反应吗?你能判断两种化合物溶液混合是否能发生反应吗?
2.基本反应类型包括哪些?各有什么特点?
3.纯净物中可分为哪几类?化合物中的酸碱盐的划分的依据是什么?
1. 医疗上可以用含有氢氧化镁的药物治疗胃酸过多,其反应的化学方程式为:Mg(OH)2 + 2HCl=MgCl2 + 2H2O,该反应属于( )A.化合反应 B.分解反应C.置换反应 D.复分解反应
2.下列各组物质的溶液,不能发生复分解反应的是 ( ) A. HCl和Ca(OH)2 B. Na2CO3和H2SO4 C. AgNO3和BaCl2 D. KCl和CuSO4
3. 在水溶液中,一般不会与其他物质发生复分解反应的物质是( ) A. KCl B. NaNO3 C. HNO3 D. Mg(OH)2
4. 下列各组物质的转变中不能一步实现的是( ) A. Na2CO3→NaCl B. K2SO4→Na2SO4 C. CaCO3→ H2O D. Ca(OH)2→NaOH
5. 分类就是按照种类、等级或性质分别归类。依据不同的分类标准,结论也不尽相同。下列每组中有一种物质具有特殊的组成或性质,而其他两种物质的组成或性质相似。请你利用所学知识将其区分出来并说明理由。
组成的元素是两种,溶液呈中性
不含碳元素或通常为液体
组成的元素是三种或中性
化学九年级下册课题1 生活中常见的盐备课课件ppt: 这是一份化学九年级下册课题1 生活中常见的盐备课课件ppt,共26页。PPT课件主要包含了氯化钠传奇,食盐Tips,粗盐提纯,本课小结等内容,欢迎下载使用。
初中化学人教版九年级下册课题1 生活中常见的盐教案配套课件ppt: 这是一份初中化学人教版九年级下册课题1 生活中常见的盐教案配套课件ppt,共48页。PPT课件主要包含了辨一辩,酸根离子,氯化钠的分布,粗盐中的杂质,粗盐提纯,碳酸钠主要用途,碳酸钙主要用途,药品稀盐酸和石灰水,产生白色沉淀,复分解反应的条件等内容,欢迎下载使用。
化学课题1 生活中常见的盐备课课件ppt: 这是一份化学课题1 生活中常见的盐备课课件ppt,共20页。PPT课件主要包含了预习交流,实验探究宏观感知,第一组,有白色固体生成,第二组,无现象,第三组,微观解释揭示原因,复分解反应,双交换价不变等内容,欢迎下载使用。














