



初中化学人教版九年级下册课题1 生活中常见的盐教学课件ppt
展开【回顾】 请书写出实验室制取CO2的方程式。
CaCO3 + 2 HCl === CaCl2 + H2CO3
【讨论】 根据上述反应,请问Na2CO3和NaHCO3能否与稀盐酸反应?如果能反应,请问它们又会生成什么物质?
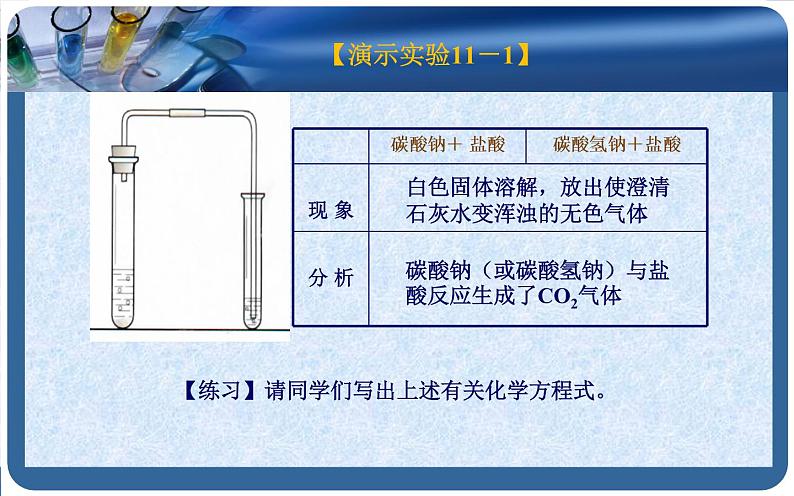
白色固体溶解,放出使澄清石灰水变浑浊的无色气体
碳酸钠(或碳酸氢钠)与盐酸反应生成了CO2气体
【练习】请同学们写出上述有关化学方程式。
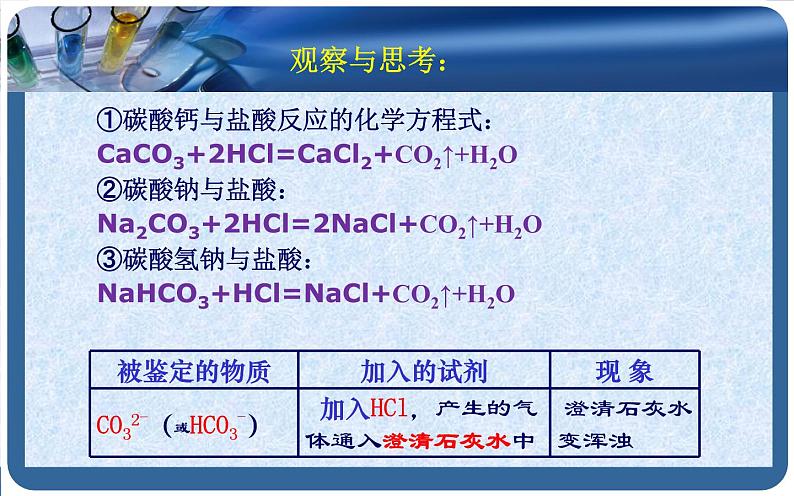
①碳酸钙与盐酸反应的化学方程式:CaCO3+2HCl=CaCl2+CO2↑+H2O②碳酸钠与盐酸:Na2CO3+2HCl=2NaCl+CO2↑+H2O③碳酸氢钠与盐酸:NaHCO3+HCl=NaCl+CO2↑+H2O
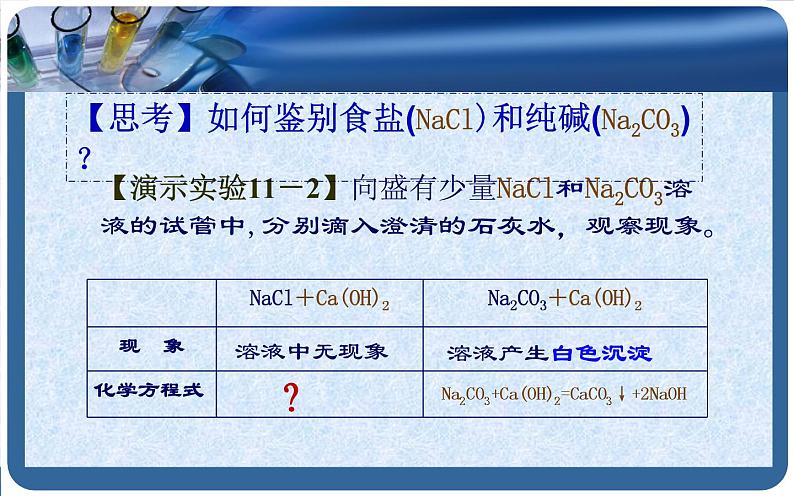
【演示实验11-2】向盛有少量NaCl和Na2CO3溶液的试管中,分别滴入澄清的石灰水,观察现象。
【思考】如何鉴别食盐(NaCl)和纯碱(Na2CO3)?
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
我国制碱工业的先驱——侯德榜
在中国化学工业史上,有一位杰出的科学 家,他为祖国的化学工业事业奋斗终生,并以独创的制碱工艺闻名于世界,他就像一块坚硬的基石,托起了中国现代化学工业的大厦,这位先驱者就是被称为“国宝”的侯德榜。 侯德榜一生在化工技术上有三大贡献。第一,揭开了苏尔维法的秘密。第二,创立了中国人自己的制碱工艺——侯氏制碱法。第三,就是他为发展小化肥工业所做的贡献。
①观察:上述几个反应有什么特点? ②讨论:由此,你又有哪些新发现? ③归纳:复分解反应的概念、一般形式与特点。
CaCO3+2HCl= CaCl2+ H2CO3
Na2CO3+2HCl= 2NaCl+ H2CO3
Na2CO3+Ca(OH)2= 2NaOH+CaCO3↓
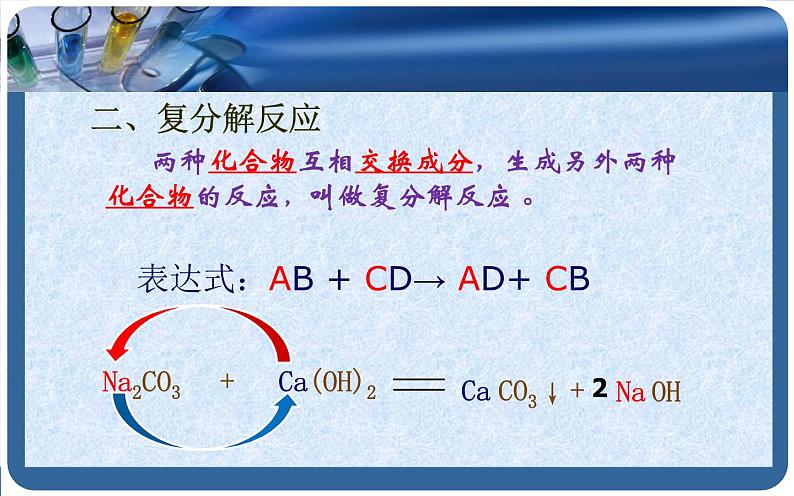
两种化合物互相交换成分,生成另外两种化合物的反应,叫做复分解反应 。
表达式:AB + CD→ AD+ CB
Na2CO3 + Ca(OH)2
【演示实验11-3】向盛有少量BaCl2溶液的试管,滴入CuSO4溶液,观察现象。
BaCl2 +CuSO4=BaSO4↓+CuCl2
【演示实验11-3】向盛有少量NaOH溶液的试管,滴入CuSO4溶液,观察现象。
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
三、复分解反应发生的条件
复分解要发生,溶液当中来进行;生成水、气或沉淀,交换成分价不变。
想一想:化学方程式是否正确?
2NaCl+Ca(OH)2 = 2NaOH + CaCl2
溶液中离子种类发生改变
CuSO4+2NaOH
2HCl + CaCO3
CaCl2+ + H2O
Ca(OH)2+ Na2CO3
溶液中离子种类没有改变
2NaCl+Ca(OH)2
2NaOH + CaCl2
酸、碱、盐的溶解性(20℃)
钾、钠、铵盐、硝酸盐都能溶于水中间;盐酸盐不溶氯化银;硫酸盐不溶硫酸钡;碳酸盐能溶只有钾、钠、铵;钾、钠、钙、钡的碱能溶;常见五酸都易溶。
注意:AgCl、BaSO4不仅不溶于水,而且还不溶于稀硝酸
1、将珍珠放入稀盐酸中,有气泡产生,生成的气体能使澄清的石灰水变浑浊,则珍珠中含有下列离子中的( )2、下列反应不属于复分解反应的是( ) A、H2SO4+Ca(OH)2=CaSO4+2H2O B、H2SO4+BaCl2=BaSO4↓ +2HCl C、2HCl+Fe=FeCl2+H2↑ D、2HCl+CaCO3=CaCl2+CO2↑+H2O
A、氯离子 B、硫酸根离子 C、碳酸根离子 D、氢氧根离子
小结: 本节课你学到了什么?
通过以上的学习和实验观察,大家不难发现盐可以和许多物质发生化学反应,你能说说盐能和哪几类物质发生反应?分别属于什么基本反应类型?
作 业
盐 + 碱 →
化学九年级下册第十一单元 盐 化肥课题1 生活中常见的盐优质教学课件ppt: 这是一份化学九年级下册第十一单元 盐 化肥课题1 生活中常见的盐优质教学课件ppt,共40页。PPT课件主要包含了纯净物,非金属,化合物,氧化物,混合物,初中化学物质的分类等内容,欢迎下载使用。
化学课题1 生活中常见的盐完美版教学ppt课件: 这是一份化学课题1 生活中常见的盐完美版教学ppt课件,共40页。PPT课件主要包含了纯净物,非金属,化合物,氧化物,混合物,初中化学物质的分类等内容,欢迎下载使用。
初中化学人教版九年级下册课题1 生活中常见的盐多媒体教学课件ppt: 这是一份初中化学人教版九年级下册课题1 生活中常见的盐多媒体教学课件ppt,共44页。PPT课件主要包含了常见的盐,食盐的用途,复分解反应的概念等内容,欢迎下载使用。














