





化学九年级下册第八单元 金属和金属材料课题 2 金属的化学性质授课课件ppt
展开初步认识金属与稀盐酸、稀硫酸的置换反应,以及与某些金属化合物溶液的置换反应。能用金属活动性顺序对有关的置换反应进行简单的判断。
一个保存至今一百年多的铝制雕像
一个使用十年的仓库铁门
铝在常温下可与氧气反应,为什么铝制品会具有很好的抗腐蚀性呢?
抗腐蚀原因:4Al + 3O2 = 2Al2O3
铝在空气中与氧气反应,其表面生成一层致密的氧化铝(Al2O3)薄膜,从而阻止铝进一步被氧化。
1.小明看到妈妈在厨房里用钢丝球用力擦洗铝锅上的污垢,立即喊起来:“妈妈,不能用钢丝球擦。”你知道为什么吗?
除去铝锅表面致密的的氧化铝薄膜,就不能保护里层的铝不再与氧气反应,使铝锅容易被腐蚀。
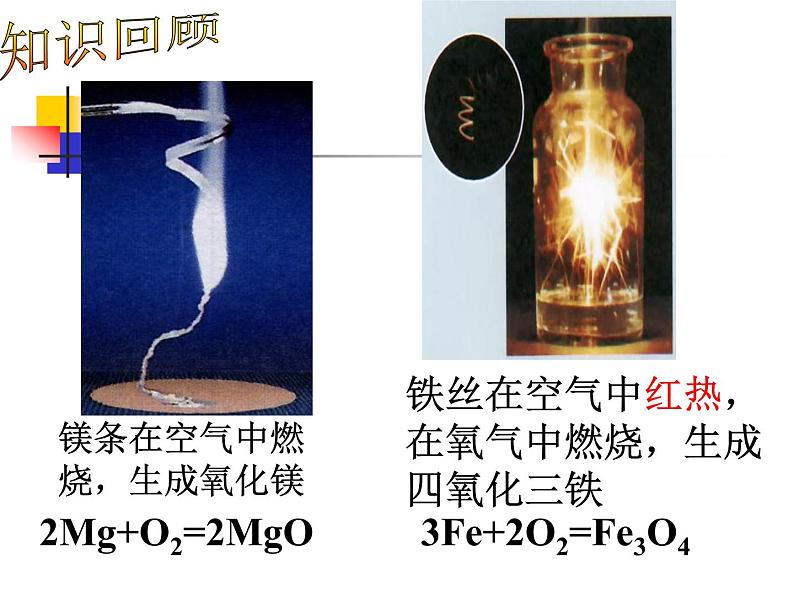
铁丝在空气中红热, 在氧气中燃烧,生成四氧化三铁
镁条在空气中燃烧,生成氧化镁
2Mg+O2=2MgO
3Fe+2O2=Fe3O4
“真金不怕火炼”说明:
金的化学性质不活泼,在高温时也不与氧气反应。
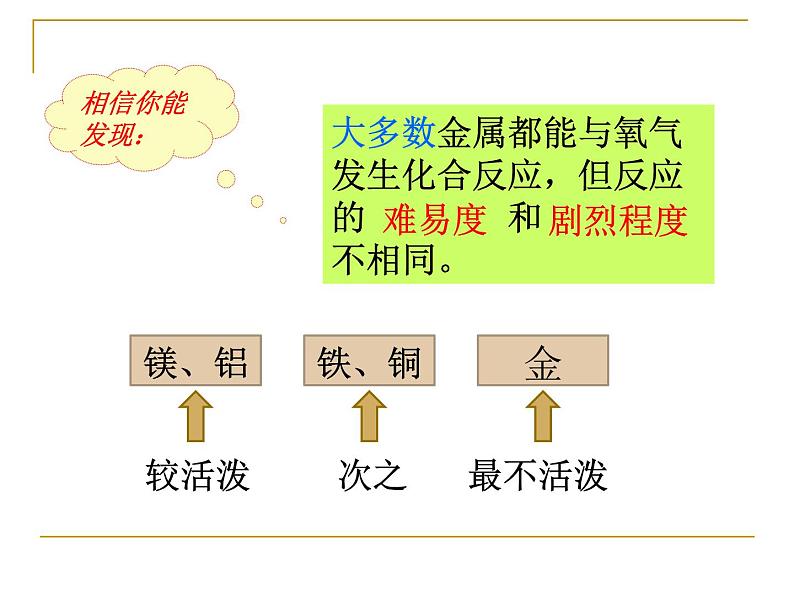
结合书中内容,和上述实验现象:1.镁、铝在常温下就能与氧气反应。2.铁、铜在常温下几乎不与氧气反应,但在高温时能与氧气反应。3.金即使在高温时也不与氧气反应。
大多数金属都能与氧气发生化合反应,但反应的 和 不相同。
一种可燃性气体的发现 16世纪中叶,瑞士化学家帕拉塞斯和17世纪英国化学家卡文迪许以及其他一些化学家,都发现有些金属与酸反应可以生成一种可燃性气体,同时在空气中燃烧火焰为淡蓝色,并且发现不同金属反应的剧烈程度不一样。 请你猜想这种气体是什么?
(Henry Cavendish,1731~1810年)
在4支试管里分别放入两小块铜、铁、锌、镁,再依次稀盐酸(或稀硫酸),仔细观察金属表面与溶液的变化,比较反应的剧烈程度。请记录实验现象。
镁、锌、铁、铜与盐酸的反应
活泼性:Mg>Zn>Fe>Cu
根据反应的难易和剧烈程度不同,把金属分为活泼金属和不活泼金属。
单质+化合物→单质+化合物由一种单质与一种化合物反应,生成另一种单质与另一种化合物的反应。
单质 化合物 化合物 单质
思考:你知道哪些反应类型?
化合反应:A + B → AB(多变一)分解反应:AB →A + B (一变多)
置换反应: A+BC→
AC+B(A把B置换出来)
1.下列反应中,属于置换反应的是( ) A. 2H2O2 = 2H2O+ O2↑ B. CuO+CO = Cu+CO2 C. H2+CuO = Cu+H2O D. CO2+H2O = H2CO3
2.下列各种金属,不能将稀盐酸中的氢置换出来的是( )A、镁B、锌C、铁D、铜
1、很多金属都能与盐酸或稀硫酸发生 ,但反应的 不相同。
2、根据金属与酸能否反应以及反应的剧烈程度,判断金属的金属活动性(即活泼程度)。
1.将一根用砂纸打磨过的铝丝浸入硫酸铜溶液中。
2.将一根洁净的铜丝浸入硝酸银溶液中。
3.将另一根洁净的铜丝浸入硫酸铝溶液中。
金属与金属化合物的溶液反应
铝丝表面有红色固体出现
1.铝丝浸入CuSO4溶液中
2.铜丝浸入AgNO3溶液中
铜丝表面有银白色固体出现
金属活动性:Al>Cu Cu>Ag
1.许多金属能与金属化合物溶液发生 反应。
2.根据金属与其它金属化合物的溶液能否发生置换反应判断 的强弱。
金属活动性: Al>Cu>Ag
练习:1.波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成。为什么不能用铁制容器来配制波尔多液?
因为铁制容器会与硫酸铜发生置换反应Fe+CuSO4 = FeSO4+Cu
2.在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢。(K Ca Na除外)
3.在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
1.在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
金属活动性由强逐渐减弱
常见金属在溶液中的活动性顺序:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
1.金属R投入稀硫酸中,有气泡产生,镁条插入R的硫酸盐溶液中,有R析出,则R、Mg、Cu的金属活动性顺序为
R>H Mg>R H>Cu 所以Mg>R>Cu
2.下列物质能否发生反应?写出能发生反应的化学方程式。(1)银与稀盐酸(2)锌与硫酸铜溶液(3)铜与硫酸锌溶液(4)铝与硝酸银溶液
(1)(3)不反应(2)Zn+CuSO4 = ZnSO4+Cu(4)Al+3AgNO3 = Al(NO3)3+3Ag
作业: 1.镁、锌、铁三种金属各30g,分别与足量稀盐酸反应,生成氢气的质量各是多少?
解:设镁、锌、铁生成氢气的质量分别为x1、x2、x3。 Mg+2HCl = MgCl2+H2 24 2 30 x1 24/30g = 2/x1 解得:x1= 2.5g 同理,解得:x2≈0.92g,x3≈1.07g答:生成氢气的质量Mg:2.5g,Zn:0.92g,Fe:1.07g
人教版九年级下册课题 2 金属的化学性质示范课ppt课件: 这是一份人教版九年级下册课题 2 金属的化学性质示范课ppt课件,共24页。PPT课件主要包含了a比较硬度,b比较密度,一金属与氧气的反应,灼烧法,加入稀硫酸或稀盐酸,FeCu,Al﹥Cu﹥Ag,课本P11探究,置换反应等内容,欢迎下载使用。
人教版九年级下册课题 2 金属的化学性质备课ppt课件: 这是一份人教版九年级下册课题 2 金属的化学性质备课ppt课件,共20页。PPT课件主要包含了联系生活,看图回答问题,火眼金睛,置换反应,金属活动性,不反应,能反应,难溶物,牛刀小试等内容,欢迎下载使用。
化学课题 2 金属的化学性质教学课件ppt: 这是一份化学课题 2 金属的化学性质教学课件ppt,共17页。PPT课件主要包含了学习目标,回顾已知,A组与盐酸,B组与硫酸,探究活动,镁与硫酸,锌与硫酸,铁与硫酸,铜与硫酸,是否与酸反应等内容,欢迎下载使用。













