

【化学】安徽省滁州市定远县民族中学2018-2019学年高一10月月考试题
展开安徽省滁州市定远县民族中学2018-2019学年高一10月月考试题
本试卷分第I卷(选择题)和第II卷(非选择题)两部分。满分100分,考试时间60分钟。请在答题卷上作答。
第I卷 选择题(共60分)
一、选择题:本卷共20小题,每小题3分,共60分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.设NA为阿伏加德罗常数,下列说法中正确的是( )
A.在常温常压下,11.2 L氮气所含有的原子数目为NA
B.活泼金属从盐酸中置换出1 mol H2,电子转移数为NA
C.500 mL 0.5mol/L Al2(SO4)3溶液中,SO42-的浓度为1.5 mol·L-1
D.1.7 g 氨气所含的电子数目为 10 NA
2.厨房中的化学知识很多,下面是有关厨房中的常见操作或常见现象,其中不属于氧化还原反应的是( )
A. 烧菜用过的铁锅,经放置常出现红棕色斑迹
B.用燃气灶燃烧沼气(主要成分为甲烷:CH4)为炒菜提供热量
C. 豆浆久置变质腐败
D. 用洗洁精清洗有油污的餐具
3.我国科学家在世界上第一次为一种名为“钻酞箐”的分子(直径为1.3×10-9m)恢复了磁性。
“钻酞箐”的分子结构和性质.与人体内的血红素及植物体内的叶绿素非常相似。下列说法不正确的是( )
A. “钻酞箐”分子所形成的分散系具有丁达尔效应
B. “钻酞箐” 分子既能透过滤纸,也能透过半透膜
C. 此项工作可以用来改变分子的某些物理性质
D. 此工作可以广泛应用于光电器件、生物技术等方面
4.下列与实验相关的叙述正确的是( )
A. 配制浓硫酸、浓硝酸的混酸时,应将浓硝酸沿玻璃棒缓慢注入浓硫酸中
B. 用量筒量取5.0mL液体,俯视读数时所得液体体积大于5mL
C. 大试管、烧瓶、锥形瓶均可用于组装气体发生装置
D. 实验室配制一定质量分数、一定物质的量浓度的溶液时均需使用容量瓶
5.NaHSO4在水溶液中能够完全电离出H+、Na+、和SO42- 。下列对于NaHSO4的分类中不正确的是( )
A.NaHSO4是盐 B.NaHSO4是酸式盐
C.NaHSO4是钠盐 D.NaHSO4是酸
6.下列各项操作中,错误的是( )
A. 通过蒸馏酒精水溶液得到95%乙醇,再与生石灰混合,蒸馏可制得无水乙醇
B. 进行分液时,分液漏斗中的下层液体从下口流出,上层液体从上口倒出
C. 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液
D. 为保证分液漏斗内的液体顺利流出,需将分液漏斗颈上的玻璃塞打开
7.下列有关实验现象正确的是( )
A. 用四氯化碳萃取碘水,下层溶液呈紫色
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C. 往氯化铁溶液中加入氢氧化钠溶液可制得氢氧化铁胶体
D. 某溶液滴加紫色石蕊试剂呈红色,该溶液一定含有某种酸
8.若配制3.6mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将使所配制的硫酸溶液浓度偏高的是( )
A. 浓硫酸稀释后立即转移到容量瓶中
B. 将稀释的硫酸溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
C. 将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外
D. 用胶头滴管加水时,仰视观察溶液凹液面与容量瓶刻度线相切
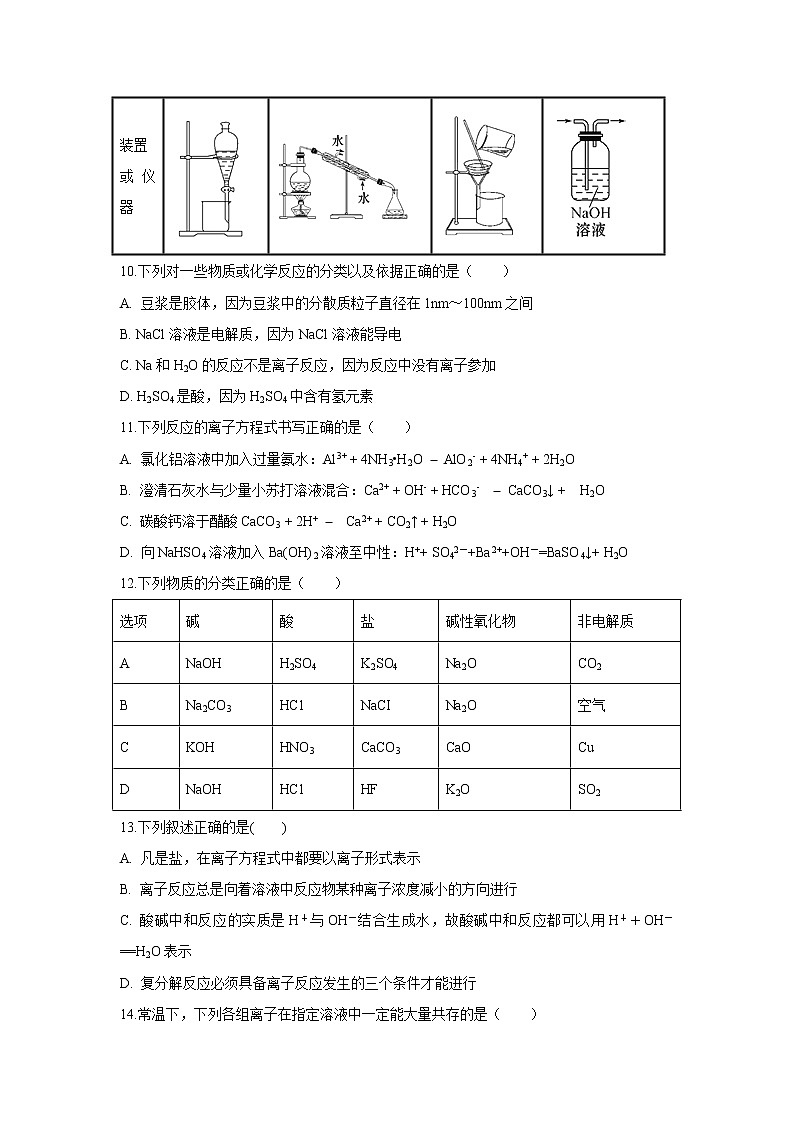
9.完成下列实验所需选择的装置或仪器都正确的是 ( )
选项 | A | B | C | D |
实验 | 分离植物油和氯化钠溶液 | 除去氯化钠晶体中混有的氯化钾晶体 | 分离CCl4中的Br2 | 除去CO2气体中的HCl气体 |
装置 或仪器 |
10.下列对一些物质或化学反应的分类以及依据正确的是( )
A. 豆浆是胶体,因为豆浆中的分散质粒子直径在1nm~100nm之间
B. NaCl溶液是电解质,因为NaCl溶液能导电
C. Na和H2O的反应不是离子反应,因为反应中没有离子参加
D. H2SO4是酸,因为H2SO4中含有氢元素
11.下列反应的离子方程式书写正确的是( )
A. 氯化铝溶液中加入过量氨水:Al3+ + 4NH3•H2O AlO2- + 4NH4+ + 2H2O
B. 澄清石灰水与少量小苏打溶液混合:Ca2+ + OH- + HCO3- CaCO3↓ + H2O
C. 碳酸钙溶于醋酸CaCO3 + 2H+ Ca2+ + CO2↑ + H2O
D. 向NaHSO4溶液加入Ba(OH)2溶液至中性:H++ SO42-+Ba2++OH-=BaSO4↓+ H2O
12.下列物质的分类正确的是( )
选项 | 碱 | 酸 | 盐 | 碱性氧化物 | 非电解质 |
A | NaOH | H2SO4 | K2SO4 | Na2O | CO2 |
B | Na2CO3 | HC1 | NaCI | Na2O | 空气 |
C | KOH | HNO3 | CaCO3 | CaO | Cu |
D | NaOH | HC1 | HF | K2O | SO2 |
13.下列叙述正确的是( )
A. 凡是盐,在离子方程式中都要以离子形式表示
B. 离子反应总是向着溶液中反应物某种离子浓度减小的方向进行
C. 酸碱中和反应的实质是H+与OH-结合生成水,故酸碱中和反应都可以用H++OH-==H2O表示
D. 复分解反应必须具备离子反应发生的三个条件才能进行
14.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 在透明溶液中:Cu2+、K+、SO42—、CO32—
B. 在强碱性溶液中:K+、Na+、CO32—、AlO2—
C. 在盐酸溶液中:K+、Fe2+、SO42—、NO3—
D. 与铝反应产生氢气的溶液中:Na+、K+、HCO3—、Cl—
15.浓硫酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6M
①氧化剂是H3AsO3;②还原性:Cl->As;
③每生成7.5gAs,还原剂失去的电子为0.3 mol;
④M为OH-;⑤ SnCl62-是氧化产物。
关于该反应的说法中正确的组合是( )
A.①③⑤ B.①③ C.①②④⑤ D.①②③④
16.下列反应既属于四种基本反应类型又属于氧化还原反应的是
A. CaO+CO2﹦CaCO3 B. Cl2+H2O﹦HCl+HClO
C. 2 NaOH+CuSO4 =Na2SO4 +Cu (OH)2 D. 2KClO32KCl+3 O2↑
17.根据反应(1)2Fe3++Cu=Cu2++2Fe2+ (2)2Fe2++Cl2=2Fe3++2Cl—(3)HClO + H+ + Cl—=H2O+Cl2,可以判断出各粒子的氧化性由强到弱顺序正确的是( )
A. HClO> Cl2> Fe3+> Cu2+ B. Cl2>HClO>Fe3+>Cu2+
C. Cl2>Fe3+>HClO>Cu2+ D. HClO>Cl2>Cu2+>Fe3+
18.对于反应3Cl2+6NaOH =5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A.Cl2是氧化剂,NaOH是还原剂
B.被氧化的Cl原子和被还原的Cl原子的物质的量之比为5∶1
C.Cl2既是氧化剂又是还原剂
D.每生成1mol的NaClO3转移6mol的电子
19.某学生以铁丝和 Cl2(2Fe+3Cl2 2FeCl3)为原料进行下列三个实验。下列选项正确的是( )
A. 实验①、 ③反应制得的物质均为纯净物
B. 实验①中的反应既是氧化还原反应,又是四种基本反应类型中的反应
C. 实验③化学方程式为 FeCl3+3H2O==Fe(OH)3↓+3HCl
D. 实验①、 ②所涉及的物质均为电解质
20.己知在碱性溶液中可发生如下反应:2R(OH)3 + 3C1O-+ 4OH- = 2RO4n-+3Cl- +5H2O。关于该反应的说法正确的是( )
A. RO4n-中 R 的化合价是+6
B. ClO—是还原剂
C. 由上述离子方程式可知,该反应是由氨水提供的碱性环境
D. 反应过程中生成1mol RO4n-,转移6mol e-。
第II卷 非选择题(共40分)
二、非选择题:本卷共4小题,共40分。
21.(13分)某次实验需用80mL、3mol/L 的稀H2SO4溶液,某同学用98%的浓H2SO4(ρ=1.84g/cm3)进行配制,请回答下列问题:
(1)98%的浓H2SO4(ρ=1.84g/cm3)的物质的量浓度为 , 需要80mL、3mol/L 的稀H2SO4溶液,则需取 mL(保留一位有效数字)的该硫酸,量取浓硫酸所用的量筒的规格是 (从下列中选用)
A.10mL B.25mL C.50mL D.100mL
(2)将下列步骤中的空格内所用仪器补充填写完整
①用量筒量取所需的浓硫酸
②将烧杯中的溶液转移到 mL的容量瓶中
③将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌
④将溶液冷却,恢复至室温
⑤向容量瓶中加入蒸馏水,在距离刻度1~2cm时,改用 加蒸馏水至刻度线
⑥盖好瓶塞,反复上下颠倒,摇匀
⑦洗涤烧杯2~3次,洗涤液也注入容量瓶中.轻轻摇动容量瓶,使溶液混合均匀.
(3)实验中上述步骤的正确顺序为 (填序号)
(4)下列各种情况对所配制溶液浓度有何影响(选填“偏高”、“偏低”或“无影响”)
A.所用的浓硫酸长时间放置在密封不好的容器中 .
B.未经冷却趁热将溶液注入容量瓶中: .
C.所用过的烧杯、玻璃棒未洗涤 .
D.定容时俯视液面读数: .
(5)取用任意体积的所配3mol/L硫酸溶液时,下列物理量中不随所取体积的多少而变化的是_______(填字母)
A.溶液中H2SO4的物质的量
B.溶液的浓度
C.溶液中SO42¯的数目
D.溶液的密度
22. (7分)现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学向1 mol·L-1氯化铁溶液中加入少量的NaOH溶液;
乙同学直接加热饱和FeCl3溶液;
丙同学向25 mL沸水中逐滴加入1 mL~2 mL FeCl3饱和溶液,继续煮沸至溶液呈红褐色,停止加热。试回答下列问题:
(1)其中操作正确的同学是____ ____;若丙同学实验中不停止加热,会看到_______________。
(2)证明有Fe(OH)3胶体生成的实验操作及现象是_____________________。
(3)制备氢氧化铁胶体的离子反应方程式:_____________________
(4)乙同学想将Fe(OH)3胶体提纯,他可以采用的方法是 。
(5)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明______________________。
②向其中加入过量稀硫酸,产生的现象是__________________。
23. (9分)某研究性学习小组为了了解HCl、NaHSO4、NaHCO3在水溶液中的电离情况,进行下列实验:
①分别测定了0.1 mol·L-1的HCl、NaHSO4、NaHCO3 溶液中H+的物质的量浓度,HCl溶液中c(H+)=0.1 mol·L-1,NaHSO4溶液中c(H+)=0.1 mol·L-1,而NaHCO3溶液中H+的物
质的量浓度远远小于0.1 mol·L-1。
②取少量NaHSO4溶液于试管中,滴入BaCl2溶液有不溶于稀硝酸的白色沉淀生成。
③取少量NaHCO3溶液于试管中,滴入几滴BaCl2溶液无明显现象。
请根据实验结果回答下列问题:
(1)分别写出HCl、NaHSO4、NaHCO3在水溶液中的电离方程式:
HCl:__________________________________________________;
NaHSO4:__________________________________________________;
NaHCO3:__________________________________________________。
(2)NaHSO4属于“酸”“碱”“盐”中的________________________。
(3)写出②中反应的化学方程式: _________________________。
(4)若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比1∶1混合,反应的离子方程式为__________________________________________________________________________。
(5)若将NaHSO4逐滴加入Ba(OH)2溶液中至Ba2+恰好完全沉淀,反应的离子方程式为_________________________________________________________________________。
24. (11分)(1)X、Y、Z三种物质存在如图所示转化。回答下列问题。
若X为黑色固体单质,A为O2,写出Z→Y的化学方程式_________________。
②若X为NaOH溶液,则写出Y→Z的化学方程式_______________________。
(2)已知常温下在溶液中可发生如下两反应:
Ce4++Fe2+=Fe3++Ce3+;Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是 。
(3)Mn2+、Bi3+、BiO3-、MnO4-、H+、H2O组成的一个氧化还原反应体系中,发生BiO3-→Bi3+的反应过程。
①该反应中,被氧化的元素是_____________,氧化剂是_______________。
将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式。
________+ ______+ ________ ______+ ________+ H2O
反应中若产生0.2mol的还原产物,则有_______mol电子转移。
【参考答案】
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
C | D | B | C | D | C | A | A | A | A |
11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
B | A | B | B | A | D | A | C | B | A |
21.(1)18.4mol/L;16.3ml;B
(2)100;胶头滴管
(3)①③④②⑦⑤⑥
(4)偏低;偏高;偏低;偏高
(5)B,D
22.(1)丙;有红褐色的沉淀生成
(2)用一束激光照射,若有一条光亮的通路,则证明有Fe(OH)3胶体生成;
(3)Fe3++3H2O(沸水)= Δ=Fe(OH)3(胶体)+3H+;
(4)渗析;
(5)① 表明Fe(OH)3胶体粒子带正电荷;②先有红褐色沉淀生成,然后沉淀溶解为黄色溶液;
23. (1)HCl===H++Cl- NaHSO4===Na++H++SO NaHCO3===Na++HCO
(2)盐
(3)NaHSO4+BaCl2===NaCl+BaSO4↓+HCl
(4)H++SO+Ba2++OH-===H2O+BaSO4↓
(5)H++SO+Ba2++OH-===H2O+BaSO4↓
24.(1)①CO2+C2CO;②CO2+Na2CO3+H2O=2NaHCO3;
(2)Ce4+>Fe3+>Sn4+;
(3)①Mn,BiO3-;②BiO3-+Mn2++H+Bi3++MnO4-+H2O;③0.4。








