

所属成套资源:中考化学一轮复习专题巩固练习 (含答案解析)
中考化学一轮复习专题巩固练习 有关金属性质的计算问题汇总(九)(含答案解析)
展开 这是一份中考化学一轮复习专题巩固练习 有关金属性质的计算问题汇总(九)(含答案解析),共22页。试卷主要包含了下列说法正确的是等内容,欢迎下载使用。
A.足量金属铁放入AgNO3溶液中,溶液变为黄色
B.金属R和稀盐酸能反应,生成物是RCl2和H2
C.将金属铁放入CuSO4溶液中,一段时间后溶液质量变小
D.将金属R放入Cu(NO3)2和AgNO3混合溶液中充分反应后过滤,若滤液为蓝色,则滤渣中一定有Cu和Ag
2.下列说法正确的是
A.原子中一定含有质子、中子和电子三种微粒
B.某物质能与碱反应生成盐和水,则该物质一定是酸
C.金属与盐溶液发生置换反应后,溶液的质量一定增加
D.同一温度下,某固体物质的饱和溶液一定比其不饱和溶液的浓度大
3.下列说法正确的是
A.未说明药品用量时,液体一般取1﹣2mL左右,固体只需盖满试管底部
B.称取0.75克食盐用于配制溶液,应该把食盐放在托盘天平的右盘
C.酒精灯用完后,先用嘴吹灭,再盖上灯帽
D.进入久未开启的菜窖前,不一定要进行灯火实验
4.将2.4 g Mg、5.6 g Fe和3.2 g Cu的混合物加入一定量的稀硫酸中,充分反应后剩余固体6 g,则生成氢气的质量是
A.0.3 gB.0.4 gC.0.5 gD.0.6 g
5.铝与足量稀硫酸反应产生硫酸铝和氢气,当反应产生2g氢气时消耗铝的质量为
A.9 gB.12gC.18gD.27g
6.某兴趣小组在研究Fe﹣Al合金、Fe﹣Cu合金、Zn﹣Cu合金、Zn﹣Fe合金时,发现其中一种合金2.5g与足量稀盐酸充分反应产生了0.2g气体,该合金可能是
A.Fe﹣Al合金B.Fe﹣Cu合金
C.Zn﹣Cu合金D.Zn﹣Fe合金
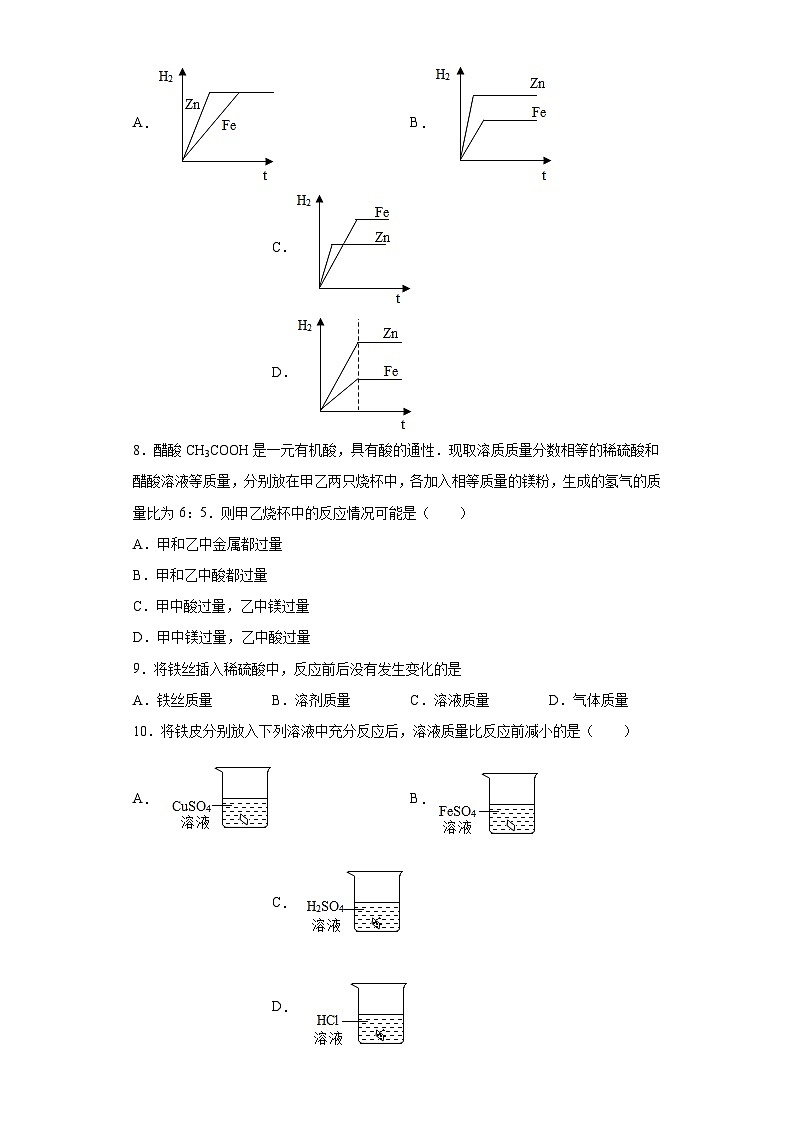
7.等质量的锌、铁两种金属分别与足量的稀硫酸反应,下列图像能正确表示生成氢气质量与反应时间之间关系的是( )
A.B.C.D.
8.醋酸CH3COOH是一元有机酸,具有酸的通性.现取溶质质量分数相等的稀硫酸和醋酸溶液等质量,分别放在甲乙两只烧杯中,各加入相等质量的镁粉,生成的氢气的质量比为6:5.则甲乙烧杯中的反应情况可能是( )
A.甲和乙中金属都过量
B.甲和乙中酸都过量
C.甲中酸过量,乙中镁过量
D.甲中镁过量,乙中酸过量
9.将铁丝插入稀硫酸中,反应前后没有发生变化的是
A.铁丝质量B.溶剂质量C.溶液质量D.气体质量
10.将铁皮分别放入下列溶液中充分反应后,溶液质量比反应前减小的是( )
A.B.C.D.
11.取5.5g氧化铜、氧化铝、氧化铁的混合物,加入9.8%稀硫酸100g恰好完全反应。则该混合物中氧元素的质量为
A.0.8g
B.1.6g
C.2.4g
D.3.2g
12.下列四个图像分别与选项中的操作相对应,其中合理的是
A.加热KClO3和MnO2的混合物制取氧气
B.等质量的镁条和等质量的氧气反应
C.向质量相等的铝粉和镁粉中分别加入浓度相等且足量的稀盐酸
D.向一定质量的CuSO4和H2SO4的混合液中逐滴滴入NaOH溶液
13.化学的研究对象是物质,氧气、水、金属和碳单质在我们的生产生活中非常重要,下列说法中正确的是
A.AB.BC.CD.D
14.将13g金属混合物粉末投入到足量的稀盐酸中充分反应得到1 .0gH2,则此混合物组成可能为
A.Fe和Zn
B.Fe和Cu
C.Mg和Al
D.Mg和Zn
15.某镁的样品中含有铝、锌、铁、铜中一种或几种杂质。现取2.4g样品,加入100g稀盐酸中,固体完全溶解,所得溶液的质量为102.2g,下列选项中杂质组成正确的是
A.AlB.Al、ZnC.Zn、FeD.Zn、Cu
16.6g镁和铁的混合粉末与100g 19.6%的稀硫酸恰好完全反应,将所得溶液蒸干,得到硫酸盐固体的质量为
A.25.2gB.24.6gC.104.6gD.无法判断
17.向一定量的Cu(NO3)2的溶液中加入一定量的锌粉,充分反应后过滤,得到滤液M和滤渣N;向滤渣N中加入稀盐酸,有无色气泡生成。下列分析判断的说法中,正确的是
A.滤液M中一定存在Cu2+
B.滤渣N的成分为Zn
C.滤液M的质量大于原溶液的质量
D.根据质量守恒,滤渣N的质量一定等于加入锌粉的质量
18.向一定质量的Cu(NO3)2和AgNO3的混合溶液中逐渐加入锌粉。反应过程中溶质Cu(NO3)2的质量随加入锌粉质量的变化关系如图所示。下列说法错误的是
A.a点时,溶液的总质量与反应前相比减小
B.b点时,溶液为Zn(NO3)2和Cu(NO3)2的混合溶液
C.c点时,溶液呈无色
D.d点时,过滤所得滤渣为Cu和Ag的混合物
19.下列说法中正确的个数是
①某物质经检测只含一种元素,该物质一定是单质
②一氧化碳和二氧化碳元素组成相同,化学性质相似
③含有一种其他金属的镁的合金2.4g放入足量的盐酸中,得到0.22g氢气,该镁合金中混有的杂质不可能是锌
④硝酸钾、氯化钠和硫酸铵在pH=11的溶液中能大量共存
⑥只用一种试剂即可鉴别NaCl、NH4NO3、(NH4)2SO4、Na2SO4四种无色溶液
A.2个
B.3个
C.4个
D.5个
20.下列图像能正确反映对应变化关系的是
A.AB.BC.CD.D
21.如图,一木块漂浮于X中,向X中缓缓加入(或通入)少量物质Y后最终木块上浮,则X与Y可能是(溶液的体积变化忽略不计)
A.②④B.①③C.①②③D.②③④
22.向CuSO4溶液中加入一定质量的Al粉,充分反应后过滤,得蓝色滤液,并将滤渣晾干(不考虑操作中的损失)。下列说法正确的是
A.滤液中只含有Al2(SO4)3
B.滤渣的质量等于Al粉的质量
C.向滤渣中滴加稀盐酸,无气泡产生
D.发生反应的化学方程式为
23.如图所示的四个图像,分别对应四种过程,其中错误的是( )
A.图①:红磷在盛有空气的密闭容器中燃烧
B.图②:电解水实验过程
C.图③:向一定质量二氧化锰中加入过氧化氢
D.图④:分别向等质量Mg和Zn中加入等质量、等浓度且足量的稀盐酸
24.某化工厂的废液中主要含有硝酸银、硝酸铜。取一定量的该废液样品。加入镁粉和铜粉,充分反应后过滤,得到滤液和滤渣。下列说法正确的个数有( )
①若向滤渣中加稀盐酸,有气泡产生,则滤液中一定没有硝酸铜、硝酸银
②若滤渣中有铜粉,则滤液中一定含有硝酸镁,可能含有硝酸铜
③若滤渣中没有铜粉,则滤液中一定含有硝酸镁、硝酸铜、硝酸银
④反应后得到滤渣的质量一定大于反应前所加固体的质量
A.1 个B.2 个C.3 个D.4 个
25.将锌、铁、镁、铝的混合粉末3.6 g投入到一定质量的稀硫酸中,恰好完全反应后,得到200 g含水88.6%的溶液,则得到氢气的质量是
A.0.1 gB.0.2 gC.0.3 gD.0.4 g
26.下列说法不正确的是
A.目前计入空气污染指数的有:二氧化硫、一氧化碳、二氧化氮、臭氧、PM2.5 等
B.生理盐水的浓度为 0.9%,指的是 100g 水中溶有 0.9g 氯化钠
C.30 g 有机物M在氧气中充分燃烧,生成 44g 二氧化碳和 18g 水,则 M 中一定含碳、氢、氧元素
D.某镁合金含有铁、铝、铜中的一种或几种,取该合金 2.4g,加入足量稀盐酸,产生 0.2 gH2,则该合金的金属组合可能有 3 种
27.向盛有20g49%稀硫酸的烧杯中加入11.2g的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列说法错误的是( )
A.m=25.4
B.a→b点,溶液的pH先增大后不变
C.c点时,溶液中有两种溶质
D.d点固体,加入盐酸一定没有气泡产生
28.向一定量的硝酸铜、硝酸亚铁的混合溶液中加入 2.4g 镁粉,充分反应后过滤、洗涤、 干燥,称得固体 6g。则下列分析正确的是( )
A.滤液中一定不含有硝酸铜B.滤液中一定含有硝酸亚铁
C.滤出的固体中可能有铜无铁D.滤出的固体中可能只有铜和镁
29.一定质量的铜和镁组成的混合物与足量稀盐酸反应,过滤后,将滤渣在空气中加热,充分反应所得产物的质量恰好等于原混合物的质量。那么原混合物中镁的质量分数是
A.80%B.64%C.50%D.20%
30.将镁粉和铝粉的混合物7.2g与足量的氧气充分反应,得到的氧化物质量可能为
A.10.6gB.12.0gC.13.0gD.13.6g
A.氧气
B.水
①氧气的化学性质比较活泼,属于可燃物②测定空气中氧气含量的实验中红磷需过量
①净化水的常用方法包括沉淀、过滤、吸附等②电解水时,在正极得到的气体在点燃前必验纯
C.碳单质
D.金属
①原子的排列方式不同,决定了碳单质的性质不同②焦炭、木炭是冶金和生活的常用燃料
①等质量的酸分别与足量的铝、锌反应,生成氢气的质量相等 ②一氧化碳还原氧化铁的实验中,实验结束时,
先停止通一氧化碳,再停止加热
A
B
C
D
加热一定量的高锰酸钾固体
两份完全相同的过氧化氢溶液分解
向一定量铁粉中加入硫酸铜溶液
加热一定量的饱和石灰水
序号
X
Y
①
水
食盐
②
氢氧化钙溶液
二氧化碳
③
稀硫酸
镁粉
④
硫酸铜溶液
氢氧化钠溶液
参考答案:
1.C
【详解】A、铁与硝酸银溶液反应生成硝酸亚铁和银,足量金属铁放入AgNO3溶液中,溶液变为浅绿色,不符合题意;
B、金属R和Fe、H活动性强弱关系为R>Fe>H,金属R和稀盐酸能反应,由题意,无法确定R的化合价,生成物不一定是RCl2,不符合题意;
C、铁与硫酸铜反应生成硫酸亚铁和铜,反应的化学反应方程式为:,每56份质量的铁可置换出64份质量的铜,溶液的质量会减少,符合题意;
D、将金属R放入Cu(NO3)2和AgNO3混合溶液中充分反应后过滤,若滤液为蓝色,则滤液中含有硝酸铜,硝酸铜可能没有参加反应,也可能是部分参加反应,则滤渣中一定有Ag,可能含有Cu,不符合题意;
【点睛】本题难度不大,考查了金属活动顺序的应用,掌握金属活动顺序并能灵活运用是正确解答此类题型的关键所在。
2.D
【详解】A、原子中不一定含有质子、中子和电子三种微粒,比如氢原子不含有中子,故A错误;
B、某物质能与碱反应生成盐和水,则该物质不一定是酸,例如非金属氧化物与碱反应生成盐和水,故B错误;
C、金属与盐反应,溶液质量的变化需要考虑进入溶液金属的原子质量与置换出来的金属的相对原子质量的大小比较,进入溶液金属的原子质量大于置换出来的金属的相对原子质量,溶液质量增加,进入溶液金属的对原子质量小于置换出来的金属的相对原子质量,溶液质量减小,故C错误;
D、饱和溶液比不饱和溶液浓的条件:同一温度、同一溶质饱和溶液比不饱和溶液浓,故D正确。故选D。
3.A
【详解】A、未说明药品用量时,液体一般取1﹣2mL左右,固体只需盖满试管底部,正确;
B、天平的精确度是0.1克,不能称取0.75克食盐,称量时应该把食盐放在托盘天平的左盘,错误;
C、酒精灯用完后,不能用嘴吹灭,应该用灯帽直接盖灭,错误;
D、二氧化碳不能供给呼吸,含量过多会使人窒息死亡,久未开启的菜窖中二氧化碳的含量可能过多,故进入前需要进行灯火实验,错误。
故选A。
4.A
【详解】金属活动性顺序为镁大于铁大于氢大于铜;混合物加入一定量稀硫酸中,铜不参与反应,故剩余固体6.0g中含有3.2g铜和6.0g-3.2g=2.8g铁;反应镁、铁质量分别为2.4g、5.6g-2.8g=2.8g;
故生成氢气质量为0.2g+0.2g=0.3g。
故选A。
5.C
【分析】通过化学方程式所体现的各物质的质量关系,用已知物质的质量去求未知物质的质量;
【详解】解:设消耗铝质量为x
x=18g
答案:C。
6.A
【分析】本题考查金属和酸反应。
【详解】A、铁、铝与稀盐酸反应的化学方程式及其质量关系:
由以上质量关系可知,生成0.2g氢气,消耗铁、铝质量分别是5.6g、1.8g,因此2.5gFe﹣Al合金与稀盐酸反应可能生成0.2g氢气,该选项符合题意;
B、由A中分析可知,生成0.2g氢气消耗5.6g铁,铜不能和稀盐酸反应,因此2.5gFe﹣Cu合金与稀盐酸反应生成氢气质量小于0.2g,该选项不符合题意;
C、锌和稀盐酸反应的化学方程式及其质量关系:
生成0.2g氢气消耗锌质量是6.5g,铜不能和稀盐酸反应,因此2.5gZn﹣Cu合金与稀盐酸反应生成氢气质量小于0.2g,该选项不符合题意;
D、由A、C分析可知,2.5gZn﹣Fe合金与稀盐酸反应生成氢气质量小于0.2g,该选项不符合题意。
故选:A。
【点睛】金属活动性强于氢元素的,可以置换氢气。
7.C
【详解】
由于锌比铁活泼,反应速率比铁快,由上述化学方程式可知,同质量的锌和铁与足量的稀硫酸反应,铁生成的氢气多。
故选:C
8.C
【详解】A、甲和乙中金属都过量,则两种质量相同的酸完全反应,因此设酸的质量都为m,生成的氢气分别为x、y,则:
显然二者的质量比不是6:5,说法错误;故不符合题意;
B、甲和乙中酸都过量,说明镁完全反应,镁的质量相等,产生的氢气应该相等,说法错误;故不符合题意;
C、镁的质量相等,产生的氢气应该相等,而甲中酸过量,则镁完全反应,产生的氢气就多;乙中镁过量,则镁没有完全反应,产生的氢气就少,因此可以符合6:5,说法正确;故符合题意;
D、镁的质量相等,产生的氢气应该相等,而甲中镁过量,则镁没有完全反应,产生的氢气就少;乙中酸过量,则镁完全反应,产生的氢气就多,因此不符合6:5,说法错误;故不符合题意;
故选C
【点睛】本题考查了金属与酸反应情况的分析,解题的关键是能够依据化学方程式进行相关量的分析计算。
9.B
【详解】在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢,铁位于氢前面,会与稀硫酸反应生成硫酸亚铁和氢气。
A、铁丝是反应物,质量会减少,A错误;
B、溶剂是水,不参与反应,质量不会变,B正确;
C、溶液会与稀硫酸溶液变成硫酸亚铁,溶液质量发生变化,C错误;
D、反应会生成气体,质量变化,D错误。
故选B。
10.A
【详解】A、根据化学方程式Fe+CuSO4=FeSO4+Cu,假设56克铁完全反应,则生成64克铜,溶液质量减少8克,故正确;
B、铁不会与硫酸亚铁溶液反应没有质量不变,故错误;
C、根据化学方程式Fe+H2SO4=FeSO4+H2↑,假设56克铁完全反应,则生成2克氢气,溶液质量增加54克,故错误;
D、根据化学方程式Fe+2HCl=FeCl2+H2↑,假设56克铁完全反应,则生成2克氢气,溶液质量增加54克,故错误。
故选A。
11.B
【详解】该反应的实质是,稀硫酸中的氢元素恰好与混合物中的氧元素完全反应生成水。因此,根据题目给定的数值可得:
x=1.6g
经过计算可知,x的值为1.6g。
故选:B。
12.C
【详解】A、氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,随着反应进行,固体质量减小,二氧化锰质量分数增大,该选项图象不合理;
B、反应的化学方程式为2Mg+O22MgO,参加反应的镁与氧气的质量比为(24×2):32=3:2;等质量的镁条和等质量的氧气反应,氧气有剩余,镁全部参加反应,故选项图象错误;
C、向等质量的铝粉和镁粉中分别加入足量的等浓度稀盐酸,若消耗稀盐酸相同,则生成氢气质量相同,故开始两斜线重合,后因稀盐酸过量,镁消耗的稀盐酸多,生成的氢气多,拐点高些,故选项图象合理;
D、向一定质量的硫酸铜和稀硫酸的混合溶液中不断加NaOH溶液时,氢氧化钠先和稀硫酸反应生成氯化钠和水,后和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,该选项图象不合理。
故选C。
13.C
【详解】A、氧气的化学性质比较活泼,能与多种物质发生燃烧反应,这是因为氧气具有助燃性;测定空气中氧气含量的实验中需要过量的红磷使装置内的氧气完全耗尽,故选项错误;
B、净化水的常用方法包括沉淀、过滤、吸附等;电解水时,在正极得到的气体是氧气,负极得到的气体是氢气,而氢气在点燃前必验纯,故选项错误;
C、物质的结构决定了物质的性质,故碳原子的排列方式不同,决定了碳单质的性质不同;而焦炭、木炭是冶金和生活的常用燃料,故选项正确;
D、等质量的酸分别与足量的铝、锌反应,因为酸的量相同,故生成氢气的质量相等;一氧化碳还原氧化铁的实验中,实验结束时,先停止加热,再停止通一氧化碳,防止生成的铁又被氧化,故选项错误;
故选择C;
14.D
【详解】当金属混合物设定为+2价金属时,假设都能反应。设混合物为M,相对原子质量为x。则
x=26;
若两种金属都反应,且本身都是+2价金属,则必须只能有一个的相对原子质量小于26,(这样排除了A)在给定的金属中只有镁的小于26,所以D选项正确。而C中由于铝为+3价金属,相对原子质量为27,当折合为+2价金属时,铝可以理解为相对原子质量为18,两个都小于26,所以C不对。
若有一种金属不反应,则能够反应的金属的相对原子质量必须小于26,所以B错误。
故选:D。
15.B
【详解】现取2.4g样品,加入100g稀盐酸中,固体完全溶解,所得溶液的质量为102.2g,则生成的氢气的质量为。
镁、铝、锌、铁均和稀盐酸反应的关系式为:
、、、
A、2.4g镁反应恰好生成0.2g氢气,1.8g铝反应生成0.2g氢气,2.4g样品与稀盐酸反应生成氢气的质量大于0.2g,故A不正确;
B、1.8g铝反应生成0.2g氢气,6.5g锌反应生成0.2g氢气,样品中铝和锌的比例合适,可以生成0.2g氢气,故B正确;
C、6.5g锌反应生成0.2g氢气,5.6g铁反应生成0.2g氢气,2.4g样品与稀盐酸反应生成氢气的质量小于0.2g,故C不正确;
D、6.5g锌反应生成0.2g氢气,铜和稀盐酸不反应,2.4g样品与稀盐酸反应生成氢气的质量小于0.2g,故D不正确。
故选B。
16.A
【详解】100g、19.6%的稀硫酸中硫酸根离子质量为:100g×19.6%×=19.2g,镁和铁的混合粉末6g完全和硫酸根离子结合生成硫酸镁、硫酸亚铁,因此得到硫酸盐固体的质量为:6g+19.2g=25.2g,
故选A。
17.C
【解析】由于锌的活动性大于铜,将一定量的锌粉投入Cu(NO3)2溶液中,锌能将铜置换出来,反应方程式:Zn+Cu(NO3)2=Zn(NO3)2+Cu。充分反应后过滤,得到滤液和滤渣。向滤渣中加入稀盐酸,有气泡冒出,说明了锌有剩余,溶液中的铜完全被置换出来了。则滤渣中一定含有锌和铜,滤液中除水外还一定含有硝酸锌,一定没有硝酸酮。
【详解】A、根据分析,铜完全被置换出来,滤液中一定不存在Cu2+,故选项错误;
B、滤渣N的成分为剩余的锌和置换出的铜,故选项错误;
C、锌能将铜置换出来,根据反应方程式:Zn+Cu(NO3)2=Zn(NO3)2+Cu可知,每65份质量的锌能生成64份质量的铜,整个过程中溶液质量增加,反应后的溶液滤液M的质量大于原溶液的质量,故选项正确;
D、锌能将铜置换出来,根据反应方程式:Zn+Cu(NO3)2=Zn(NO3)2+Cu可知,每65份质量的锌能生成64份质量的铜,滤液质量增大,滤渣质量减小,N的质量一定小于加入锌粉的质量,故选项错误。
故选C。
18.C
【分析】向一定质量的Cu(NO3)2和AgNO3的混合溶液中逐渐加入锌粉,由金属活动性顺序可知,Zn>Cu>Ag,故锌粉加入后先与AgNO3溶液反应,再与Cu(NO3)2溶液反应,据此回答问题。
【详解】A、a点表示的是锌粉与AgNO3溶液正在反应,由Zn的相对原子质量为65,Ag的相对原子质量为108可知,65份的Zn能置换出108份的Ag,故溶液质量在减小,选项正确,不符合题意;
B、b点之后随着锌粉的加入,Cu(NO3)2溶液质量开始减小,说明b点时Zn与Cu(NO3)2发生反应,且b点时AgNO3已被反应完,故溶液中不再含有AgNO3,则此时,溶液为Zn与AgNO3反应生成的Zn(NO3)2和还没有开始参与反应的Cu(NO3)2的混合溶液,选项正确,不符合题意;
C、c点表示溶液中Cu(NO3)2还没有反应完,则此时溶液中仍然存在铜离子,溶液的颜色仍为蓝色,选项错误,符合题意;
D、d点时Cu(NO3)2质量为0,说明此时Cu(NO3)2全部反应完,且此时Zn和Cu(NO3)2恰好完全反应,则此时Zn的质量也为0,故过滤得到的滤渣为Zn与AgNO3和Zn与Cu(NO3)2反应得到的Ag和Cu,选项正确,不符合题意。
故选C。
19.A
【详解】①某物质经检测只含一种元素,该物质不一定是单质,也有可能是混合物,错误;
②一氧化碳和二氧化碳元素组成相同,但是他们分子不同,化学性质不同,错误;
③根据化学方程式Zn+2HCl=ZnCl2+H2↑,65gZn得到2g氢气。假设是2.4克纯净的锌与足量的稀盐酸反应,生成氢气小于0.2克,故不可能是锌,正确;
④铵根离子与氢氧根离子反应生成氨气和水,故不能大量共存;因此硫酸铵在pH=11的溶液中不能大量共存,错误;
⑥氢氧化钡与氯化钠不能反应,与硝酸铵反应产生氨气,与硫酸铵反应生硫酸钡沉淀和氨气,与硫酸钠反应生成硫酸钡沉淀,所以可以用氢氧化钡鉴别。加入后无明显现象是NaCl;加入后有刺激性气味气体生成是NH4NO3;加入后有白色沉淀和刺激性气味气体生成的是(NH4)2SO4 ;加入后有白色沉淀生成的是Na2SO4。正确。
有2条正确。故选A。
20.B
【详解】A、高锰酸钾加热生成锰酸钾、二氧化锰、氧气,剩余固体中含有氧元素,所以固体中氧元素的质量分数逐渐减少,最后是一定值,不能为零,故A错误;
B、催化剂只是改变反应速率,不影响生成物的质量,催化剂能加快过氧化氢的分解,故B正确;
C、向一定量铁粉中加入硫酸铜溶液,,根据化学方程式,生成金属的质量变大,故C错误;
D、加热一定量的饱和石灰水,溶解度变小,溶液质量变小,故D错误。
故选B。
21.B
【详解】根据物理方面的知识可知,木块的重力等于它受到的液体的浮力,浮力等于木块排开液体的重力,最终木块上浮说明溶液的密度增大。
①食盐溶于水后密度增大,符合题意;
②氢氧化钙能和二氧化碳反应生成碳酸钙沉淀和水,由原来含有溶质的溶液变成纯水,密度变小,不符合题意;
③镁和稀硫酸反应能生成硫酸镁和氢气,根据可知溶液的质量增大,密度增大,符合题意;
④硫酸铜和铁反应能生成硫酸亚铁和铜,根据可知溶液的质量减小,密度变小,不符合题意。
故选:B。
22.C
【详解】A、铝和硫酸铜反应生成硫酸铝和铜,充分反应后过滤,得蓝色滤液,说明滤液中含有硫酸铜,则滤液中含有硫酸铜和硫酸铝,故A不正确;
B、铝和硫酸铜反应生成硫酸铝和铜,反应的关系式为,每54份质量的铝反应生成192份质量的铜,反应后固体的质量变大了,则滤渣的质量不等于Al粉的质量,故B不正确;
C、充分反应后过滤,得蓝色滤液,说明硫酸铜有剩余,铝粉反应完全,固体中铜不与稀盐酸反应,则向滤渣中滴加稀盐酸,无气泡产生,故C正确;
D、铝和硫酸铜生成铜和硫酸铝,反应的化学方程式为,故D不正确。
故选C。
23.D
【详解】A、红磷燃烧放热,导致压强增大,完全反应后氧气消耗,温度降低,压强减小,并且小于原来的压强,该选项对应关系正确;
B、电解水生成氢气和氧气,氢气和氧气体积比是2:1,该选项对应关系正确;
C、过氧化氢在二氧化锰催化作用下分解生成水和氧气,随着反应进行,氧气质量增大,该选项对应关系正确;
D、稀盐酸和镁反应生成氯化镁和氢气,和锌反应生成氯化锌和氢气,等质量Mg和Zn中加入等质量、等浓度且足量的稀盐酸时,根据、,最终镁和稀盐酸反应生成的氢气多,该选项对应关系不正确。
故选:D。
24.C
【分析】由于金属活动性镁>铜>银,硝酸银、硝酸铜的废液样品,加入镁粉和铜粉后,镁先和硝酸银反应,生成硝酸镁和银,滤渣中一定有银,滤液中一定有硝酸镁。
【详解】①若向滤渣中加稀盐酸,有气泡产生,说明滤渣中一定有镁,镁和硝酸铜硝酸银反应,则滤液中一定没有硝酸铜、硝酸银,选项正确。
②若滤渣中有铜粉,滤液中一定没有硝酸银,可能含有硝酸铜,由分析可知滤液中一定有硝酸镁,故选项正确。
③若滤渣中没有铜粉,说明镁和铜与硝酸银完全反应,滤液中一定含有硝酸镁、硝酸铜,硝酸银可能有剩余也可能没有剩余,选项错误。
④硝酸银、硝酸铜的废液样品,加入镁粉和铜粉后可能发生的反应,
由反应可知,反应后得到滤渣的质量一定大于反应前所加固体的质量,选项正确。
故正确个数3个选C。
25.D
【详解】由质量守恒定律和题中信息知,反应后溶质的质量为200g×(1-88.6%)=22.8g,硫酸根质量为22.8g-3.6g=19.2g,设反应生成的氢气的质量为x,根据质量守恒定律可知:
故选D。
26.B
【详解】A、目前计入空气污染指数的有:二氧化硫、一氧化碳、二氧化氮、臭氧、PM2.5等,故A正确;
B、生理盐水的浓度为 0.9%,指的是 100g 生理盐水中溶有 0.9g 氯化钠,故B错误;
C、44g 二氧化碳中碳元素的质量为:=12g,18g 水中氢元素的质量为:=2g,根据质量守恒定律,有机物M中一定含有碳、氢元素,且碳、氢元素的质量分别为12g、2g,质量之和为12g+2g=14g6g,所以2.4g 镁粉没有全部参与硝酸铜反应,还有部分镁粉与硝酸亚铁反应,也就是说溶液中的硝酸铜已全部参与反应,滤溶液中一定不含硝酸铜,可能含有硝酸亚铁,一定含有硝酸镁,生成的固体中一定含有铜和铁,可能还有镁。
【详解】A、溶液中的硝酸铜已全部参与反应,滤液中一定不含有硝酸铜,符合题意;
B、滤液中可能含有硝酸亚铁,不符合题意;
C、滤出的固体中一定有铜和铁,不符合题意;
D、滤出的固体中一定有铜和铁,可能有镁,不符合题意。故选A。
29.D
【详解】由于固体质量前后不变,所以镁的质量和与铜反应的氧气的质量相等。
设镁的质量为x,即反应的氧气的质量为x,设铜的质量为y
原混合物中镁的质量分数为×100%=20%
故选:D。
【点睛】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
30.C
【分析】可以采用极值法,假设7.2g全部为镁粉或铝粉,则与足量的氧气充分反应,得到的氧化物质量应处于计算出的两个值之间。
【详解】设7.2g镁与足量氧气反应产生氧化镁的质量为x,7.2g铝与足量氧气反应产生氧化铝的质量为y
由此可见,若全部为铝,则得到的氧化物质量13.6g,如果全为镁,得到的氧化物质量12g,由于是混合物,因此混合物得到的氧化物质量应介于12g与13.6g之间。
故选C。
相关试卷
这是一份中考化学一轮复习专题巩固练习 有关金属性质的计算问题汇总(九)(含答案解析),共22页。试卷主要包含了下列说法正确的是等内容,欢迎下载使用。
这是一份中考化学一轮复习专题巩固练习 有关金属性质的计算问题汇总(一)(含答案解析),共17页。试卷主要包含了下列说法正确的是等内容,欢迎下载使用。
这是一份中考化学一轮复习专题巩固练习 有关金属性质的计算问题汇总(十)(含答案解析),共22页。试卷主要包含了下列说法正确的是,小明用托盘天平称量6.5g白糖等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 






.png)




