




人教版 (2019)必修 第二册第一节 硫及其化合物集体备课ppt课件
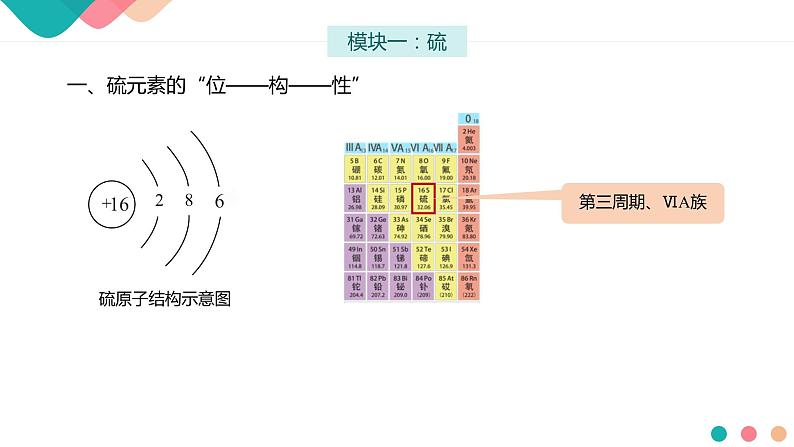
展开一、硫元素的“位——构——性”
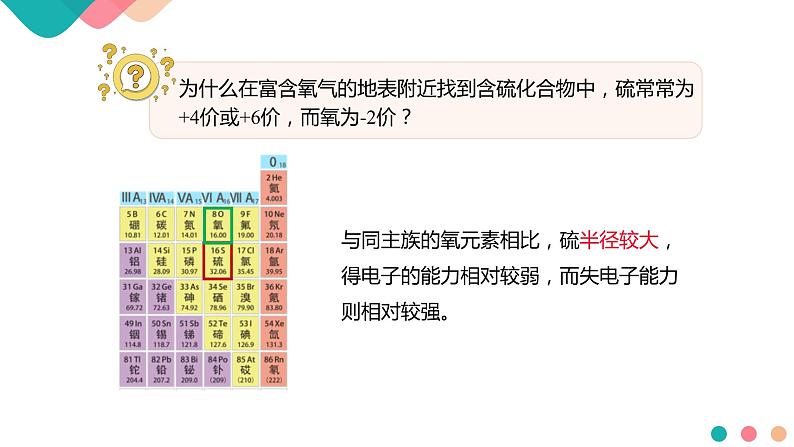
与同主族的氧元素相比,硫半径较大,得电子的能力相对较弱,而失电子能力则相对较强。
二、硫在自然界中的存在
存在于火山口、地壳岩层
主要为硫化物和硫酸盐,火山喷出物中含有硫的氢化物和氧化物等
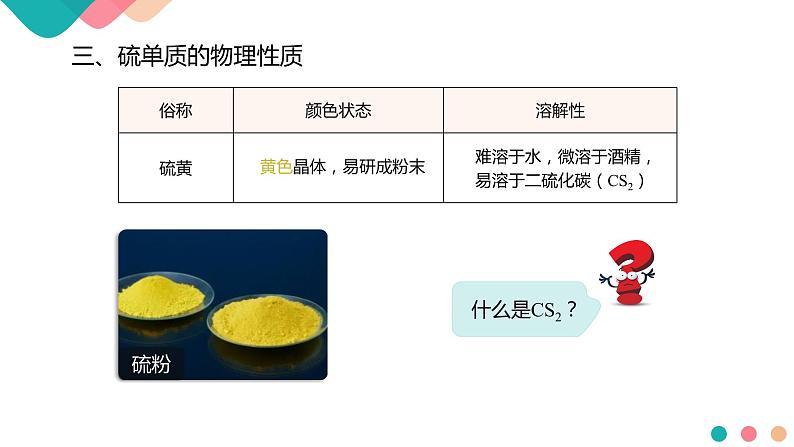
难溶于水,微溶于酒精,易溶于二硫化碳(CS2)
硫元素化合价主要有:-2、0、+4、+6
用二硫化碳溶剂或者用热的 NaOH 溶液
汞蒸气有毒,一旦打碎温度计或实验室中汞泄露,可以撒上硫粉处理
S + Hg == HgS
1. 下列有关硫的性质及应用的描述,错误的是( )A. 从硫的化合价角度分析,单质硫既具有氧化性又具有还原性B. 单质硫与变价金属反应时一般生成低价态金属硫化物C. 试管内壁沾有硫粉,可用CS2或热的NaOH溶液洗涤D. 单质硫燃烧时,氧气少量可生成SO2,氧气足量时可生成SO3
2. 晋代炼丹家、医药学家葛洪所著《抱朴子》一书中记载“丹砂烧之成水银,积变又还成丹砂”,这句话中的丹砂指的是HgS,下列有关说法正确的是( )A. 这个过程只涉及物理变化B. “积变又还成丹砂”过程中发生反应:HgS Hg+SC. 实验室中不慎洒落的水银不能用硫黄处理D. “丹砂烧之成水银”过程中还可能产生SO2
一、SO2 的物理性质
二、SO2 的化学性质
溶液呈酸性 PH<7、溶液呈红色
SO2溶于水后形成的水溶液显酸性,体现了酸性氧化物的性质。
亚硫酸是一种弱酸,不稳定,易分解:
通过下列反应说明二氧化硫具有哪些性质?
SO2 + 2H2S = 3S+ 2H2O
二氧化硫既具有氧化性有具有还原性
核心素养之“证据推理与模型认知”—— 检验SO2和CO2混合气体中存在CO2的流程模型
二氧化硫具有漂白性,但漂白生成的 无色物质不稳定,加热又能恢复原来 的颜色。
品红褪色,加热后又恢复原来的红色
HClO、Na2O2、H2O2
利用SO2的漂白性/还原性,可通入品红酸性高锰酸钾/溴水等溶液。
不能,因为弱酸不能制强酸。
加入碱性物质如NH3/NH3·H2O,可产生BaSO3沉淀;或强氧化性物质如Cl2/酸性KMnO4等,可产生BaSO4沉淀。
3. 下列有关物质的性质与用途不具有对应关系的是( )A. SO2具有还原性,可用作葡萄酒抗氧化剂B. SO2具有氧化性,可用作纸浆漂白剂C. SO2是酸性氧化物,可用氢氧化钠溶液吸收D. SO2具有漂白性,可使品红溶液褪色
4. 按如图所示进行实验,下列说法不正确的是( )A. 石蕊溶液变红说明SO2溶于水所形成的溶液显酸性B. 品红溶液、酸性高锰酸钾溶液褪色原因不相同C. H2S溶液中出现淡黄色沉淀,该反应体现了SO2的还原性D. 该实验说明SO2的性质具有多样性
5.下列物质能使品红溶液褪色,且褪色原理基本相同的是( )①活性炭②新制氯水③二氧化硫④臭氧⑤过氧化钠⑥双氧水A.①②④B.②③⑤C.②④⑤⑥D.③④⑥
6. 检验SO2中是否混有CO2气体,可采用的方法是( )A. 通过品红溶液B. 先通过足量NaOH溶液,再通入澄清石灰水C. 通过澄清石灰水D. 先通过足量溴水,再通过澄清石灰水
高中化学人教版 (2019)必修 第二册第一节 硫及其化合物课文配套ppt课件: 这是一份高中化学人教版 (2019)必修 第二册第一节 硫及其化合物课文配套ppt课件,共30页。PPT课件主要包含了学习目标,核心素养,1游离态,硫的存在,物理性质,原子结构,化学性质,Hg+SHgS,二氧化硫,SO2等内容,欢迎下载使用。
人教版 (2019)必修 第二册第一节 硫及其化合物说课ppt课件: 这是一份人教版 (2019)必修 第二册第一节 硫及其化合物说课ppt课件,共31页。PPT课件主要包含了考纲要求,二二氧化硫,酸性氧化物的通性,还原性,四三氧化硫,五硫化氢等内容,欢迎下载使用。
高中化学第三章 铁 金属材料实验活动2 铁及其化合物的性质说课ppt课件: 这是一份高中化学第三章 铁 金属材料实验活动2 铁及其化合物的性质说课ppt课件,共23页。PPT课件主要包含了ⅥA族,自然界的硫单质,火山口附近的硫,自然界的硫化合物,黄铁矿,白铁矿,磁黄铁矿,硫的性质,硫的化学性质,2还原性等内容,欢迎下载使用。













