




2021学年第一节 硫及其化合物教课内容ppt课件
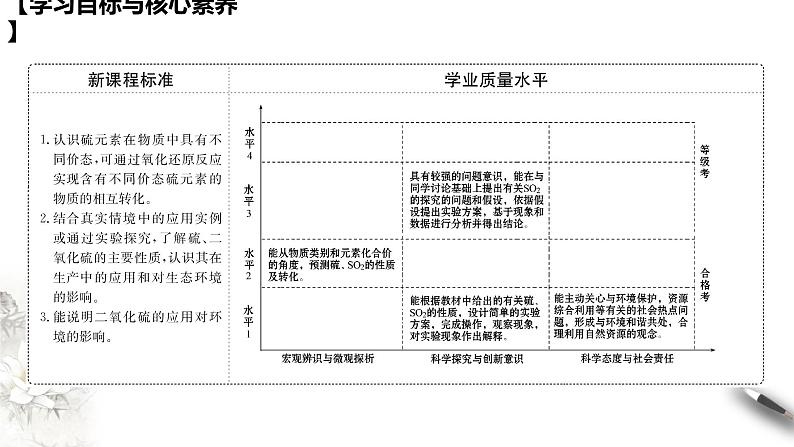
展开【学习目标与核心素养】
学习目标 1、认识硫的存在与性质。 2、会依据酸性氧化物的通性及硫元素的化合价分析理解硫的氧化物的性质,会比较二氧化硫和氯水漂白性的区别。 3、了解可逆反应的特点。
核心素养 1、通过学习硫及二氧化硫的知识培养学生论据推理与模型认知的化学核心素养。 2、通过实验进一步训练学生的操作技能,体会实验对认识和研究物质性质的重要作用,培养学生科学探究的化学核心素养。
硫元素在元素周期表中的位置
硫是一种重要的非金属元素,位于元素周期表的第三周期,VIA族。
硫原子的最外层有6个电子,在化学反应中容易得到2个电子,形成-2价的硫的化合物。与同主族的氧元素相比,硫元素的原子多一个电子层,得点子的能力相对较弱,而失电子能力则相对较强。这也是我们在富含样子的地表附近找到含硫化合物中,硫常常为+4价或+6价,而氧为-2价的原因。
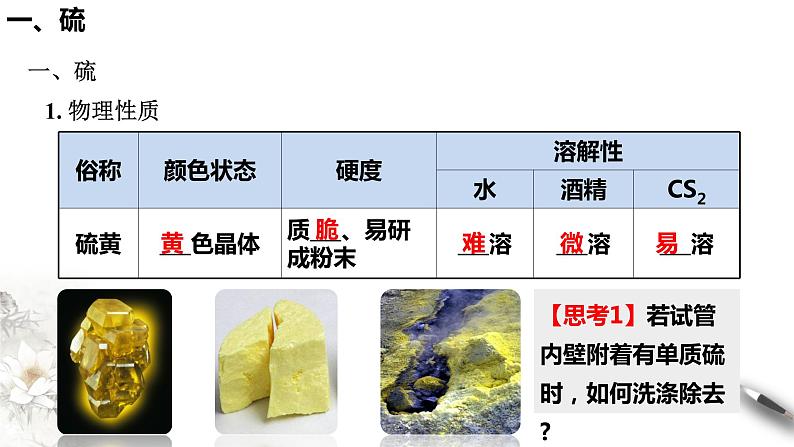
一、硫 1. 物理性质
【思考1】若试管内壁附着有单质硫时,如何洗涤除去?
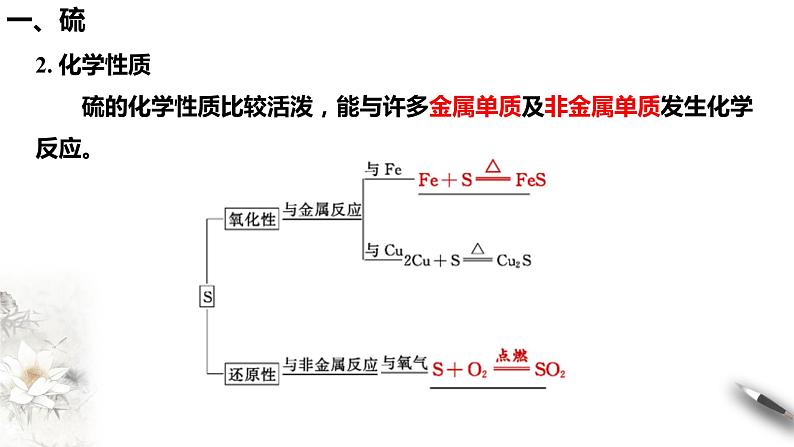
2. 化学性质 硫的化学性质比较活泼,能与许多金属单质及非金属单质发生化学反应。
3. 用途 硫黄主要用于制造硫酸、化肥、火柴及杀虫剂等,还用于制造黑火药、烟花爆竹等。
【思考2】 能不能根据Fe、Cu与S、Cl2反应的产物判断S和Cl2的氧化性的强弱?
可以。Fe、Cu与S反应生成低价的化合物,Fe、Cu与Cl2反应生成高价的化合物,故Cl2的氧化性大于S。
2.化学性质 (1) 实验探究 【实验5-1】
把充满SO2,塞有橡胶塞的试管倒立在水中,在水面下打开橡胶塞,观察试管内液面的上升。待液面高度不再明显变化时,在水下用橡胶塞塞紧试管口,取出试管,用pH试纸测定试管中溶液的酸碱度(保留该溶液供实验5-2使用)
可逆反应①正反应:向_______方向进行的反应;②逆反应:向_______方向进行的反应;③可逆反应:在_________下,既能向正反应方向进行,_____又能向逆反应方向进行的反应。
2. 化学性质 (1) 酸性氧化物的通性
SO2+2NaOH===Na2SO3+H2O
SO2 +CaO===CaSO3
三氧化硫具有酸性氧化物的通性SO3+Ca(OH)2===CaSO4+H2OSO3+CaO===CaSO4SO3+H2O===H2SO4(放出大量的热)
SO2+Br2+2H2O===H2SO4+2HBr
5SO2+2KMnO4+2H2O===K2SO4 + 2MnSO4+2H2SO4
SO2+2H2S===3S+2H2O
(2) 还原性(+4 → +6)
SO2可使氯水、KMnO4溶液褪色,可用于吸收或鉴别
(3) 氧化性(+4 → 0)
(4) 漂白性【实验5-2】
无色溶液又恢复原来的红色
SO2的漂白是暂时性的
实验过程中可以闻到刺激性气味
用试管取2mL 在实验5-1中得到的溶液,向其中滴入1-2滴品红溶液,振荡,观察溶液的颜色变化。然后加热试管,注意通风,在观察溶液的变化。
二氧化硫具有漂白作用,工业上常用二氧化硫来漂白纸浆、毛、丝等。
常见漂白剂的漂白原理及特点
3. 用途 制硫酸、漂白剂(漂白纸浆、毛、丝等)、杀菌消毒、食品添加剂。
SO2和CO2的性质比较
无色、有刺激性气味、易溶于水(1∶40)
无色、无味、能溶于水(1∶1)
能使品红褪色,能使澄清石灰水变浑浊
不能使品红褪色,能使澄清石灰水变浑浊
(1) CO2和SO2均为酸性氧化物,在性质上具有一定的相似性,结合已有的知识探究能否用澄清石灰水鉴别CO2和SO2,为什么?
不能。少量的CO2和SO2通入澄清石灰水中,均产生白色沉淀;足量的CO2和SO2通入澄清石灰水中现象都是先变浑浊后变澄清。
(2)如何检验某无色气体是SO2还是CO2?
将气体通入品红溶液中,若品红溶液褪为无色,加热,褪色后的溶液又恢复红色,则气体为SO2;若品红溶液不褪色,则为CO2。
1.下列说法正确的是________(填序号)。①硫的非金属性较强,所以只以化合态存在于自然界中。②分离黑火药中的硝酸钾、木炭、硫黄要用到二硫化碳、水及过滤操作。③硫与金属或非金属反应时均作氧化剂。④硫在空气中燃烧产物只是SO2。⑤不能由单质直接化合而制得CuS、CuCl2、Fe2S3、FeCl2。⑥用蒸馏水清洗试管内壁残留的硫。
2.判断下列有关SO2性质的叙述不正确的是________(填序号)。①能使澄清石灰水变浑浊。②能使湿润的蓝色石蕊试纸变红。③能使品红溶液褪色。④通入BaCl2溶液生成白色沉淀。⑤通入足量的NaOH溶液中再加BaCl2溶液产生白色沉淀,该沉淀能溶于盐酸。⑥通入溴水中能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀生成。⑦1 ml二氧化硫与足量水反应生成1 ml亚硫酸。⑧实验室制备SO2时,多余的SO2可用碱液吸收。
3.将硫黄在氧气中燃烧生成气体A,把气体A溶于水得溶液B,向B中滴加溴水,溴水褪色而B变为C;在C中加入Na2S产生气体D,若将D通入B溶液,可得沉淀E;A、B、C、D、E中均含有硫元素。在下列各组中按A、B、C、D、E排列的是( )A.SO2、H2SO4、H2SO3、H2S、SB.SO2、H2SO3、H2SO4、SO2、SO3C.SO2、H2SO4、H2SO3、SO2、SD.SO2、H2SO3、H2SO4、H2S、S
4.某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
请回答下列问题:(1)装置A中的化学方程式为 。
Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O
(2)实验过程中,装置B中产生的现象为____________________,这说明SO2具有______。(3)装置C的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象:__________________________________________________________________。(4)尾气可采用______溶液吸收。
品红溶液褪色后,关闭分液漏斗旋塞,点燃酒精灯加热,溶液
高中化学人教版 (2019)必修 第二册第一节 硫及其化合物教学ppt课件: 这是一份高中化学人教版 (2019)必修 第二册<a href="/hx/tb_c4000033_t3/?tag_id=26" target="_blank">第一节 硫及其化合物教学ppt课件</a>,共1页。
人教版 (2019)必修 第二册第一节 硫及其化合物集体备课ppt课件: 这是一份人教版 (2019)必修 第二册<a href="/hx/tb_c4000033_t3/?tag_id=26" target="_blank">第一节 硫及其化合物集体备课ppt课件</a>,共35页。PPT课件主要包含了游离态,化合态,硫单质的物理性质,黄色晶体易研成粉末,硫单质的化学性质,价态观,与金属反应,与非金属反应,氧化性Cl2>S,硫单质的用途等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第二册第一节 硫及其化合物课文配套ppt课件: 这是一份高中化学人教版 (2019)必修 第二册第一节 硫及其化合物课文配套ppt课件,共30页。PPT课件主要包含了学习目标,核心素养,1游离态,硫的存在,物理性质,原子结构,化学性质,Hg+SHgS,二氧化硫,SO2等内容,欢迎下载使用。













