
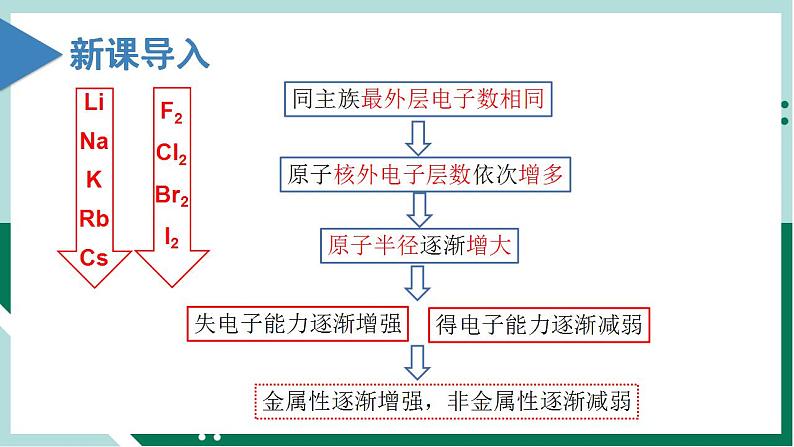
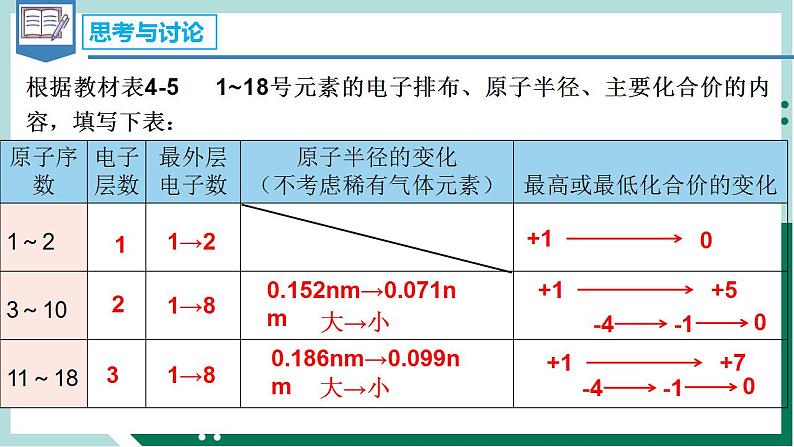

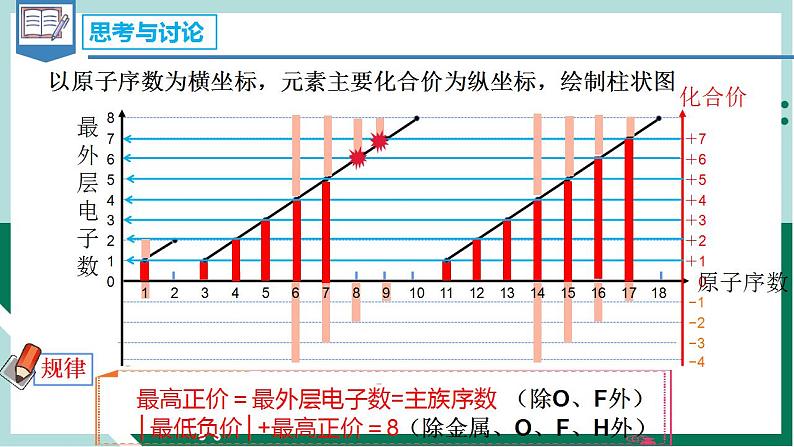






化学第二节 元素周期律备课课件ppt
展开4.2.1元素周期律
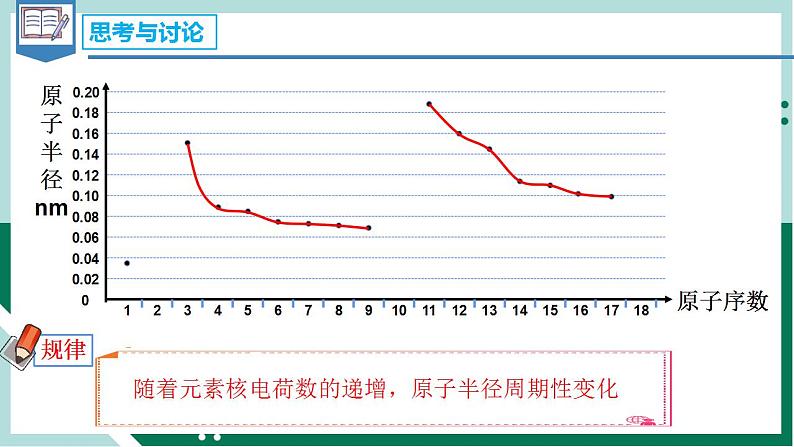
1.元素的性质随着原子序数的递增而成周期性变化的主要原因是
A.电子层数呈周期性变化 B.原子半径呈周期性变化
C.相对原子质量依次增大 D.最外层电子排布呈周期性变化
2.下列说法正确的是
A.第三周期的金属元素从左到右原子半径依次增大
B.HF、HCl、HBr、HI的热稳定性从左到右依次增强
C.第三周期非金属元素含氧酸的酸性从左到右依次增强
D.元素周期律是元素原子核外电子排布周期性变化的结果
3.几种短周期元素的原子半径及主要化合价如图所示,下列叙述正确的是
A.X、Y的最高价氧化物都是两性氧化物
B.Y的最高价氧化物对应的水化物能溶于NaOH溶液
C.Z的非金属性强于W
D.X的单质在第三周期中还原性最强
4.X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是
A.原子序数:X>Y>Z B.最高化合价:Z>X>Y
C.离子半径:X2->Y+>Z- D.原子最外层电子数:X>Y>Z
5.下列微粒半径大小关系正确的是
A.F>Cl>Br>I B.Na<Mg<Al<Si<P<S<Cl
C.Na<Na+、Cl<Cl- D.O2->F->Na+>Mg2+>Al3+
6.如表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断。以下叙述正确的是
元素代号 | A | B | C | D | E |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
A.气态氢化物的稳定性:D<C
B.E的氧化物对应水化物均为强酸
C.A、B简单离子的氧化性强弱关系为:B3+<A2+
D.C、E形成的简单离子半径大小关系为:C2->E-
7.如下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是
A.气态氢化物的稳定性:X<W
B.X与Y可以形成阴阳离子个数比为1:1和1:2的两种离子化合物
C.由X、Y、Z、W、R五种元素形成的简单离子中半径最小的是X2-
D.Y和W可以形成离子化合物
8.已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构,则下列关于X、Y、Z、W四种元素的描述中,正确的是
A.原子序数:Y>X>Z>W B.原子最外层电子数:Y>X>Z>W
C.原子半径:Y>X>Z>W D.金属性:X<Y,还原性:W2->Z-
9.短周期主族元素X、Y、Z、W在元素周期表的相对位置如图所示,它们的原子序数之和为39。下列说法错误的是
X | Y |
| Z |
|
|
| W |
A.常温常压下,X单质为固态 B.Z和W的主要化合价相同
C.原子半径:rW>rX>rY>rZ D.Y的氢化物与W的氢化物相遇产生白烟
10.短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的主族序数是其周期数的3倍,Z可与X形成淡黄色化合物Z2X2,Y、W最外层电子数相同。下列说法正确的是
A.化合物ZWX具有强氧化性 B.简单离子的还原性:Y>X>W
C.简单离子的半径:Y>Z>X>W D.简单氢化物水溶液的酸性:Y>W
11.随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。
(1)G元素在周期表中的位置为_______。
(2)元素A与C形成AC2与C与D形成的D2C2发生反应的化学方程式为_______。
(3)A、B、F三种元素的原子半径由大到小的顺序是_______。(填元素符号)
(4)D元素最高价氧化物的水化物与E元素的最高价氧化物的水化物反应的离子方程式是___。
(5)元素C、G形成的简单气态氢化物中,H2C与H2G的稳定性较强的是_______(填化学式)。
(6)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷(Rb)是37号元素,相对原子质量是85,位于IA族。关于铷的下列说法中不正确的是_______(填序号)。
A.与水反应比钠更剧烈
B.Rb2O2与水能剧烈反应并释放出O2
C.单质Rb具有很强的氧化性
D.RbOH的碱性比同浓度的NaOH弱
高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表备课课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表备课课件ppt,文件包含415卤素教学课件高一化学同步备课系列人教版1pptx、415卤族元素答案docx、415卤族元素学生docx等3份课件配套教学资源,其中PPT共22页, 欢迎下载使用。
化学必修 第一册第四章 物质结构 元素周期律第一节 原子结构与元素周期表备课课件ppt: 这是一份化学必修 第一册第四章 物质结构 元素周期律第一节 原子结构与元素周期表备课课件ppt,文件包含414碱金属教学课件高一化学同步备课系列人教版1pptx、414碱金属答案docx、414碱金属学生docx等3份课件配套教学资源,其中PPT共22页, 欢迎下载使用。
高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表备课ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表备课ppt课件,文件包含413核素教学课件高一化学同步备课系列人教版1pptx、413核素答案docx、413核素学生docx等3份课件配套教学资源,其中PPT共21页, 欢迎下载使用。













