化学必修 第一册第三节 氧化还原反应第1课时学案
展开氧化还原反应
第一课时
【学习目标】
1.通过对化学反应方程式的观察,寻找的共同之处,从而得出氧化还原反应的定义。
2.理解氧化还原反应与四大基本反应类型的关系。
3.理解化合价升降与电子转移的关系。
【学习重难点】
重点:用化合价升降和电子转移的观点理解氧化还原反应。
难点:理解氧化还原反应的本质。
【新课内容】
一、氧化还原反应的特征
1.如何将氧化铜通过反应制得铜单质?
化学反应方程式 |
| |
|
|
|
| ||
| ||
(1)这三个反应有什么共同特征?
(2)氧的得失与元素化合价升降有什么规律?请以第一个方程式为例加以解释。
(3)从化合价角度,重新给氧化还原反应定义
氧化反应: ;
还原反应: ;
氧化还原反应: ;
2.学以致用
⑴下列反应是否属于氧化还原反应?
⑵以下各反应又属于四大基本反应中的哪种反应类型?
化学反应方程式 | 是否是氧化还原反应 | 四大基本反应类型 |
①2Na+Cl22NaCl |
|
|
②CaO+H2O=Ca(OH)2 |
|
|
③CaCO3CaO+CO2↑
|
|
|
④2H2O2H2↑+O2↑ |
|
|
⑤Zn+H2SO4=ZnSO4+H2↑ |
|
|
⑥NaOH+HCl=NaCl+H2O |
|
|
⑦CaCO3+2HCl=CaCl2+CO2↑+H2O |
|
|
⑧Fe2O3+3CO2Fe+3CO2 |
|
|
⑨CuO+H2Cu+H2O |
|
|
⑶分析四大基本反应类型与氧化还原反应的关系,用数学集合中的图示法,将图画在下面。
二、氧化还原反应的本质
【问题引导】在下面这个反应中,钠和氯元素的化合价为什么会发生变化?
2Na+Cl22NaCl
【漫画故事】从本质重新定义氧化还原反应
氧化反应: ;
还原反应: ;
氧化还原定义: ;
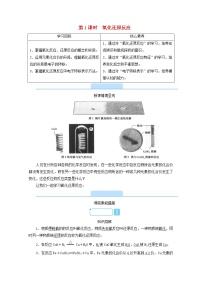
【实验探究】
实验原理:Fe+CuSO4=FeSO4=Cu
实验用品:铁片、铜片、小烧杯、灵敏电流表、两根导线及硫酸铜溶液;
实验现象:
实验结论:
【总结感悟】
现在请大家用双线桥模型来研究以下反应中化合价升降、电子转移与氧化还原反应的关系。
规律:
三、生活和诗中的氧化还原反应
四、学习小结
高中化学人教版 (2019)必修 第一册第三节 氧化还原反应学案: 这是一份高中化学人教版 (2019)必修 第一册第三节 氧化还原反应学案,共8页。
人教版 (2019)必修 第一册第三节 氧化还原反应学案: 这是一份人教版 (2019)必修 第一册第三节 氧化还原反应学案,共19页。学案主要包含了知识点填空答案,检测反馈答案,交流讨论等内容,欢迎下载使用。
鲁科版 (2019)必修 第一册第3节 氧化还原反应第1课时学案设计: 这是一份鲁科版 (2019)必修 第一册第3节 氧化还原反应第1课时学案设计,共17页。学案主要包含了双线桥法,单线桥法,非选择题等内容,欢迎下载使用。