




高中人教版 (2019)第一节 钠及其化合物课文ppt课件
展开1.认识钠是一种比较活泼的金属2.了解钠的物理 性质和主要化学性质。
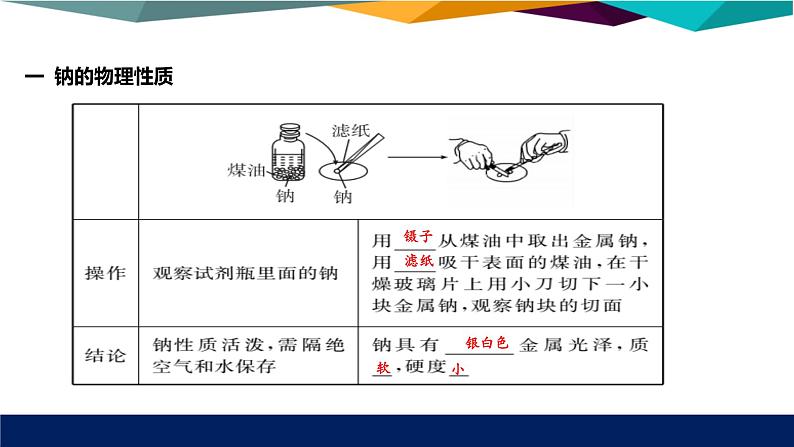
(1)取用金属钠时,应如何操作?答案:取用金属钠时,不能用手拿,应该用镊子夹取。(2)切取钠时,剩余的钠块如何处理?答案:切取钠时,剩余的钠块不能随意丢弃,应放回原试剂瓶。(3)钠保存在煤油中的原因是什么?答案:钠保存在煤油中,是因为钠的密度比煤油大,沉入煤油底部,从而使钠与空气隔绝。
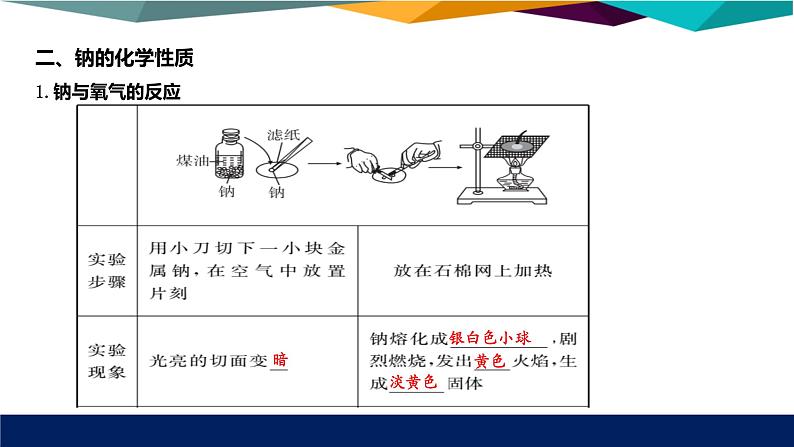
二、钠的化学性质1.钠与氧气的反应
4Na+O2====2Na2O
2Na+2H2O====2NaOH
(1)钠与水反应的现象说明了什么问题?(从活泼性角度)答案:钠与水反应的现象说明钠是一种非常活泼的金属。(2)结合钠的性质,想一想为什么不能直接用手取钠?答案:手上有汗液,钠与水反应放热并生成NaOH,会灼伤皮肤。
(3)把钠投入稀盐酸中,有何现象?相比钠与水的反应哪个更剧烈?为什么?并写出钠与盐酸反应的化学方程式。答案:浮、熔、游、响,钠与盐酸溶液反应比与水反应更剧烈,因为钠与水反应的实质是钠与H+反应,盐酸中H+浓度比水中的大,所以更剧烈。2Na+2HCl====2NaCl+H2↑。
(4)钠长时间露置于空气中会变暗,然后变成液体,再变成白色固体,最后变成白色粉末。列出其变化过程并用化学方程式表示。答案:钠在空气中变质的过程:Na Na2O NaOH Na2CO3·10H2O Na2CO3,故Na、Na2O、Na2O2、NaOH在空气中露置时,最终均转化为Na2CO3。4Na+O2 === 2Na2O;Na2O+H2O == 2NaOH;2NaOH+CO2+9H2O === Na2CO3·10H2O;Na2CO3·10H2O===Na2CO3+10H2O。
3.金属钠与盐溶液的反应将少量金属钠块放入硫酸铜溶液中,观察现象并讨论分析原因。现象:___________________________________。化学方程式:________________________ _______________________________。
浮、熔、游、响、溶液中生成蓝色沉淀
2Na+2H2O====2NaOH+H2↑、
2NaOH+CuSO4====Cu(OH)2↓+Na2SO4
(1)钠能不能从盐溶液中置换出金属?为什么?答案:钠不能从盐溶液中置换出金属,因为钠会先和水反应生成NaOH和H2,NaOH再和盐反应。(2)钠与熔融态的盐可以反应,可以置换出较不活泼的金属。如4Na+TiCl4 Ti+4NaCl,用钠还可以制取锆、铌、钽等金属。
三 钠的存在、保存及用途1.存在:钠的化学性质很活泼,在自然界中以_______存在。2.保存:因为常温下钠能与空气中的_____、___反应,所以钠保存在_____中,主要是为了隔绝_____。3.用途:①制取Na2O2等钠的化合物;②钠和钾的合金(室温呈液态)作原子反应堆的导热剂;③在电光源上,用钠制造高压钠灯。
化学必修 第一册第一节 钠及其化合物精品ppt课件: 这是一份化学必修 第一册<a href="/hx/tb_c161979_t3/?tag_id=26" target="_blank">第一节 钠及其化合物精品ppt课件</a>,共37页。PPT课件主要包含了钠与非金属的反应,钠与水的反应等内容,欢迎下载使用。
人教版 (2019)必修 第一册第一节 钠及其化合物备课ppt课件: 这是一份人教版 (2019)必修 第一册第一节 钠及其化合物备课ppt课件,共35页。PPT课件主要包含了夯基提能·一遍过,化合物,银白色的金属光泽,石蜡油,答案C,淡黄色,Na2S,钠与水的反应,NaOH+H2↑,干燥的沙土等内容,欢迎下载使用。
人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第一节 钠及其化合物教课内容ppt课件: 这是一份人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第一节 钠及其化合物教课内容ppt课件,共32页。













