








- 1.3氧化还原反应(第二课时)课件+教案+练习 课件 82 次下载
- 2.1钠及其化合物(第一课时)课件+教案+练习 课件 93 次下载
- 2.2氯及其化合物(第一课时)课件+教案+练习 课件 87 次下载
- 2.2氯及其化合物(第二课时)课件+教案+练习 课件 87 次下载
- 2.2氯及其化合物(第三课时)课件+教案+练习 课件 86 次下载
人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第一节 钠及其化合物图文ppt课件
展开一、新课导入二、Na2CO3和NaHCO3的物理性质三、Na2CO3和NaHCO3的化学性质(1)热稳定性 (2)与盐酸的反应 (3)与碱的反应 (4)与盐的反应四、Na2CO3和NaHCO3的相互转换五、Na2CO3和NaHCO3的鉴别方法六、侯德榜制碱法七、焰色反应八、碱金属
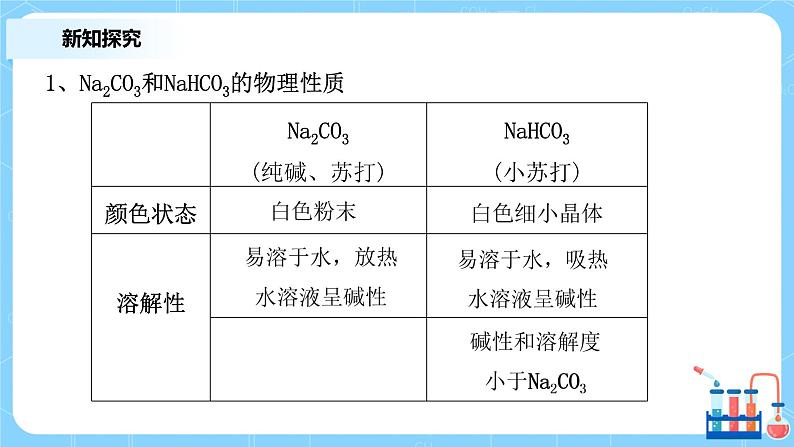
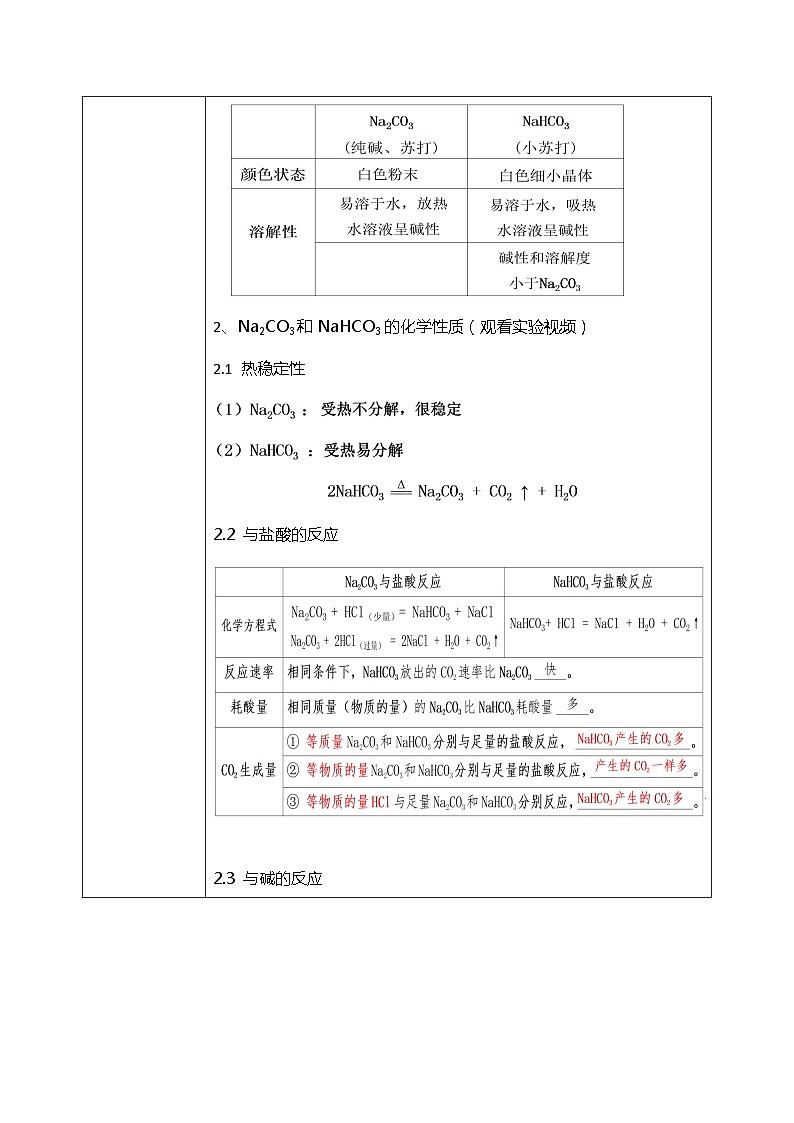
1、Na2CO3和NaHCO3的物理性质
2、Na2CO3和NaHCO3的化学性质
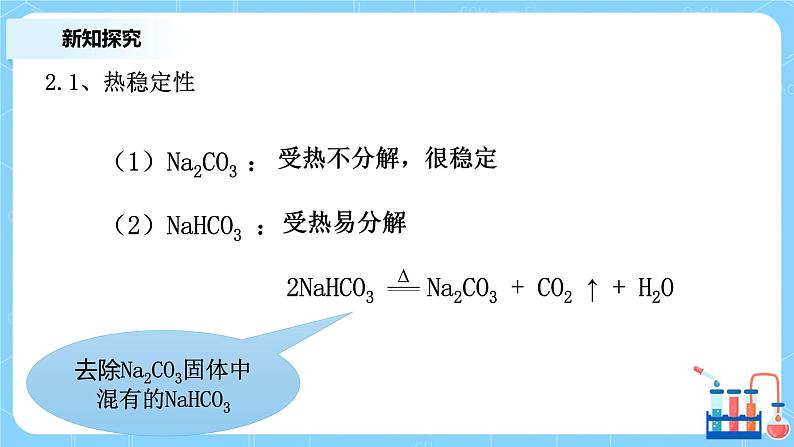
(1)Na2CO3 :(2)NaHCO3 : 2NaHCO3 Na2CO3 + CO2 ↑ + H2O
去除Na2CO3固体中混有的NaHCO3
一、与NaOH反应:二、与澄清石灰水的反应: Na2CO3 + Ca(OH)2 = CaCO3↓ + 2NaOH 2NaHCO3 + Ca(OH)2(少量) = CaCO3↓ + 2H2O + Na2CO3 NaHCO3 + Ca(OH)2(过量) = CaCO3↓ + H2O + NaOH
(1)与CaCl2的反应: (2)与CaSO4的反应: CO32- + CaSO4 CaCO3 + SO42-
3、Na2CO3和NaHCO3的相互转换
Na2CO3 NaHCO3
通入CO2 / 滴加少量酸
向Na2CO3溶液中通入CO2: Na2CO3 + H2O + CO2 = 2NaHCO3向Na2CO3溶液中滴加少量酸:Na2CO3 + HCl = NaHCO3 + NaClNaHCO3受热分解:2NaHCO3 Na2CO3 + H2O + CO2↑NaHCO3与碱反应:NaHCO3 + NaOH = Na2CO3+ H2O
4、Na2CO3和NaHCO3的鉴别方法
向饱和NaCl溶液中通入足量NH3、CO2 : NaCl + H2O + CO2+ NH3 = NaHCO3↓+ NH4Cl 2NaHCO3 Na2CO3 + H2O + CO2↑(1)先通入NH3再通入CO2。(2)利用相同浓度下NaHCO3溶解度相对较小的性质。(3)CO2可以循环利用。(4)可得到副产品NH4Cl。
书写离子方程式时不能拆分
(洗)—— 将铂丝(或光洁无锈的铁丝)用盐酸洗净(烧)—— 将洗净的铂丝在外焰上灼烧至与原火焰颜色相同(蘸)—— 蘸取试样(烧)—— 在外焰上灼烧,并观察火焰的颜色(洗)—— 用盐酸洗净铂丝(或铁丝),并在外焰上灼烧至无色
某些金属或它们的化合物在灼烧时,使火焰产生特殊的颜色。用于检验某些金属元素,属于物理变化,是电子跃迁的结果。
一定透过蓝色钴玻璃,否则无法排除Na干扰。
1、Na2CO3和NaHCO3的物理性质2、Na2CO3和NaHCO3的化学性质 (1)热稳定性 (2)与盐酸的反应 (3)与碱的反应 (4)与盐的反应3、Na2CO3和NaHCO3的鉴别方法
请学生课后了解纯碱的生产历史,进一步认识侯氏制碱法的原理。
化学必修 第一册第一节 钠及其化合物优质课ppt课件: 这是一份化学必修 第一册第一节 钠及其化合物优质课ppt课件,共60页。PPT课件主要包含了过氧化钠,过氧化钠长什么样子,滴水生,过氧化钠有何用途,焰色试验,还有什么疑问,课堂小结等内容,欢迎下载使用。
高中化学第二章 海水中的重要元素——钠和氯第一节 钠及其化合物精品ppt课件: 这是一份高中化学第二章 海水中的重要元素——钠和氯第一节 钠及其化合物精品ppt课件,共60页。PPT课件主要包含了活泼的金属单质钠,如果要研制钠电池,我们要从哪里入手,的总储量可达4亿亿吨,NaCl,钠的工业制备,Na+,Na+H2O→,OH-,你观到哪些现等内容,欢迎下载使用。
人教版 (2019)必修 第一册第一节 钠及其化合物授课ppt课件: 这是一份人教版 (2019)必修 第一册第一节 钠及其化合物授课ppt课件,共29页。PPT课件主要包含了导入新课,海水晒盐,海洋生物,钠与氧气的反应,钠与水的反应,相关链接,课堂小结,达标检测等内容,欢迎下载使用。














