






沪教版九年级上册第1节 构成物质的基本微粒备课课件ppt
展开1.通过实验探究,了解微粒的性质,并能用微粒的观点解释某些常见的现象;2.认识物质是由分子、原子和离子等微粒构成的;3.知道原子的构成,及相对原子质量的意义;4.以氯化钠为例,了解离子的概念及形成;5.了解化学在宏观物质与微观粒子之间建立联系的途径和特点。
我国在1964年10月16日成功爆炸我国第一颗原子弹。你知道原子弹的能量来自哪里吗?
原子是一个实心的小球吗?原子还能再分吗?
英国化学家道尔顿(J.Daltn , 1766~1844)
英国物理学家汤姆生( ,1856~1940)
卢瑟福和他的助手做了著名的α粒子散射实验
英国科学家卢瑟福(E.Rutherfrd,1871~1937)
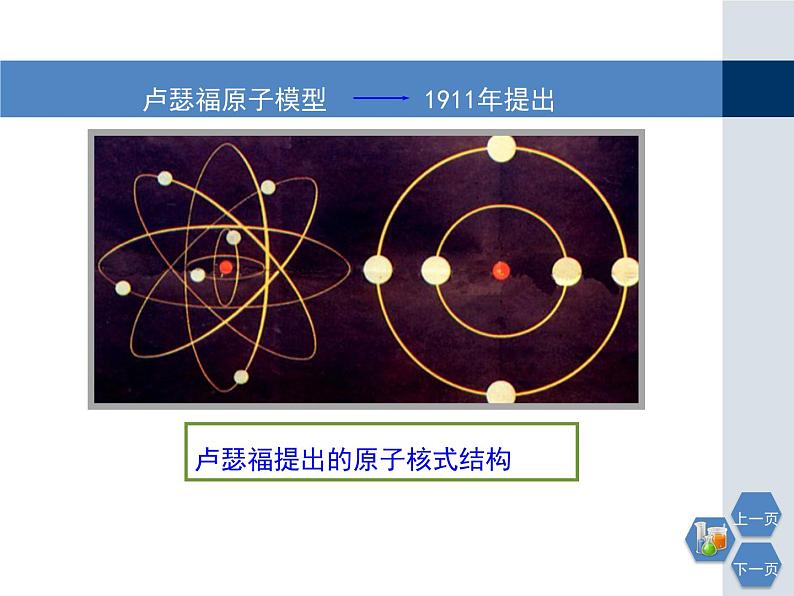
卢瑟福提出的原子核式结构
1919年 卢瑟福发现质子1919年,卢瑟福用α粒子轰击氮原子核时,捕捉到了一种新的质量更小的粒子,将其命名为质子。在这个不同寻常的实验中,卢瑟福不仅发现了质子,还实现了人类历史上第一个核反应。1932年,英国物理学家查德威克用α粒子轰击铍原子核捕捉到了中子。
原子核还可以再分,原子弹就是利用了原子核裂变时放出的巨大能量。
1.原子的构成原子由原子核和核外电子组成,原子核由质子和中子组成。
如氦原子核内有2个质子,则氦原子核带2个单位正电荷(即+2)。科学上把原子核所带的正电荷数称为核电荷数,氦原子的核电荷数为2
2.质子、中子、电子的电性和电量
一个质子带一个单位正电荷中子不带电一个电子带一个单位负电荷
不一定所有的原子核内都有中子
分析下表可以获得哪些信息?
不同种类的原子,其核电荷数、质子数是不同的。一个原子其核内质子数与中子数不一定相同。同种原子其核电荷数=质子数=核外电子数。
原子核的大小约为10-15 m~10-14 m。原子的直径大约是10-10 m。
3.原子核与原子大小的比较
比较电子、原子核的质量大小
2.m(原子) = m(原子核) + m(电子) ≈ m(原子核) ≈ m(质子) + m(中子)
1.电子质量很小,整个原子的质量主要集中在原子核上
如此小的值,该如何计算?
相对原子质量定义: 以一种碳原子的质量的1/12作为基准,其他原子的质量与这一基准的比,称为这种原子的相对原子质量(符号为Ar)。
=1.993×10-27Kg
=1.66×10-27Kg
水(H2O)的相对分子质量= (H的相对原子质量×2) + (O的相对原子质量×1)=(1×2) + (16×1) =18
试一试:计算O2、H2O2的相对分子质量。
相对分子质量(Mr) = 化学式中各原子相对原子质量的总和
规律:近似相对原子质量=质子数+中子数
例.已知铯-137的质子数为55,中子数为82。下列有关铯-137的说法正确的是( )A.铯-137原子的核外电子数为82 B.铯-137的相对原子质量为137gC.铯-137原子的核电荷数为55 D.铯-137属于非金属元素
6.门捷列夫的元素周期表
原子序数=核电荷数=质子数
元素周期表中某一格所得信息:
1-20号元素氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙
6.核外电子的运动状况:
电子层 1 2 3 4 5 6 7
表示电子层以及电子层上的电子数
表示原子核以及核内的质子数
(1)根据能量最低原理,先排满第一层,再排第二层,依次向外。(2)第一层最多排2个电子 ;第二层最多排8个电子;(3)一般情况下,化学反应中的原子最外层达到稳定结构(即最外层电子数为8个或第一个电子层时为2个)。
1.判断下列原子结构示意图的正误
O Al F Na P
⑴比镁原子少1个质子的原子。⑵原子核只有1个质子的原子。⑶核电荷数为18的原子。
2.用原子结构示意图表示:
读图探索:1.下面各原子的原子结构示意图排列有什么规律?2.原子的化学性质和原子的哪些结构关系最密切?
一般情况下,化学反应中的原子总要使自己的最外层达到稳定结构(即最外层电子数为8个或一个电子层时为2个)。
原子结构与原子性质的关系
易发生化学反应、性质活泼
难得失电子(为稳定结构)
极难发生化学反应、性质稳定
原子的化学性质与原子最外层电子数关系最为密切
1.指出下列哪几种原子的化学性质相似
2.下列五种微粒中最易失去电子的是 ,最易得到电子的是 ,原子化学性质比较相似的是 。
A B C
D E
由于金属原子、非金属原子的原子核外最外层没有达到稳定结构,在化学反应中容易得失电子,从而达到稳定结构,那么,得失电子的结果怎样呢?
每个镁离子带2个单位的正电荷
原子中:质子数=电子数
阳离子中:质子数>电子数阴离子中:质子数<电子数
4.原子和离子的联系和区别
(带正电) (带负电)
物质与构成微粒之间的关系:
【典例1】1911年著名物理学家卢瑟福为探索原子的内部结构进行了实验。在用一束带正电的、质量比电子大得多的高速运动的α粒子轰击金箔时发现:(1)大多数α粒子能穿透金箔而不改变原来的运动方向;(2)一小部分α粒子改变了原来的运动方向;(3)有极少部分α粒子被弹了回来。下列对原子结构的认识错误的是( )A.原子核体积很小 B.原子核带正电C.原子内部有很大的空间 D.原子是实心的球体
【典例2】下列说法中,正确的是( )A.所有碳原子的质量都相等 B.相对原子质量以碳原子质量的1/12作为标准C.相对原子质量和原子的实际质量是一个概念 D.一种原子的相对原子质量近似等于原子核内质子数和中子数之和
【典例3】(2010·株州中考)如图为氯原子的结构示意图,下列有关说法错误的是( )A.氯原子的核电荷数为17B.氯原子最外层有7个电子C.氯原子的质子数为17D.在化学反应中氯原子容易失去电子
【典例4】下列说法中正确的是( )A.结构示意图为 的粒子一定是氖原子 B.Mg2+的核电荷数是12,则其核外电子数为14C.Na和Na+的化学性质相同 D.原子变成离子时,得失电子都有可能
1.原子结构中,下列等式成立的是( )①中子数=质子数 ②核电荷数=电子数 ③质子数=电子数 ④核电荷数=中子数A.①②④ B.①③ C. ②③ D.①②③2.原子结构中一定含有的微粒是( )A.质子、中子、电子 B.质子、电子C.质子、中子 D.中子、电子
3.原子中决定相对原子质量大小的主要微粒是( )A.质子数和电子数 B.核电荷数 C.中子数和电子数 D.质子数和中子数4.(2010·乐山中考)硒是人体必需的一种微量元素,严重缺硒有可能诱发皮肤疾病。已知硒的原子序数为34,质子数与中子数之和为79。下列有关硒原子的说法中,不正确的是( )A.核外电子数为34 B.核电荷数为79C.质子数为34 D.中子数为45
5.(2010·兰州中考)下列各粒子结构示意图中,表示化学性质最稳定的原子是( ) A B C D
6.某原子的结构示意图为 有关它的说法正确的是( )A.最外层电子数是8 B.质子数为12C.该原子化学性质稳定 D.该原子属于非金属原子
7.(2010·鞍山中考)右图是钠原子结构示意图。根据图可知钠原子中质子数为 ,在化学反应中钠原子容易 (填得失几个电子),而变成 (用符号表示)。
下图为钠元素的原子结构示意图,下列说法不正确的是 ( )A.钠原子核外有三个电子层B.钠原子在化学反应中易得到电子C.钠原子最外层电子数为1D.钠原子核外电子总数为11
下列说法不正确的是( )A.原子可以通过得失电子变成离子,但离子不能变成原子B.原子、分子、离子都是构成物质的微粒C.原子的质量几乎都集中在原子核上D.食盐是由离子构成的
沪教版第1节 构成物质的基本微粒精品ppt课件: 这是一份沪教版第1节 构成物质的基本微粒精品ppt课件,文件包含第3章第1节第2课时教学课件pptx、第3章第1节第2课时教案含练习docx等2份课件配套教学资源,其中PPT共18页, 欢迎下载使用。
沪教版九年级上册第3章 物质构成的奥秘第1节 构成物质的基本微粒评课课件ppt: 这是一份沪教版九年级上册第3章 物质构成的奥秘第1节 构成物质的基本微粒评课课件ppt,共15页。PPT课件主要包含了绚丽多姿的物质,微粒的性质,比一比谁的力气大,探究微粒的特点,做一做等内容,欢迎下载使用。
沪教版九年级上册第3章 物质构成的奥秘第1节 构成物质的基本微粒备课ppt课件: 这是一份沪教版九年级上册第3章 物质构成的奥秘第1节 构成物质的基本微粒备课ppt课件,共14页。PPT课件主要包含了物质是由什么组成的,物质是由什么构成的,氮微粒,氧微粒,我的解释,提出假说,证据之四,解释论证等内容,欢迎下载使用。













