








初中化学沪教版九年级上册第1节 构成物质的基本微粒精品ppt课件
展开第3章 物质构成的奥秘
第1节 构成物质的基本微粒
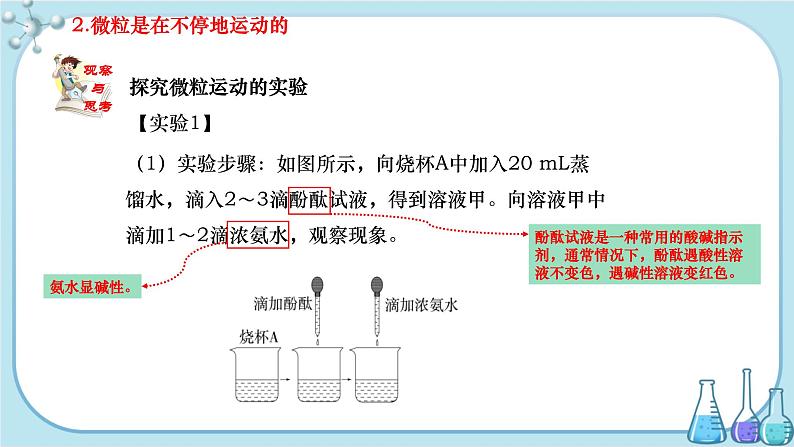
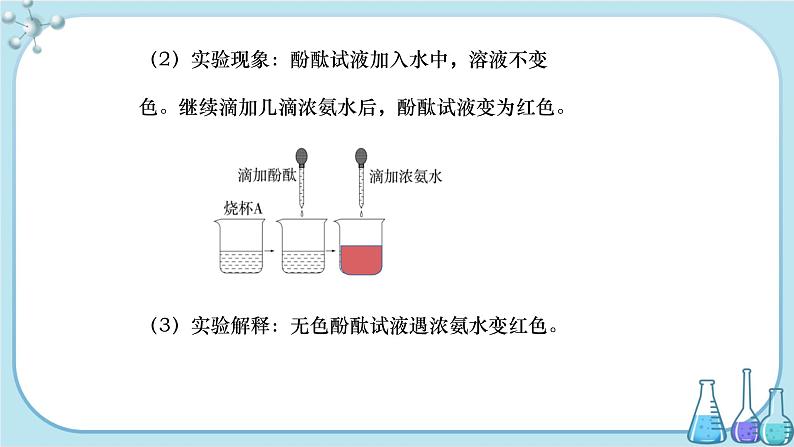
设计说明 本节内容是从微观的角度研究物质的组成,建立物质是由微粒构成的基本观念。本节知识比较抽象,让学生根据现象进行想象,进入微观世界,建立起物质是由微粒构成的基本观念,并明确微粒所具有的基本性质。分子和原子是初中学生初次接触到的微小粒子,学生将从认识分子、原子的真实存在,开始认识微观世界,是化学学习由形象到抽象、从宏观转向微观的开始。原子的构成是学习本章的基础,后面元素的概念就是在此基础上引出的,在介绍完原子与分子之间的变化及联系后,又从内部结构认识原子,再从宏观的质量和相对质量上进行把握和应用。原子结构示意图为学习离子的形成和离子符号的书写有重要的意义,在教学过程中,借助直观的多媒体课件和一些关于微观粒子运动变化的动画或图片,诱发学生想象,帮助他们对知识的理解,把抽象的知识形象化,激发学生学习这部分知识的兴趣。 教学目标 【知识与技能】 1.知道物质是由微粒构成的。知道分子是保持物质化学性质的最小粒子,原子是化学变化中的最小粒子,知道离子也是构成物质的一种粒子。 2.能用微粒的观点解释某些常见的现象。 3.知道分子、原子和离子的联系和区别。 4.知道原子的构成以及构成粒子之间的关系。 5.知道相对原子质量的含义,并学会查相对原子质量表。 6.能运用相对原子质量的两个公式进行相关计算。能根据相对原子质量求算相对分子质量。 7.了解原子核外的电子是分层排布的。了解构建原子结构示意图是一种模型化的方法。 8.了解典型元素(稀有气体、金属和非金属)原子核外电子排布的特点。 9.知道原子和离子通过得失电子可以相互转化,了解离子形成的过程。 【过程与方法】 1.能运用分子、原子的观点解释物质的变化和物质的分类。 2.充分利用教材提供的图、表等资料教学手段,化抽象为直观,初步学会运用类比、想象、归纳、概括等方法获取信息并进行加工。 【情感、态度与价值观】 1.逐步提高抽象的思维能力、想象力和分析推理能力。激发学生对微观世界的探究欲和学习化学的兴趣。 2.进行世界的物质性、物质的可分性的辨证唯物主义观点的教育。 重点难点 教学重点 1.认识物质是由微粒构成的、微粒是不断运动的、微粒之间存在空隙。 2.知道构成物质的三种基本微粒:分子、原子、离子。 3.知道原子的构成,掌握三种微粒之间的联系与区别。 4.能根据相对原子质量求算相对分子质量。 教学难点 1.能用微粒的观点解释某些常见的生活现象。 2.学会用比较的方法来研究事物的异同点。 教学方法 1.利用比较法学习原子、分子、离子等微观粒子。学习运用对比的方法在微观世界和宏观世界之间架起一座桥梁。 2.以实验探究为主线,结合交流、讨论、分析归纳等方法,培养学生善于动手、善于观察、善于思考的能力。 教具、学具 大烧杯、小烧杯、胶头滴管、一端封口的细玻璃管、注射器、蒸馏水、酚酞试液、浓氨水、无水酒精、多媒体课件等。 授课时数 4课时 第1课时 教学过程 导入新课 “墙角数枝梅,凌寒独自开。遥知不是雪,为有暗香来。”这首古诗大家都很熟悉,为什么诗人在远处就能闻到花香呢?是因为产生花香的粒子不断运动的结果。本节我们就开始学习构成物质的基本粒子。 讲授新课 【教师提问】 根据前面的学习和已有的经验,你对物质的构成微粒有怎样的认识?可用哪些事实来解释你的认识? 【教师点拨】 物质的构成微粒很小,可用肉眼看不到来解释。 【教师讲述】 一、微粒的性质 1.微粒很小,肉眼看不见 (1)物质都是由极其微小的、肉眼看不见的微粒构成的。如水是由水微粒构成的,蔗糖是由蔗糖微粒构成的。 (2)大量的微粒聚在一起的时候,就形成了我们感知的物质。 【教师点拨】 一滴水的质量很小,但一滴水里大约有1.67×1021个水分子,这些水分子如果10亿人来数,每人每分钟数100个,日夜不停,需要三万多年才能数完。 【多媒体展示】 【实验演示】 2.微粒是在不停地运动的 【实验1】 (1)实验步骤:如图所示,向烧杯A中加入20 mL蒸馏水,滴入2~3滴酚酞试液,得到溶液甲。向溶液甲中滴加1~2滴浓氨水,观察现象。 (2)实验现象:酚酞试液加入水中,溶液不变色。继续滴加几滴浓氨水后,酚酞试液变为红色。 (3)实验解释:无色酚酞试液遇浓氨水变红色。 【教师点拨】 (1)酚酞试液是一种常用的酸碱指示剂,通常情况下,酚酞遇酸性溶液不变色,遇碱性溶液变红色。 (2)氨水显碱性。
【多媒体展示】 【实验演示】 【实验2】 (1)实验步骤:如图所示,在烧杯C中重新配制甲溶液。在烧杯B中加入3~5 mL浓氨水,用一个大烧杯把两个烧杯罩在一起,观察实验现象。 (2)实验现象:烧杯C中酚酞试液变红。 (3)实验解释:构成浓氨水的微粒从烧杯B中运动到烧杯C中去了,无色酚酞试液遇氨水变红色。 【教师点拨】 构成物质的微粒是不断运动的,微粒的运动速率与温度有关。温度越高,微粒运动速率越快。例如湿衣服在夏天比在冬天干得快。 【多媒体展示】
【教师提问】 同学们还能想到哪些体现微粒在不停运动的其他实例? 【教师点拨】 ①走近鲜花盛开的花园时,会闻到花的香味。 ②湿衣服晒干。 ③打开盛酒精的试剂瓶时,会嗅到酒精的气味。 ④训练有素的警犬,能够利用罪犯留下的气味,顺藤摸瓜,抓到罪犯。 ⑤酒香不怕巷子深。 【实验演示】 3.微粒之间有空隙 【实验1】水与酒精混合实验 取一根约30 cm长一端封口的细玻璃管,进行以下实验。 事先预测结果,并与实际记录值进行比较。 (1)实验步骤:先往玻璃管中加入滴有红墨水的水至玻璃管容积的1/2,再滴入无水酒精,使其充满玻璃管。用手指堵紧开口的一端,颠倒数次。 (2)预测结果:三种结果如下 ①酒精与水混合后,体积大于两者体积之和。 ②酒精与水混合后,体积小于两者体积之和。 ③酒精与水混合后,体积等于两者体积之和。 (3)实验结果:酒精与水混合后,体积小于两者体积之和。 (4)实验解释:说明微粒之间有空隙,不同物质微粒之间空隙的大小不同。 【实验2】水和空气的压缩实验 (1)实验步骤:取两支大小相同的医用注射器,将栓塞向外拉,分别吸入等体积的空气和水,用手指顶住注射器末端的小孔,将栓塞慢慢推入。 (2)实验现象:抽取空气的注射器容易压缩,抽取水的注射器不易压缩。 (3)实验解释:空气微粒之间的空隙大,易被压缩,水微粒之间的空隙小,不易被压缩。 【教师点拨】 (1)在固体、液体中,微粒之间的空隙比较小,在气体物质中,微粒之间的空隙比较大,所以气体物质往往比较容易被压缩,固体和液体物质不易被压缩。 (2)同一种物质,随着三态(固态、液态、气态)的变化,其微粒间的空隙也发生变化。 (3)一般物质有热胀冷缩的现象,这是构成物质的微粒之间的空隙受热时增大、遇冷时减小的缘故,微粒本身的大小并没有改变。 【教师讲述】 4.构成物质的基本微粒 科学家经过长期研究证实,构成物质的基本微粒有分子、原子和离子。 (1)由分子构成的物质:氢气、氧气、氮气、二氧化碳、氨气、水、酒精等。 (2)由原子构成的物质:铁、铜、汞、金刚石、硅等。 (3)由离子构成的物质:氯化钠、碳酸钠(纯碱)、硫酸铜等。 课堂小结 今天,我们学习了微粒的性质,我们知道:微粒很小,肉眼看不见;微粒是在不停地运动的;微粒之间有空隙。构成物质的基本微粒包括原子、分子和离子。 当堂达标 1.下列各组物质中,都由分子构成的一组是( ) A.金和金刚石 B.水和氨气 C.汞和氯化钠 D.干冰和硫酸铜 答案:B 2.下列事实中能说明微粒间有空隙的是( ) A. 25 m3石油气可装入0.024 m3的钢瓶中 B.湿衣服在阳光下比阴凉处易干 C.一滴水中约有1.67×1021个水分子 D.通电时水分子变为氧分子、氢分子 答案:A 3.某兴趣小组的同学做如图甲和乙的实验探究分子的运动。从微粒角度解释下列有关问题。
甲 乙 (1)①图甲中品红在水中扩散的原因是______________。 ②品红在热水中扩散速度快,其原因是_________________________。 (2)①图乙的实验现象是_______________________________________。 ②实验结论是_________________。 答案:(1)①微粒是不断运动的 ②温度升高,微粒的运动速率加快 (2)①烧杯A中液体由无色变为红色,烧杯B中液体不变色 ②微粒是不断运动的 板书设计 第3章 物质构成的奥秘 第1节 构成物质的基本微粒 第1课时 一、微粒的性质 1.微粒很小,肉眼看不见 2.微粒是在不停地运动的 3.微粒之间有空隙 4.构成物质的基本微粒
|
沪教版九年级上册第1节 构成物质的基本微粒试讲课教学ppt课件: 这是一份沪教版九年级上册第1节 构成物质的基本微粒试讲课教学ppt课件,文件包含31构成物质的基本微粒第1课时课件pptx、31构成物质的基本微粒第1课时练习含答案解析docx、31构成物质的基本微粒第1课时练习docx、01高锰酸钾由微粒构成wmv、02分子运动现象-氨水wmv、03酒精与水混合wmv、04气体与液体的压缩性比较wmv等7份课件配套教学资源,其中PPT共24页, 欢迎下载使用。
初中化学沪教版九年级上册第1节 构成物质的基本微粒公开课ppt课件: 这是一份初中化学沪教版九年级上册第1节 构成物质的基本微粒公开课ppt课件,文件包含第3章第1节第4课时教学课件pptx、第3章第1节第4课时教案含练习docx等2份课件配套教学资源,其中PPT共20页, 欢迎下载使用。
化学第1节 构成物质的基本微粒优质ppt课件: 这是一份化学第1节 构成物质的基本微粒优质ppt课件,文件包含第3章第1节第3课时教学课件pptx、第3章第1节第3课时教案含练习docx等2份课件配套教学资源,其中PPT共18页, 欢迎下载使用。













