



初中化学人教版九年级下册课题3 溶液的浓度课文配套课件ppt
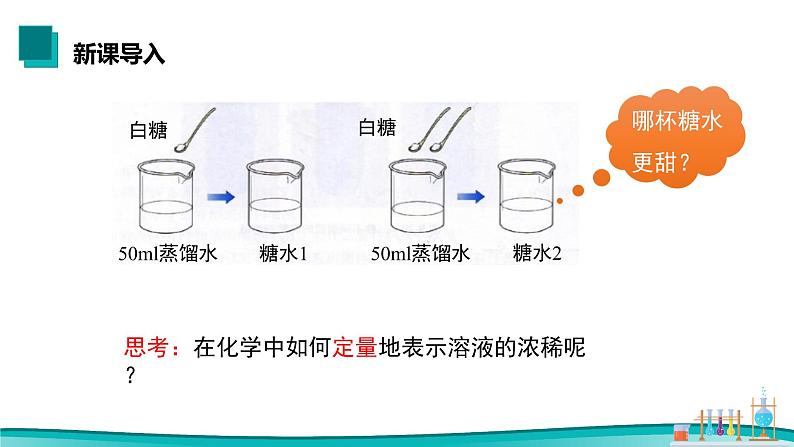
展开思考:在化学中如何定量地表示溶液的浓稀呢?
实验9-7:三种浓稀不同的硫酸铜溶液
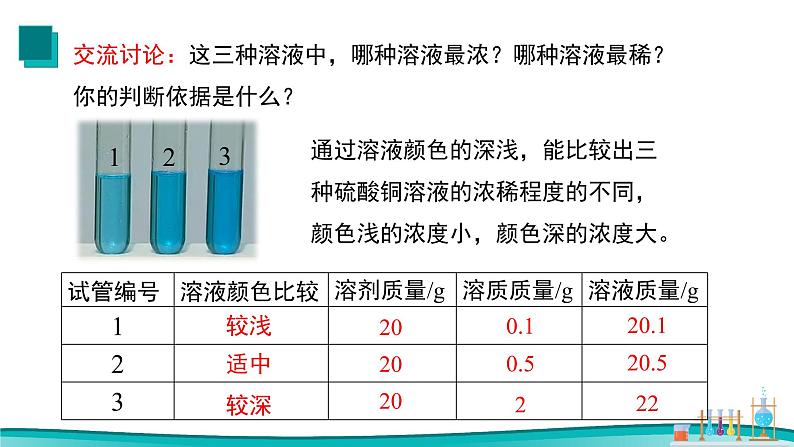
交流讨论:这三种溶液中,哪种溶液最浓?哪种溶液最稀?你的判断依据是什么?
通过溶液颜色的深浅,能比较出三种硫酸铜溶液的浓稀程度的不同,颜色浅的浓度小,颜色深的浓度大。
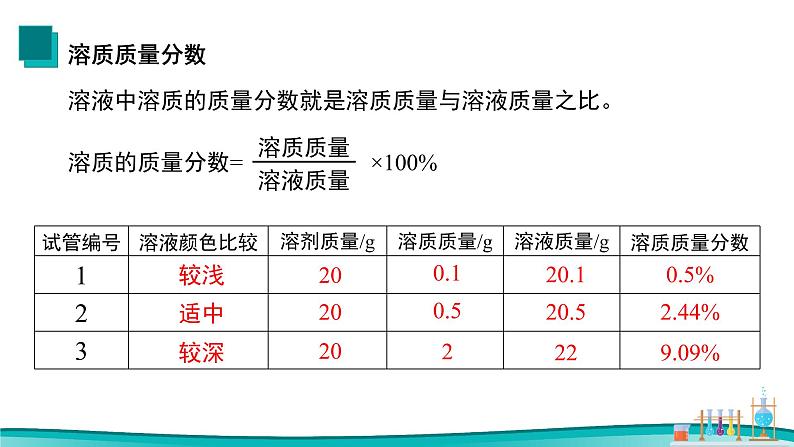
溶液中溶质的质量分数就是溶质质量与溶液质量之比。
农用16%的食盐水选种
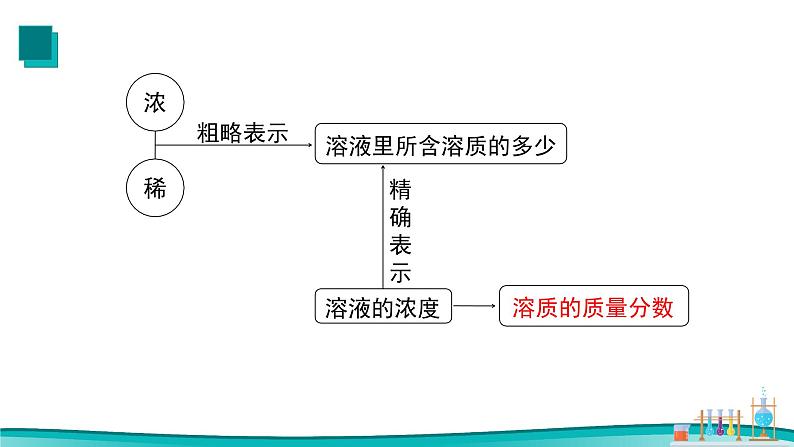
溶质质量分数——定量表示溶液的浓度
对于溶质为液体的溶液而言,常用体积分数来表示溶液的浓度。
用作消毒剂的医用酒精中乙醇的体积分数为75%,就是指每100体积的医用酒精中含75体积的乙醇。
实验9-8:配制两种质量分数不同的氯化钠溶液
交流讨论:已知20℃时,氯化钠的溶解度是36g。有人说:“20℃时,氯化钠饱和溶液中溶质的质量分数为36%。”这种说法对吗?为什么?
交流讨论:如果用S表固体物质的溶解度,用a%表示溶质的质量分数,如何表示出两者之间的关系呢?
某温度下饱和溶液的溶质质量分数=
在20℃时,Ca(OH)2的溶解度是0.17g,问此温度下将1g Ca(OH)2固体放入200g水中,充分溶解后,所得溶液的溶质质量分数是多少?
该温度下200g水中只能溶解0.34g Ca(OH)2固体,溶液即饱和。
答:所得溶液的溶质质量分数是0.17%。
交流讨论:根据溶质的质量分数的公式,能不能得到溶质和溶剂的质量?
溶质质量=溶液质量×溶质的质量分数
溶液质量=溶质质量+溶剂质量
溶剂质量=溶液质量-溶质质量
【例题1】在农业生产上,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150 kg的这种溶液,需要氯化钠和水的质量各是多少?
解:溶质质量=溶液质量×溶质的质量分数 =150 kg×16% =24 kg 溶剂质量=溶液质量-溶质质量 = 150 kg-24 kg = 126 kg答:配制150 kg质量分数为16%的氯化钠溶液需24 kg氯化钠和126 kg水。
【例题2】化学实验室现有质量分数98%的浓硫酸,但在实验中常需要用较稀的硫酸。要把50g上述浓硫酸稀释为质量分数为20%的硫酸,需要水的质量是多少?
解:设稀释后溶液的质量为x
50g ×98% = x×20%
答:需要水的质量195g。
需要水的质量= 245 g– 50g = 195g
【分析】稀释前溶质质量=稀释后溶质质量
配制10%的硫酸溶液98g,需要98%的浓硫酸(密度为1.84g/mL)的体积是多少?
解:设需要98%的浓硫酸的体积为V。
V×1.84g/mL×98%=98g×10%
答:需要98%的浓硫酸的体积为5.4mL。
【例题3】40g10%NaOH溶液跟多少克10%盐酸完全反应?反应后溶液的溶质的质量分数是多少?
解:设稀盐酸的质量为X,生成的NaCl的质量为Y
NaOH + HCl = NaCl + H2O
40g×10% X ×10% Y
40 36.5 58.5
有关溶质的质量分数与化学方程式相结合的计算
解该类题时,一定要正确写出该反应的化学方程式。
有溶液参与的反应,只是溶液中的溶质参与了反应。
反应后溶液的质量=反应前的总质量-生成气体的质量- 生成沉淀的质量-不溶物的质量。
溶质的质量分数与化学方程式的综合计算
100g某硫酸恰好与13g锌完全反应。试计算这种硫酸中溶质的质量分数。
解:设硫酸中溶质的质量为X
Zn + H2SO4 = ZnSO4 + H2↑
65 98
13g X
答:这种硫酸溶液中溶质的质量分数为19.6%。
实验演示——配制50g溶质质量分数为6%的氯化钠溶液
计算:配制50g溶质质量分数为6%的氯化钠溶液,需要氯化钠 g;水 g。
称量:用天平称量所需的氯化钠,放入烧杯中;
溶解:用玻璃棒搅拌,使氯化钠溶解。
量取:用量筒量取所需的水(水的密度近似看做1g/cm3),倒入盛有氯化钠的烧杯中。
实验室中配制一定溶质质量分数的溶液
思考:1.配置一定溶质质量分数的溶液需要用到哪些仪器?2.若所配溶液的溶质质量分数偏大或偏小,你认为可能的原因有哪些?
1.溶液浓度的定量表示方法:2.有关溶质质量分数的计算
③有关溶液稀释或浓缩的计算依据是稀释或浓缩前后溶质的质量不变。
④有关化学方程式的计算中,溶液的质量不能直接代入化学方程式中计算,必须换算成溶质的质量。
②某温度下饱和溶液的溶质质量分数=
3.实验室中配制一定溶质质量分数溶液:计算→称量→量取→溶解→装瓶贴签。
①溶质质量分数的简单计算
1.对5%的食盐溶液含义的解释错误的是( )A.100克水中溶解了5克食盐 B.100克食盐溶液中含有5克食盐C.将5克食盐溶于95克水中所得溶液D.该溶液中溶质与溶液的质量比为1∶20
2.配制质量分数为20%的某盐溶液,需向100 g水中所加盐的质量是( )A.20克 B.25克 C.10克 D.40克3.从1升10%的硫酸溶液中取出100毫升这种溶液,则100毫升硫酸溶液中溶质的质量分数为( )A.1% B.10% C.11.1% D.9%
4.从溶质的质量分数为20%的某溶液中,倒出其体积的3/4后,再加水至原来的体积,然后再倒出其体积的2/3,最后剩余溶液中溶质的质量分数为( )A.3% B.4% C.5% D.6%
5.在一定温度下的饱和食盐水里加入少量的硝酸钾晶体,则( )①硝酸钾晶体不溶 ②硝酸钾晶体溶解 ③溶液中食盐的质量分数不变 ④溶液中食盐的质量分数减小 ⑤溶液中食盐的质量分数增大A.①③ B.②③ C.②④ D.②⑤
化学九年级下册课题3 溶液的浓度多媒体教学ppt课件: 这是一份化学九年级下册课题3 溶液的浓度多媒体教学ppt课件,共6页。PPT课件主要包含了实验9-5,回答并分析问题,溶质的质量分数,计算式,计算式变形,溶液稀释的计算,245g,V2211mL,请同学小结计算公式,第二课时等内容,欢迎下载使用。
化学九年级下册课题3 溶液的浓度课文配套ppt课件: 这是一份化学九年级下册课题3 溶液的浓度课文配套ppt课件,共15页。PPT课件主要包含了质量单位要统一,议一议,氯化钠,gX10%,g+2g,=9%,计算的依据,能力延伸等内容,欢迎下载使用。
初中化学人教版九年级下册课题3 溶液的浓度背景图课件ppt: 这是一份初中化学人教版九年级下册课题3 溶液的浓度背景图课件ppt,共13页。PPT课件主要包含了温故知新,实验回顾,托盘天平,ml量筒,玻璃棒,装瓶存放,火眼金星,板书设计,无影响,想想议一议等内容,欢迎下载使用。













