




高中化学第三节 醛酮精品ppt课件
展开这种原子团叫羰基,如在其一端连接一个氢原子就形成了
醛基(-CHO)与烃基(或氢原子)相连构成的一类化合物就叫醛,可用通式RCHO表示。
从结构上看,由烃基(或氢原子)跟醛基(-CHO)相连而成的化合物叫醛。
3、饱和一元醛的通式:
CnH2nO 或 CnH2n+1CHO
甲醛 乙醛
①醛基的个数:一元醛、二元醛、多元醛
②烃基的种类:脂肪醛、脂环醛、芳香醛
③烃基是否饱和:饱和醛、不饱和醛
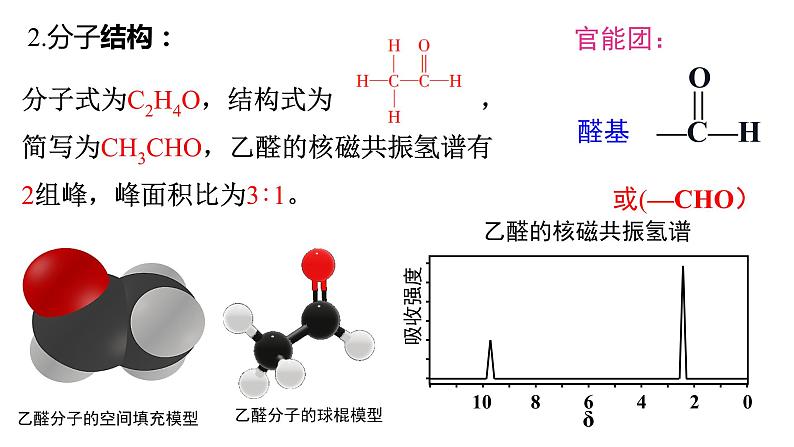
分子式为C2H4O,结构式为 ,简写为CH3CHO,乙醛的核磁共振氢谱有2组峰,峰面积比为3∶1。
①催化加氢又称为还原反应,化学方程式为
乙醛能和一些极性试剂发生加成反应,例如与氢氰酸加成:
通常能与碳氧双键加成:H2、HCN能与碳碳双键加成:H2、X2、HX、H2O
醛基与极性分子加成时,极性分子中带正电荷的原子或原子团连接在醛基的氧原子上,带负电荷的原子或原子团连接在碳原子上。
试管内壁出现光亮的银镜
取1 mL 2%的AgNO3溶液于洁净试管中,一边振荡试管,一边逐滴滴入2%的稀氨水,至生成的沉淀恰好完全溶解,制得银氨溶液。
AgNO3+NH3·H2O=AgOH↓+NH4NO3
AgOH+2NH3·H2O=Ag(NH3)2OH+2H2O
①试管内壁必须光滑、洁净;
②实验的银氨溶液应现配现用;氨水不能太浓
③必须用水浴加热,不可用酒精灯直接加热;
④加热时不能振荡和摇动试管。
实验后附着的银镜的试管如何洗净?
可用稀硝酸浸泡,再用水洗除去。
②与新制的Cu(OH)2(又叫菲林试剂)反应
a、必须用新制的Cu(OH)2:
一方面,新制的Cu(OH)2为絮状物,跟醛的接触面积大
另一方面,久置的Cu(OH)2,易转变成Cu2(OH)2CO3
b、制备Cu(OH)2时,NaOH必须过量,且质量分数要大些,这样形成的Cu(OH)2能加快乙醛的氧化使现象明显
c、该反应必须加热到沸腾,才有明显的红色沉淀产生,但不能太久,否则会有黑色的沉淀CuO生成
d、用途:检验醛基,医疗上检测尿糖
已知银氨溶液和新制的氢氧化铜属于弱氧化剂,思考乙醛能不能使酸性高锰酸钾溶液褪色?提示:酸性高锰酸钾溶液属于强氧化剂,故乙醛能使酸性高锰酸钾溶液褪色。
(2)氧化反应:体现乙醛的还原性
(2)被强氧化剂氧化:
遇到酸性高锰酸钾溶液和溴水使其褪色
注:必须是溴水,溴的CCl4溶液不会氧化醛基,因为其中不含氧
(3)催化氧化(加氧):
(4)被弱氧化剂氧化:
CH3CHO+2Ag(NH3)2OH 2Ag↓+CH3COONH4+3NH3+H2O
②与新制的Cu(OH)2反应:
CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
RCH2OH RCHO RCOOH
自然界的许多植物中都含有醛,其中有些具有特殊的香味,可作为植物香料使用。
桂皮和杏仁中分别含有肉桂醛和苯甲醛
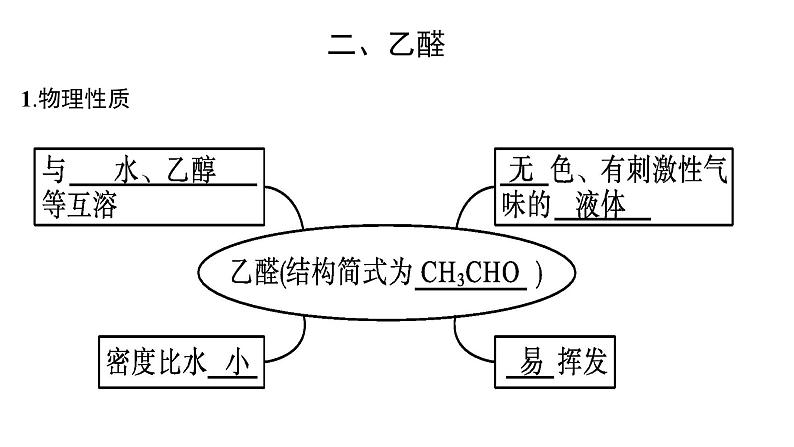
三、醛类物质的物理性质
1、熔沸点随碳原子数增多而变大,随支链增多而减小。密度随碳原子数增多而逐渐变大;
2、随着碳原子数的增多,在水中的溶解度逐渐减小,低级醛易溶于水(CH3CHO、HCHO)
3、 除了甲醛是气体,其他的醛常温下是液体或者固体,有一定气味(或刺激性气味)。
四、醛类物质的化学性质
1、加成反应(还原反应):与H2、HCN反应;
(2)被高锰酸钾、溴水等强氧化剂氧化
(3)被银氨溶液、新制氢氧化铜等若氧化剂氧化
俗名蚁醛,最简单的醛类物质,是一种无色、有强烈刺激性气味的气体,易溶于水,质量分数为35%~40%的水溶液叫做福尔马林,具有防腐和杀菌能力,常作防腐杀菌剂(消毒、浸制标本);制药(农药、消毒剂),香料,染料;制造酚醛树脂、脲醛树脂、维纶等。
五、常见醛——甲醛、丙醛、苯甲醛
结构:
①、常温下甲醛为无色有刺激性气味的气体。②、甲醛中有2个活泼氢可被氧化。
1ml甲醛最多可以还原得到多少mlAg?
从结构: H—C—H 分析
(注意:相当于含有两个醛基的特殊结构)
②被新制Cu(OH)2碱性悬浊液氧化
苯甲醛是最简单的芳香醛,俗称苦杏仁油,是一种有苦杏仁气味的无色液体
杏仁中含有苯甲醛,苯甲醛是制造染料、香料及药物的重要原料。
①加成反应(还原反应):与H2、HCN反应;
II、被高锰酸钾、溴水等强氧化剂氧化
III、被银氨溶液、新制氢氧化铜等若氧化剂氧化
(2)桂皮中含有肉桂醛。肉桂醛的化学性质主要体现在醛基上
醛类的两个特征反应及—CHO的检验
含醛基物质中碳碳双键的检验方法
(1)醛基和碳碳双键性质的比较
(2)含醛基物质中碳碳双键的检验流程
易错警示 (1)能发生银镜反应的物质不一定是醛类,也可以是甲酸、甲酸酯和葡萄糖等。(2)配制银氨溶液是向AgNO3稀溶液中逐滴加稀氨水,直到最初生成的沉淀恰好溶解为止,顺序不能颠倒。(3)银镜反应、与新制的氢氧化铜的反应都必须在碱性条件下进行,若溶液呈酸性,必须先用氢氧化钠溶液中和至碱性。
b 被弱氧化剂氧化(银氨溶液、新制的Cu(OH)2)
c 使酸性高锰酸钾溶液、溴水褪色
1.下列物质中不属于醛类的是( )③CH2=CH—CHO ④Cl—CH2—CHOA.①③ B.②④ C.②③ D.①④
解析:①属于醛类,②属于酯类,③属于醛类,④中含有氯元素,不属于醛类。
2.下列有关说法正确的是( )A.醛一定含醛基,含有醛基的物质一定是醛B.丙醛只有丙酮一种同分异构体C.醛类物质在常温常压下都为液体或固体D.含醛基的物质在一定条件下可与H2发生还原反应解析:醛的官能团是醛基,但含醛基的物质不一定是醛,A项错误;丙醛的同分异构体除 外,还有CH2=CH—CH2OH等,B项错误;常温常压下,甲醛为气体,C项错误;醛基能被H2还原为醇羟基,D项正确。
3.下列说法中,正确的是( )A.乙醛与苯甲醛互为同系物B.苯乙醛的结构简式:C.醛类既能被氧化为羧酸,又能被还原为醇D.完全燃烧等物质的量的乙醛和乙醇,消耗氧气的质量相等解析:乙醛、苯甲醛都属于醛,但结构不相似,不互为同系物,A项错;醛基应写成—CHO而不可写成—COH,B项错;完全燃烧1 ml乙醛、乙醇消耗氧气的物质的量分别为2.5 ml、3 ml,则质量不相等,D项错。
4.某学生做乙醛还原性的实验,取1 ml·L-1的硫酸铜溶液2 mL和0.4 ml·L-1的氢氧化钠溶液4 mL,在一个试管中混合后加入0.5 mL 40%的乙醛溶液加热至沸腾,无砖红色沉淀,实验失败的原因是( )A.氢氧化钠的量不够B.硫酸铜的量不够C.乙醛溶液太少D.加热时间不够解析:该实验成功的关键之一是NaOH必须过量,而本次实验中所加的NaOH还不足以使CuSO4完全沉淀为Cu(OH)2。
5.(1)做乙醛被新制的氢氧化铜氧化的实验时,下列各步操作中:①振荡后加入0.5 mL乙醛溶液;②加入10%的氢氧化钠溶液2 mL;③加入5%的CuSO4溶液4~5滴;④加热试管。正确的顺序是 。 (2)实验室配制少量银氨溶液的方法是:先向试管中加入 ,然后 ,其反应的化学方程式为 、 ,向银氨溶液中滴加少量的乙醛, ,片刻即可在试管内壁形成银镜,化学方程式为 。
解析(1)做该实验时,应将少量CuSO4溶液滴入NaOH溶液中得新制的Cu(OH)2,然后 加入乙醛溶液,并用酒精灯加热至沸腾,即可产生砖红色Cu2O沉淀。(2)要熟悉银氨溶液的配制及所发生的反应。
5.有机化合物A在一定条件下可发生以下转化:其中B可发生银镜反应,C跟石灰石反应产生能使澄清石灰水变浑浊的气体。(1)A、B、C的结构简式和名称依次是 、 、 。 (2)写出下列反应的化学方程式:①A→B的化学方程式为 ; ②B→C的化学方程式为 ; ③B→A的化学方程式为 。
高中第3节 醛和酮 糖类和核酸教学ppt课件: 这是一份高中<a href="/hx/tb_c4002623_t3/?tag_id=26" target="_blank">第3节 醛和酮 糖类和核酸教学ppt课件</a>,文件包含新教材精创231常见的醛酮醛酮的化学性质课件鲁科版选择性必修3共24页PPTpptx、新教材精创231常见的醛酮醛酮的化学性质教学设计鲁科版选择性必修3docx、新教材精创231常见的醛酮醛酮的化学性质学案鲁科版选择性必修3docx等3份课件配套教学资源,其中PPT共24页, 欢迎下载使用。
高中化学人教版 (2019)选择性必修3第三节 醛酮优秀课件ppt: 这是一份高中化学人教版 (2019)选择性必修3第三节 醛酮优秀课件ppt,共83页。PPT课件主要包含了CH3CHO,第一部分醛的结构,醛的结构,结构简式,官能团,-CHO,HCHO,苯甲醛,烃基或H原子,RCHO等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修3第三节 醛酮优秀课件ppt: 这是一份高中化学人教版 (2019)选择性必修3第三节 醛酮优秀课件ppt,共60页。PPT课件主要包含了新课导入,第三节醛酮,第三章,新知讲解,官能团,表示方法,简写为RCHO,醛基碳的杂化类型,⒈物理性质,⒉分子结构等内容,欢迎下载使用。












