




苏教版 (2019)选择性必修1第三单元 化学平衡的移动教课课件ppt
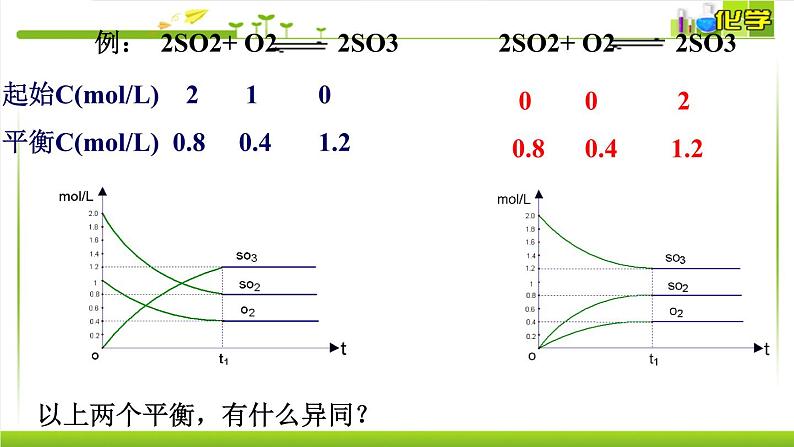
展开起始C(ml/L) 2 1 0平衡C(ml/L) 0.8 0.4 1.2
0 0 2 0.8 0.4 1.2
以上两个平衡,有什么异同?
在一定条件下(恒温恒容或恒温恒压),对同一可逆反应,只是起始时加入物质的物质的量不同,而达到化学平衡时,同种物质的百分含量相同,这样的平衡称为等效平衡。
质量分数、体积分数、物质的量分数等
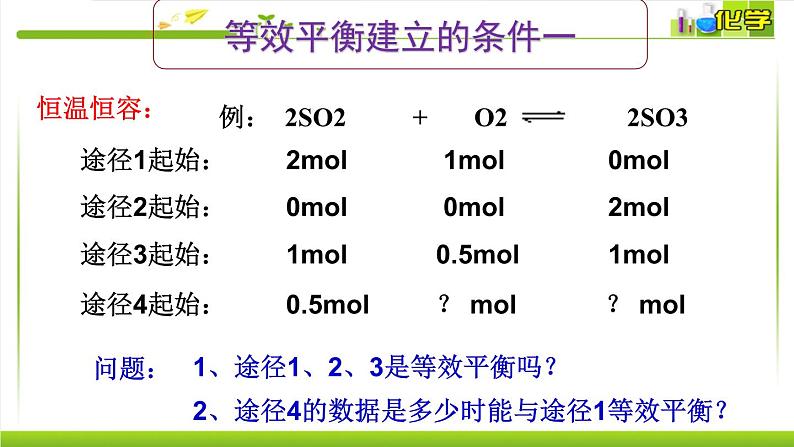
途径1起始: 2ml 1ml 0ml
途径2起始: 0ml 0ml 2ml
途径3起始: 1ml 0.5ml 1ml
途径4起始: 0.5ml ? ml ? ml
问题:
1、途径1、2、3是等效平衡吗?
2、途径4的数据是多少时能与途径1等效平衡?
恒温恒容条件,建立等效平衡的条件:
把不同的起始状态,通过化学方程式中的计量数,换算成同一边物质(反应物一边或生成物一边),如果各反应物或生成物的物质的量相等,则是等效平衡。
一边倒后,料相同,则等效
(2+2)mlA+(1+1)mlB
途径1起始: 2ml 1ml 0ml
途径2起始: 4ml 2ml 0ml
途径3起始: 3ml 1ml 2ml
2、途径2、3与途径1中体积分数、质量分数相同吗?各物质n相同吗?C相同吗?
体积分数相同质量分数相同, n不同 C不同。
途径2起始: 4ml 2ml 0ml
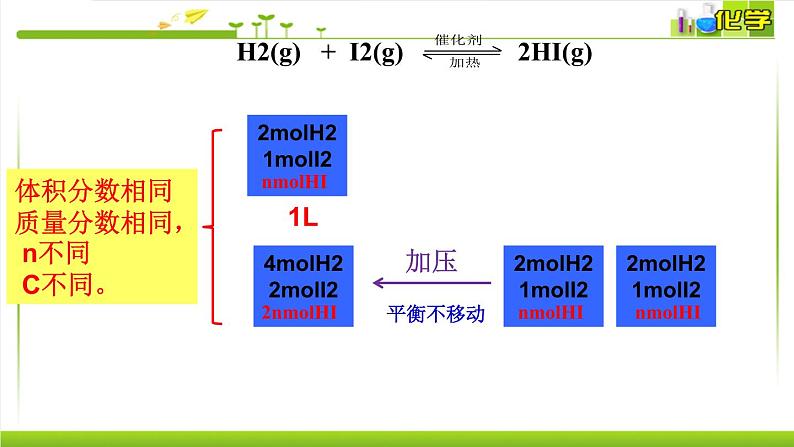
思考:按以下方式投料,是否会建立等效平衡呢?
2mlSO21mlO2
4mlSO22mlO2
恒温恒容条件下(△n(g)=0)反应中,建立等效平衡的条件:
把不同的起始状态,通过化学方程式中的计量数,换算成同一边物质(反应物一边或生成物一边),如果各反应物或生成物的物质的量之比相等,则是等效平衡。
例2 在固定体积的密闭容器内,加入2ml A、1ml B,发生反应: A(g)+B(g) 2C(g)达 到平衡时,C的质量分数为W%。在相同(T、V)条件下,按下列情况充入物质达到平衡时C的质量分数仍为W%的是 A.2ml C B.3ml C C.4ml A、2ml B D.1ml A、2ml C
途径1起始: 2ml 1ml 0ml
途径2起始: 4ml 2ml 0ml
问题:1、途径1、2是等效平衡吗?
2、途径2与途径1中体积分数、质量分数相同吗?各物质n相同吗?C相同吗?
2mlSO2 1ml O2
4mlSO2 2ml O2
体积分数相同质量分数相同, C相同n不同
恒温恒压条件,所有可逆反应,建立等效平衡的条件:
例3 在一个盛有催化剂容积可变的密闭容器中,保持一定的温度和压强,进行以下反应:N2+3H2 2NH3。已知加入1mlN2和4ml H2时,达到平衡后生成amlNH3。在恒温恒压下欲保持平衡时各组分的体积分数不变。填写下列空白:
人教版 (2019)选择性必修1实验活动1 探究影响化学平衡移动的因素教案配套ppt课件: 这是一份人教版 (2019)选择性必修1<a href="/hx/tb_c4002423_t3/?tag_id=26" target="_blank">实验活动1 探究影响化学平衡移动的因素教案配套ppt课件</a>,共19页。PPT课件主要包含了①②③,①②③④,解题方法,2aL,6aL等内容,欢迎下载使用。
高中化学苏教版 (2019)选择性必修1第三单元 化学平衡的移动获奖ppt课件: 这是一份高中化学苏教版 (2019)选择性必修1第三单元 化学平衡的移动获奖ppt课件,共14页。PPT课件主要包含了等效平衡的概念,随堂训练1,随堂训练2,随堂训练3,习题研究,作业布置等内容,欢迎下载使用。
化学第二节 化学平衡课文配套课件ppt: 这是一份化学第二节 化学平衡课文配套课件ppt,共30页。PPT课件主要包含了等效平衡,等效平衡的含义,等效平衡的标志,恒温恒容条件下,等效平衡的分类,4与1等效,一边倒后比相同则等效,此为放缩法,处理方法,物质的量等内容,欢迎下载使用。













