




高中化学苏教版 (2019)选择性必修1专题2 化学反应速率与化学平衡第二单元 化学反应的方向与限度图文ppt课件
展开1.定义:在同一条件下,既可以向正反应方向进行,同时又可以向逆反应方向进行的反应
③可逆反应有一定的限度。
①正反应和逆反应发生的条件相同;
②反应物、生成物共同存在;(反应不彻底)
平衡时:C反、C生不再变化, 达到了平衡状态,v正=v逆≠0
反应开始时:C反最大, v正最大;
反应进行过程中:C反↓, v正↓;
C生=0 , v逆=0
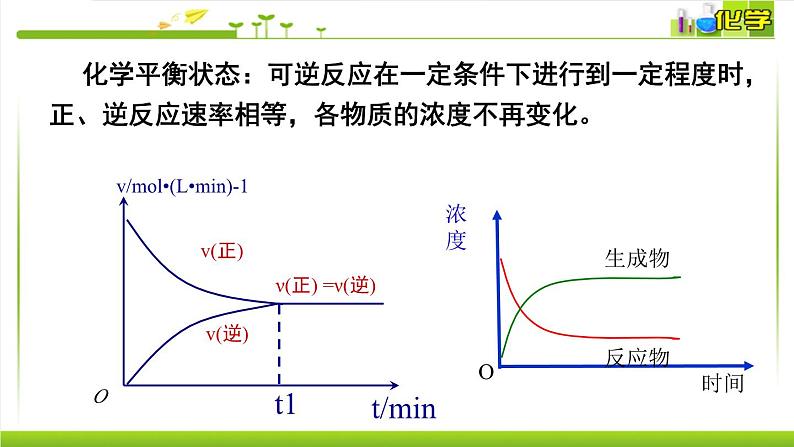
化学平衡状态:可逆反应在一定条件下进行到一定程度时,正、逆反应速率相等,各物质的浓度不再变化。
v/ml•(L•min)-1
(4)“定”:平衡时反应物和生成物浓度保持不变。
(1)“逆”:可逆反应才有化学平衡状态。
(3)“动”:化学平衡是一个动态平衡。
(2)“等”:平衡时, v(正)=v(逆) 且大于0。
(5)“变”:改变外界条件时,平衡会发生移动 (旧的平衡被破坏,并在新的条件下建立新的平衡)。
四.化学平衡的判断依据
(1) v(正)=v(逆)
(2) 反应混合物中各组分的浓度保持不变。
可逆反应在一定条件下进行到一定程度时,正、逆反应速率相等,各物质的浓度不再变化。
①同种物质: vA(正)=vA(逆)
②不同物质: vA(正)与vB(逆)之比等于它们系数之比
各组分n、m、物质的量分数、质量分数、体积分数
关键:正逆相等,变量不变
①转化率不变:(转化量/起始量)×100%
③温度:任何化学反应都伴随着能量变化,体系温度不变时,达到平衡
3、不同反应平衡状态的判定
N2(g)+3H2(g) ⇌ 2NH3(g)
反应特点:纯气体反应,反应前后气体的物质的量改变
恒量不变不能说明达到平衡
H2(g)+I2(g)⇌2HI(g)
反应特点:纯气体反应,反应前后气体的物质的量不变
它们均不能说明达到平衡
C(s)+CO2(g) ⇌ 2CO(g)
反应特点:有固体(或液体)参与或生产的反应,反应前后气体的物质的量改变
它们不变均能说明反应达到了平衡
Fe2O3(s)+ 3CO(g) ⇌ 2Fe(s)+3CO2(g)
反应特点:有固体(或液体)参与或生产的反应,反应前后气体的物质的量不变
高中化学苏教版 (2019)选择性必修1第二单元 化学反应的方向与限度试讲课课件ppt: 这是一份高中化学苏教版 (2019)选择性必修1第二单元 化学反应的方向与限度试讲课课件ppt,共29页。PPT课件主要包含了总结归纳,习题研究,作业布置等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修1第二节 化学平衡获奖课件ppt: 这是一份高中化学人教版 (2019)选择性必修1第二节 化学平衡获奖课件ppt,文件包含221化学平衡状态化学平衡常数练习解析版docx、221化学平衡状态化学平衡常数练习原卷版docx等2份课件配套教学资源,其中PPT共0页, 欢迎下载使用。
人教版 (2019)选择性必修1第二节 化学平衡获奖课件ppt: 这是一份人教版 (2019)选择性必修1第二节 化学平衡获奖课件ppt,文件包含人教版高中化学选择性必修一221《化学平衡状态化学平衡常数》课件pptx、人教版高中化学选择性必修一221《化学平衡状态化学平衡常数》学案docx等2份课件配套教学资源,其中PPT共40页, 欢迎下载使用。













