





化学选择性必修1第四单元 沉淀溶解平衡说课ppt课件
展开据有关资料介绍,全国目前有近40万余台锅炉,在每年的事故统计中,因水质不良、水垢严重引起的事故超过事故数的20%。由于结生水垢,每年要浪费燃料达千万吨,并造成了几亿元的经济损失。
锅炉的水垢的主要成分CaCO3、Mg(OH)2和CaSO4,用酸可以除去CaCO3、Mg(OH)2 , CaSO4怎么除去呢?
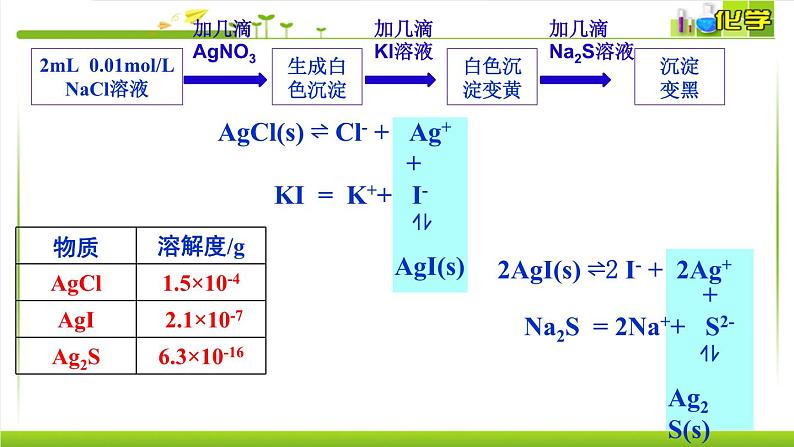
2mL 0.01ml/LNaCl溶液
AgCl(s) ⇌ Cl- + Ag+
+KI = K++ I-
2AgI(s) ⇌2 I- + 2Ag+
+Na2S = 2Na++ S2-
1.实质:沉淀溶解平衡的移动
①一般溶解能力相对较强的物质易转化为溶解能力相对较弱的物质 。
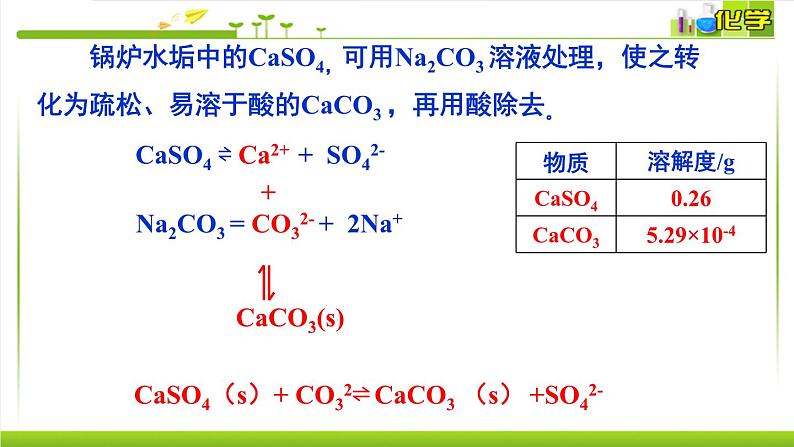
CaSO4 ⇌ Ca2+ + SO42-
CaSO4(s)+ CO32⇌ CaCO3 (s) +SO42-
Na2CO3 = CO32- + 2Na+
锅炉水垢中的CaSO4,可用Na2CO3 溶液处理,使之转化为疏松、易溶于酸的CaCO3 ,再用酸除去。
例如:重晶石BaSO4转化为易溶于酸的BaCO3 。
②在某些特殊情况下,控制反应条件,也能使溶解能力相对较弱的物质转化为溶解能力相对较强的物质 。
BaSO4 ⇌ Ba2+ + SO42-
BaSO4(s)+ CO32⇌ BaCO3 (s) +SO42-
BaSO4 、BaCO3
1. 牙釉质:主要成分为Ca5(PO4)3OH(羟基磷灰石);是一种难溶电解质。 2. 残留在牙齿上的糖发酵会产生H+。
Ca5(PO4)3OH(s) ⇌5Ca2++ 3PO43- + OH-
Ca5(PO4)3OH(s)+F- ⇌ Ca5(PO4)3F(s) + OH-
含氟牙膏中的氟离子会与 Ca5(PO4)3OH 反应生成Ca5(PO4)3F (氟磷灰石) 。
1.工业废水中除去Cu2+、Hg2+等重金属离子,应使生成沉淀溶解度越小越好,一般选择Na2S做沉淀剂。
KSP(MnS)=2.5×10-13ml2·L-2KSP(FeS)=6.3×10-18 ml2·L-2KSP(CuS)=1.3×10-36 ml2·L-2KSP(HgS)=6.4×10-53 ml2·L-2
2.沉淀剂在沉淀杂质离子时,不影响其他离子的存在。
常温下,Cu2+/Sn4+混合液中c(Cu2+)=0.022ml·L-1, 若将Sn4+完全沉淀,调节溶液的pH范围为_______。(当溶液中的离子浓度小于10-5ml·L-1时,沉淀完全,已知:Ksp[Sn(OH)4]=1×10-55;Ksp[Cu(OH)2]=2.2×10-20)
思考: ①Sn4+完全沉淀时PH怎样计算? ②PH等于多少时Cu2+开始沉淀
则c(H+)=1×10-1.5ml·L-1,pH=1.5
则c(H+)=1×10-5ml·L-1,pH=5
高中化学人教版 (2019)选择性必修1第四节 沉淀溶解平衡说课ppt课件: 这是一份高中化学人教版 (2019)选择性必修1第四节 沉淀溶解平衡说课ppt课件,共18页。
高中化学苏教版 (2019)选择性必修1第四单元 沉淀溶解平衡优秀课件ppt: 这是一份高中化学苏教版 (2019)选择性必修1第四单元 沉淀溶解平衡优秀课件ppt,共21页。PPT课件主要包含了核心素养发展目标,了解沉淀的转化,学习目标,课前导入,交流讨论,沉淀的生成,随堂反馈,实验探究一,沉淀的转化,原理解释等内容,欢迎下载使用。
化学选择性必修1第四节 沉淀溶解平衡完美版ppt课件: 这是一份化学选择性必修1第四节 沉淀溶解平衡完美版ppt课件,文件包含新人教版化学选择性必修一342沉淀溶解平衡的应用课件pptx、新人教版化学选择性必修一342沉淀溶解平衡的应用针对练习含解析docx、新人教版化学选择性必修一342沉淀溶解平衡的应用教案doc等3份课件配套教学资源,其中PPT共27页, 欢迎下载使用。













