



高中化学人教版 (新课标)选修5 有机化学基础第二节 醛教课内容课件ppt
展开1.能记住乙醛的组成、结构、性质和用途,能说出甲醛、苯甲醛的性质和用途。2.记住醛的结构特点,会运用醛的性质。3.通过实验进一步训练操作技能、体会实验对认识和研究物质性质的重要作用。
一、醛类1.官能团醛基(—CHO)。2.通式饱和一元醛为CnH2nO(n≥1)或CnH2n+1CHO(n≥0)。3.物理性质递变规律随分子中碳原子数目增多,醛类物质的熔沸点逐渐升高,水溶性逐渐降低。
是不是分子组成为CnH2nO(n≥1)的有机物都属于饱和一元醛?提示:不一定。根据分子中的C、H原子个数比为1∶2可知,该分子可以是含双键的链状有机物,也可以是环状有机物,如分子式为C2H4O的有机物,可能为乙醛(CH3CHO),也可能为乙烯醇(CH2 CHOH),还可能为环氧乙烷( )。
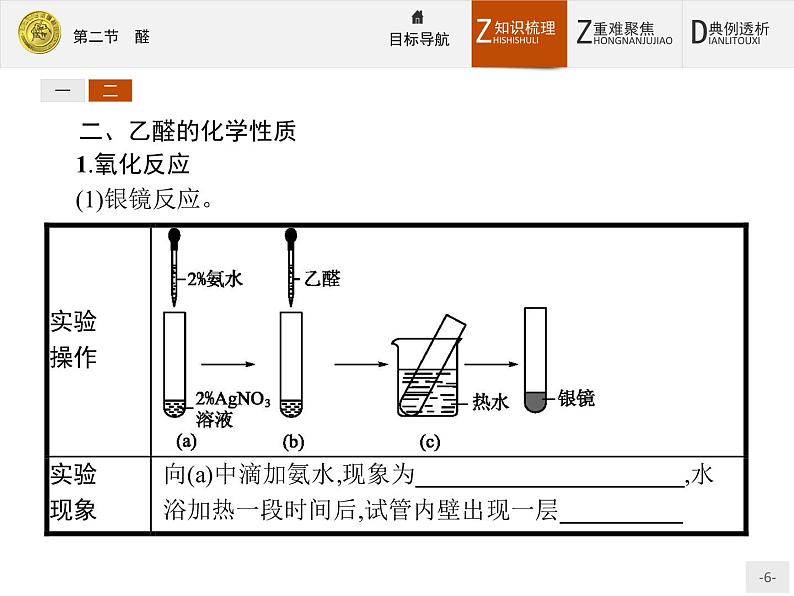
二、乙醛的化学性质1.氧化反应(1)银镜反应。
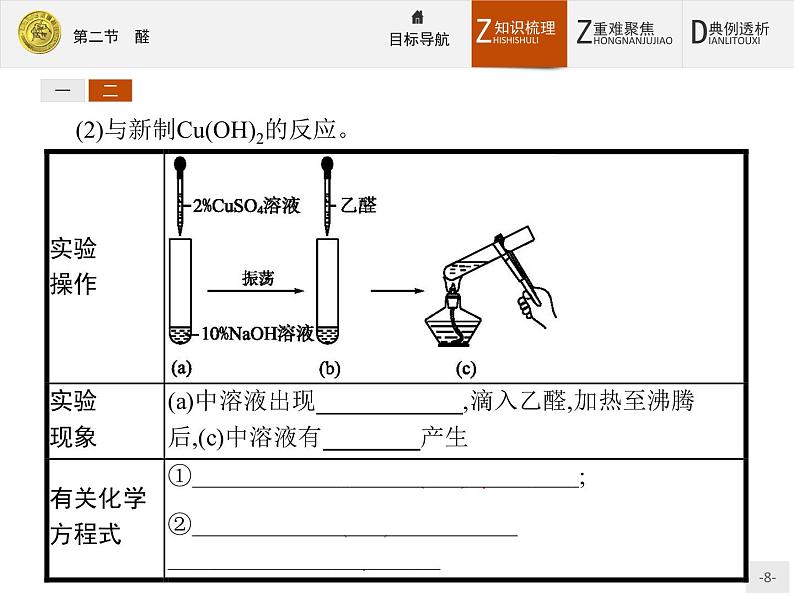
(2)与新制Cu(OH)2的反应。
乙醛能使溴水或KMnO4酸性溶液褪色吗?为什么?提示:能。因为醛具有较强的还原性,能被Ag(NH3)2OH溶液或新制Cu(OH)2等弱氧化剂氧化。而溴水或KMnO4酸性溶液的氧化能力比Ag(NH3)2OH溶液、Cu(OH)2强得多,故溴水、KMnO4酸性溶液也能氧化乙醛,而自身被还原,从而使溶液褪色。
(3)催化氧化。乙醛在有催化剂并加热的条件下,能被氧气氧化为乙酸,反应的化学方程式为:2CH3CHO+O2 2CH3COOH。(4)燃烧反应方程式:2CH3CHO+5O2 4CO2+4H2O。2.加成反应乙醛蒸气和H2的混合气体通过热的镍催化剂,发生加成反应的化学方程式为:
一、醛基与醛的关系以及醛基的性质与检验1.醛基与醛的关系(1)醛基为醛类有机物的官能团,因此醛中一定含醛基,而含醛基结构的物质不一定是醛。(2)含醛基结构的物质主要有:①醛类;②甲酸;③甲酸盐;④甲酸某酯;⑤某些糖类,如葡萄糖、麦芽糖等;⑥其他含醛基结构的多官能团有机物。2.醛基的性质与检验(1)醛基的性质。醛基可被氧化剂氧化为羧基,也可被H2还原为醇羟基,因此既有还原性,又有氧化性,可用图示表示如下:
特别提醒醛类物质发生银镜反应或与新制Cu(OH)2反应均需在碱性条件下进行。
二、有机化学中的“氧化”“还原”反应1.有机物发生氧化反应、还原反应的判断方法
2.有机化学中常见的氧化反应、还原反应(1)氧化反应:①有机物的燃烧均为氧化反应;②烯烃的催化氧化(加氧,生成醛或酮)、使KMnO4酸性溶液褪色;③炔烃、苯的同系物使KMnO4酸性溶液褪色(如—CH3→—COOH,去2个氢,加2个氧);④醇→醛→羧酸。(2)具有还原性的基团主要有 、—C≡C—、—OH(醇、酚等)、—CHO等。常见的氧化剂有O2、O3、KMnO4酸性溶液、溴水、银氨溶液、新制Cu(OH)2等。(3)还原反应:①烯烃、炔烃等所有含碳碳不饱和键的物质的催化加氢;②醛、酮的催化加氢。
温馨提示(1)同一个有机反应,从不同的角度来分析,它可能属于不同的反应类型,如烯烃、炔烃、醛等与H2的反应,既属于加成反应又属于还原反应,醇变成烯烃的反应既属于(分子内)脱水反应又属于消去反应等。这种情况在有机化学中比较普遍,它启示我们要从多个角度去分析有机反应。(2)“A B C”这条连续氧化链是“醇→醛→羧酸(—CH2OH→—CHO→—COOH)”;“C A B”这条氧化还原链是“醇←醛→羧酸(—CH2OH ← —CHO→ —COOH)”的特征。
三、使溴的CCl4溶液、KMnO4酸性溶液褪色的有机物及褪色原因的比较
注:“√”代表能,“×”代表不能。
特别提醒直馏汽油、苯、CCl4、己烷等分别与溴水混合,能通过萃取作用使溴水中的溴进入非极性有机溶剂而被萃取,使溴水褪色,但属于物理变化。
知识点1 醛的性质及检验【例题1】 丙烯醛的结构简式为 。下列关于它性质的叙述中错误的是 ( )A.能使溴水褪色,也能使高锰酸钾酸性溶液褪色B.在一定条件下与H2充分反应,生成1-丙醇C.能发生银镜反应表现出氧化性D.在一定条件下能被空气氧化
解析:由于丙烯醛含有 ,又含有 ,所以它既有 的性质,也有醛的性质。①可与溴水发生加成反应;②可与高锰酸钾酸性溶液反应;③催化加H2生成饱和一元醇;④被O2氧化;⑤发生银镜反应等。A、B、D三项的叙述是正确的。丙烯醛在与Ag(NH3)2OH发生银镜反应时,表现出还原性,故选C项。答案:C点拨有机物分子中若含有多个官能团,判断其性质时,先全面分析各个官能团对应的性质,再进行归类整合。
知识点2 醛的有关计算【例题2】 某3 g醛与足量的银氨溶液反应,结果析出43.2 g Ag,则该醛为( )A.甲醛B.乙醛C.丙醛D.丁醛解析:因1 ml一元醛通常可以还原得到2 ml Ag,现得到0.4 ml Ag,故醛为0.2 ml,该醛的相对分子质量 但联想1 ml 甲醛可以得到4 ml Ag,3 g (0.1 ml)甲醛可得到43.2 g(0.4 ml)Ag,符合题意。答案:A
点拨通常一元醛与银氨溶液反应时,R—CHO+2Ag(NH3)2OH RCOONH4+2Ag↓+3NH3+H2O,但HCHO+4Ag(NH3)2OH 4Ag↓+6NH3+2H2O+(NH4)2CO3。故做此类题时,应把HCHO单独考虑,排除HCHO后,再用通式求算。
知识点3 有机化学中氧化还原反应的判断【例题3】 判断下列反应类型是氧化反应还是还原反应:
高中化学人教版 (2019)选择性必修3第三节 醛酮完美版ppt课件: 这是一份高中化学人教版 (2019)选择性必修3<a href="/hx/tb_c4002470_t3/?tag_id=26" target="_blank">第三节 醛酮完美版ppt课件</a>,共34页。PPT课件主要包含了CH3-C-H,+H-H,O-H等内容,欢迎下载使用。
高中人教版 (新课标)第二节 醛评课课件ppt: 这是一份高中人教版 (新课标)第二节 醛评课课件ppt,共36页。PPT课件主要包含了学习目标,乙醛的物理性质,乙醛的组成和结构,醛基上的氢,甲基上的氢,学与问,乙醛的化学性质,葡萄糖的结构式,二氧化反应,1配制银氨溶液等内容,欢迎下载使用。
高中化学人教版 (新课标)选修5 有机化学基础第二节 醛示范课ppt课件: 这是一份高中化学人教版 (新课标)选修5 有机化学基础第二节 醛示范课ppt课件,共31页。PPT课件主要包含了生活中的醛你知道吗,新知导入,杏仁含苯甲醛,桂皮含肉桂醛,结构式,结构简式,CHO,醛基和醛,常见的醛,官能团醛基等内容,欢迎下载使用。













