





高中鲁科版 (2019)第3节 饮食中的有机化合物课文内容课件ppt
展开1.比较活泼、容易发生反应并决定着某类有机化合物共同特性的原子或者原子团称为官能团。2.乙醇的官能团名称为羟基,乙醇不能与碳酸钙反应。3.乙醇属于烃的衍生物。
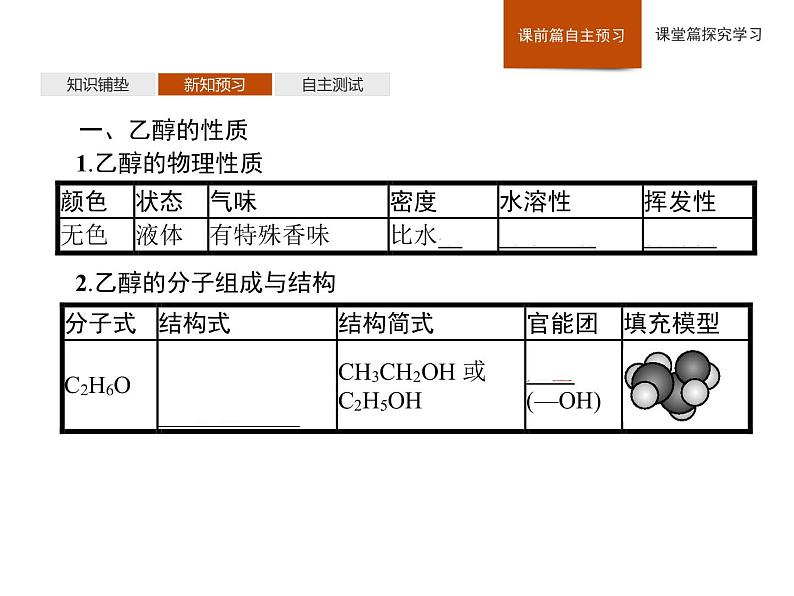
一、乙醇的性质1.乙醇的物理性质
2.乙醇的分子组成与结构
3.乙醇的化学性质(1)【实验1】乙醇的燃烧。
(2)【实验2】乙醇的催化氧化。
(3)【实验3】乙醇被强氧化剂氧化。
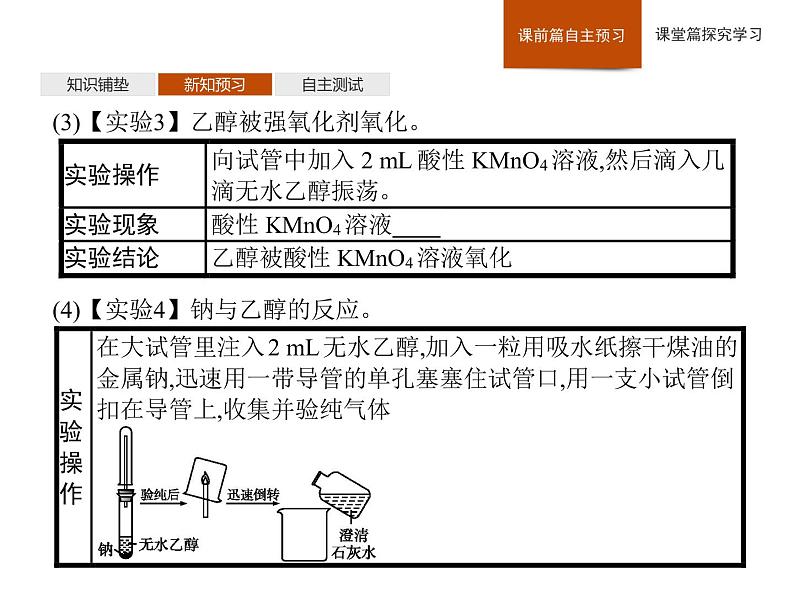
(4)【实验4】钠与乙醇的反应。
4.乙醇的用途(1)用作酒精灯、内燃机等的燃料。(2)用作化工原料。(3)医疗上常用体积分数为75%的乙醇溶液作消毒剂。
【微思考】如何检验乙醇中是否含水?提示:可通过向乙醇中加入无水硫酸铜(CuSO4)检验乙醇中是否含水,若无水硫酸铜变蓝,说明乙醇中有水,若无水硫酸铜不变色,则证明乙醇中不含水。
1.判断正误,正确的打“√”,错误的打“×”。(1)在相同状况下,相同体积的乙醇气体和乙烯气体都完全燃烧,耗氧量相同。 ( )(2)用乙醇作燃料会导致酸雨。 ( )(3)乙醇能发生脱水反应证明乙醇分子中有一个氢原子与另外氢原子不同。 ( )(4)相同物质的量的—OH和OH-含有相同的电子数。 ( )(5)乙醇燃烧,乙醇分子中所有的化学键都断裂。 ( )(6)医院里常用质量分数为75%的乙醇溶液进行杀菌、消毒。 ( )答案:(1)√ (2)× (3)× (4)× (5)√ (6)×
2.下列物质中可以使酸性高锰酸钾溶液褪色,但不能使溴水褪色的是( )A.甲烷B.乙烯C.乙醇D.苯答案:C解析:甲烷不与酸性高锰酸钾和溴水反应,乙烯能使酸性高锰酸钾和溴水都褪色,苯不与酸性高锰酸钾和溴水反应,乙醇能被酸性高锰酸钾溶液氧化,使其褪色,但不能与溴水反应。
乙醇的结构与化学性质问题探究为了探究乙醇和金属钠反应的产物,某同学做了以下实验。
1.简要描述实验现象。2.根据实验现象分析气体产物的成分。3.结合烷烃的性质分析,生成的气体产物与乙醇分子中的哪部分结构相关。
提示:1.放出的气体在空气中安静地燃烧,火焰呈淡蓝色。澄清石灰水无明显现象。2.根据实验现象和元素组成分析生成的气体应该是氢气。3.烷烃不能与金属钠发生反应,因此生成的氢气中的氢原子应该来自羟基氢。
知识归纳(1)钠与水、乙醇反应的比较:
(2)乙醇与金属钠反应:①在乙醇分子里,被钠置换的氢是羟基中的氢,而不是乙基上的氢。可以依据产生氢气的量来判断醇分子中羟基的数目。②除了Na外,K、Ca、Mg等活泼的金属也能置换乙醇分子中羟基中的氢原子而生成H2,如2CH3CH2OH+Ca (CH3CH2O)2Ca+H2↑。
(1)实验前检验该装置的气密性的实验操作是 。 (2)有人认为上述装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为 (填“正确”或“不正确”)。 (3)如果实验开始前b导管内未充满水,则实验结果将 (填“偏大”或“偏小”)。 (4)若测得有1.15 g C2H6O参加反应,把量筒c中的水的体积换算成标准状况下H2的体积为280 mL,结合计算和讨论得出下列结构式 (填“①”或“②”)正确。
答案:(1)连接好装置,关闭分液漏斗的活塞,将右侧导管插入水槽,微热烧瓶,右侧导管口若有气泡冒出,冷却后形成一段水柱,且一段时间内水柱不变化,证明装置气密性良好(2)不正确 (3)偏小 (4)②解析:该实验的关键是准确测量反应产生气体的体积,根据产生气体的体积可以确定被置换的氢原子的个数。(3)中如果实验开始前b导管内未充满水,则会使排出水的体积减小,故实验结果偏小。(4)根据题意计算可得参加反应的乙醇的物质的量是0.025 ml,生成氢气的物质的量是0.012 5 ml,即乙醇分子中的6个氢原子所处的化学环境并不完全相同,有1个氢原子不同于其他的氢原子,从而确定乙醇的结构式为②中所示。
变式训练1下列有关金属钠在水中和在乙醇中的反应情况对比正确的是( )A.钠能置换出水中所有的氢,却只能置换出乙醇里羟基中的氢B.钠都要浮在水面上或乙醇液面上C.钠无论与水反应还是与乙醇反应都要放出热量D.钠在乙醇中反应更剧烈,是因为乙醇分子中含有的氢原子比水分子中的多答案:C解析:钠和水反应生成氢氧化钠和氢气,则不能置换出水中所有的氢,故A错误;钠的密度比水小,比乙醇大,故B错误;钠与水、乙醇的反应都为放热反应,故C正确;钠与水反应较钠与乙醇反应更为剧烈,故D错误。
乙醇的催化氧化反应问题探究如图所示为反应中乙醇分子中可能断裂的化学键。
在乙醇和金属钠的反应和乙醇的燃烧反应中,上图中的哪些化学键分别发生断裂?指出乙醇与氧气在铜作催化剂时发生反应断键的位置。
提示:乙醇反应时断键情况
知识归纳乙醇催化氧化的机理(1)反应条件。加热条件下,用金属铜或银作催化剂。(2)反应历程。
(3)反应实质。乙醇分子脱去羟基中的氢原子以及与羟基直接相连的碳原子上的氢原子形成碳氧双键,脱下的氢原子与CuO中的氧原子结合生成H2O,使CuO重新变成Cu。该反应中,乙醇被催化氧化。有机物的氧化反应常见类型:①燃烧;②醇的催化氧化;③被酸性高锰酸钾溶液氧化,如乙烯被酸性高锰酸钾溶液氧化。有机物发生氧化反应时,通常表现为去氢(分子中的氢原子减少)和得氧(分子中的氧原子增多)两种形式。
典例剖析例2如图所示为某化学兴趣小组设计的乙醇催化氧化及其产物检验的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。
图中A为无水乙醇(沸点为78 ℃),B为绕成螺旋状的细铜丝或银丝,C为无水CuSO4粉末,D为碱石灰,F为新制的碱性Cu(OH)2悬浊液。已知乙醛能与新制Cu(OH)2在加热条件下反应生成砖红色沉淀。
(1)在上述装置中,实验时需要加热的仪器为(填仪器或某部位的代号) 。 (2)为使A中乙醇平稳汽化成乙醇蒸气,常采用的方法是 ,D处使用碱石灰的作用是 。 (3)检验乙醇氧化产物时F中的实验现象是 。 (4)E处是一种纯净物,其反应方程式为 。 (5)写出乙醇发生催化氧化的化学方程式 。
答案:(1)E、A、B、F(2)水浴加热 防止F中的水蒸气进入C中与无水CuSO4作用,影响产物水的检验(3)产生砖红色沉淀
解析:(1)固体加热制氧气需要加热,乙醇变为蒸汽需加热,乙醇的催化氧化要加热,乙醛和氧气的反应也要加热。(2)为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是水浴加热;碱石灰具有吸水作用,D处使用碱石灰可以防止F中的水蒸气进入C中与无水CuSO4作用,否则会影响产物水的检验。(3)乙醛能和新制氢氧化铜在加热条件下反应生成砖红色沉淀,所以F中会产生砖红色沉淀。
变式训练2下列四种有机物的分子式都是C4H10O,其中不能被氧化为同碳原子数的醛的是( )
A.①②B.②③C.③④D.①④答案:D
1.CH3CH2OH分子中的氢原子的环境有( )A.1种B.2种C.3种D.6种答案:C解析:CH3CH2OH分子中—CH3上的3个氢原子等效,—CH2—中的氢原子等效,故分子中含有3种不同的氢原子,故选C。
2.用普通的工业酒精(含量约为96%)制取无水酒精的方法是( )A.蒸馏 B.加浓硫酸蒸馏C.加生石灰蒸馏D.加金属钠蒸馏答案:C解析:工业酒精中酒精与水易形成共沸混合物,不能直接蒸馏,故A错误;加浓硫酸蒸馏会生成乙醚、乙烯等物质,故B错误;工业酒精中酒精与水易形成共沸混合物,不能直接蒸馏,应加CaO,CaO与水反应后增大与乙醇的沸点差异,然后蒸馏可得到乙醇,故C正确;水、乙醇均能与金属钠反应,故D错误。
3.(双选)下列关于乙醇的说法正确的是( )A.乙醇在水溶液中不能电离,所以乙醇是非电解质B.乙醇结构中有—OH,所以乙醇显碱性C.乙醇分子中只有羟基上的氢原子可被钠置换出来D.常温下,1 ml乙醇可与足量的Na反应生成11.2 L H2答案:AC解析:乙醇在水溶液中不能电离,乙醇是非电解质,故A正确;乙醇的水溶液为中性,故B错误;乙醇分子中羟基上的氢原子比烃基上的氢原子活泼,羟基上的氢原子可被钠置换出来,故C正确;1 ml乙醇可与足量的Na反应生成0.5 ml H2,在常温下体积不是11.2 L,故D错误。
4.分子式为C4H10O且能与乙酸发生酯化反应的有机物有 ( )A.2种B.3种C.4种D.5种答案:C解析:分子式为C4H10O且能与乙酸发生酯化反应,说明分子中含有—OH,该物质为丁醇,丁醇的同分异构体的种数与丁基或者丁烷的1-氯取代物的种数一样,故答案为C。
5.如图是A分子的球棍模型和B分子的填充模型,回答下列问题:(1)A和B的关系是 。 (2)写出A分子在催化剂存在条件下加热时和氧气反应的化学方程式: 。 (3)写出B分子和金属钠反应的化学方程式: 。 (4)B在加热条件下能够与HBr发生反应生成溴乙烷,该反应类型是 。
高中化学第1节 原子结构与元素性质图文课件ppt: 这是一份高中化学第1节 原子结构与元素性质图文课件ppt,共45页。PPT课件主要包含了电子数,质子数,质量数,中子数,相对原子质量,点击右图进入等内容,欢迎下载使用。
鲁科版 (2019)必修 第二册第3章 简单的有机化合物第3节 饮食中的有机化合物图片ppt课件: 这是一份鲁科版 (2019)必修 第二册第3章 简单的有机化合物第3节 饮食中的有机化合物图片ppt课件,共46页。PPT课件主要包含了CO2+3H2O,②催化氧化,由黑变红,刺激性,2与金属钠反应,无色无味,淡蓝色等内容,欢迎下载使用。
高中化学鲁科版 (2019)必修 第二册第3节 饮食中的有机化合物评课课件ppt: 这是一份高中化学鲁科版 (2019)必修 第二册第3节 饮食中的有机化合物评课课件ppt,共44页。PPT课件主要包含了无色透明,任意比互溶,CH3CH2OH,刺激性,无色气泡,乙醇的催化氧化反应,点击右图进入等内容,欢迎下载使用。













