





初中化学第九单元 溶液课题2 溶解度教案配套课件ppt
展开【思考】同学们你们能简单的猜测一下这些美丽的盐花是如何形成的吗?上节课我们已经学过了氯化钠能溶于水中,但是它能无限的溶解在水中吗?溶解和盐花的形成又有什么关系呢?让我们一起走进课题2 溶解度来揭晓这些答案吧!
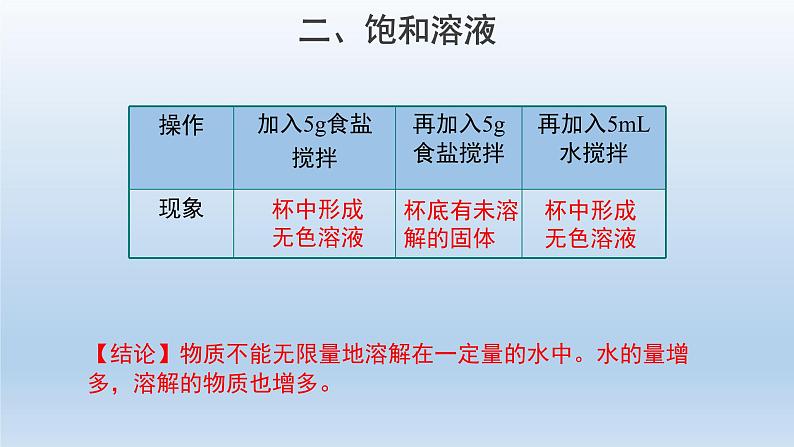
【活动探究1】在常温下,取大约20 mL水倒入玻璃杯中,加入5 g食盐, 搅拌,等食盐溶解后,再加5g,搅拌,观察现象。然后再加入5mL水,搅拌,观察现象。
【结论】物质不能无限量地溶解在一定量的水中。水的量增多,溶解的物质也增多。
【活动探究2】在常温下,取大约20mL水倒入玻璃杯中,加入5g硝酸钾,搅拌,等硝酸钾溶解后,再加5g,搅拌……加了几次后,烧杯中的硝酸钾固体才有剩余而不再溶解?然后加热,观察现象。再加5g硝酸钾,观察现象。等溶液冷却后,又有什么现象发生?
【结论】温度升高,一定量的水中可以溶解更多的物质;温度降低,一定量的水中溶解的物质的质量减少。
【小结】溶剂中溶解溶质的多少与溶剂的量和温度有关。
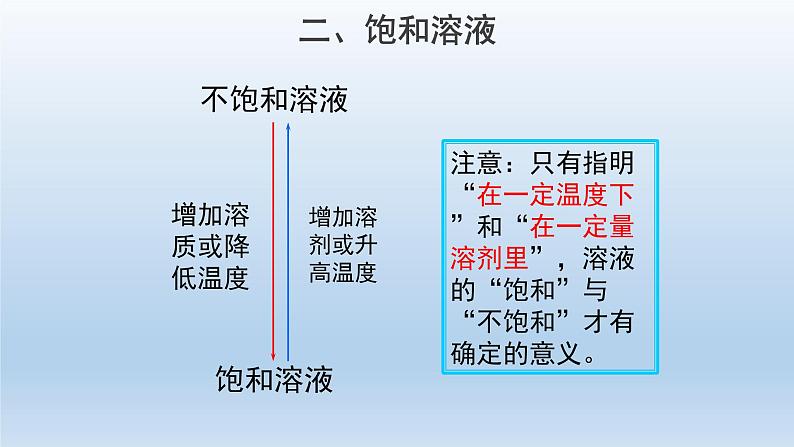
【饱和溶液】在一定温度下,在一定量的溶剂里不能再溶解某种溶质的溶液,叫做这种溶质的饱和溶液。
【不饱和溶液】在一定温度下,在一定量的溶剂里还能继续溶解某种溶质的溶液,叫做这种溶质的不饱和溶液。
注意:只有指明“在一定温度下”和“在一定量溶剂里”,溶液的“饱和”与“不饱和”才有确定的意义。
【结晶】溶解在溶液里的溶质以晶体的形式析出,叫做结晶。
只有在温度确定、溶剂的量也确定的条件下才能作出比较。
【溶解度】在一定温度下,某固体物质在100g溶剂里达到饱和状态时所溶解的质量。
说明:通常所说的溶解度是指物质在水里的溶解度。
【思考】食盐和硝酸钾都可以溶解在水中,那么,到底谁溶得更多呢?
四大要素: 1 . 一定温度; 2 . 100克溶剂; 3 . 饱和状态; 4 . 指溶质的质量。
如:在20℃时,100g水中溶解36g氯化钠达到饱和,我们就说20℃时,氯化钠的溶解度是36g。
又如:60℃时,硝酸钾的溶解度是110克,说明在60℃时,100g水里最多能溶解110g硝酸钾。
【思考】理解了溶解度的概念,那你了解平时所说的“易溶”、“难溶”与溶解度的关系吗?
同种溶质在不同的溶 剂中的溶解能力不同
不同的溶质在同种溶 剂中的溶解能力不同
易溶 、可溶 、 微溶 、难(不)溶
1 .测定20 ℃时硝酸钾在水中的溶解度时,所用的溶液一定是20 ℃时硝酸钾的( )A.浓溶液 B .稀溶液 C .饱和溶液 D .不饱和溶液2 .把室温下的不饱和食盐水变成饱和溶液,最好的方法是( )A .蒸发水 B .加食盐 C .给溶液降温 D .给溶液升温
3.20 ℃时,食盐的溶解度是36 g,它的含义是( )A.20 ℃时,136 g饱和食盐水中含有36 g食盐 B.100 g水中最多溶解36 g食盐C.20 ℃时,饱和食盐水中含有36 g食盐D.20 ℃时,100 g饱和食盐水中含有36 g食盐
人教版九年级下册第九单元 溶液课题2 溶解度授课ppt课件: 这是一份人教版九年级下册第九单元 溶液课题2 溶解度授课ppt课件,共60页。PPT课件主要包含了归纳总结一,归纳总结二,归纳总结三,归纳总结四,溶解度第一课时,溶解度,应该在同一温度下,这样行吗,应该溶剂的量相同,应该达到饱和状态等内容,欢迎下载使用。
初中人教版课题2 溶解度背景图课件ppt: 这是一份初中人教版课题2 溶解度背景图课件ppt,共37页。PPT课件主要包含了饱和溶液,浓溶液与稀溶液,不一定,注结晶的方法,蒸发结晶蒸发溶剂,贮水池,蒸发池,结晶池,氯化钠,多种化工原料等内容,欢迎下载使用。
初中化学人教版九年级下册第九单元 溶液课题2 溶解度背景图课件ppt: 这是一份初中化学人教版九年级下册第九单元 溶液课题2 溶解度背景图课件ppt,共60页。PPT课件主要包含了情境引入,你吃“饱”了没,与情绪有关,与体型有关,饱和溶液,饱和溶液和不饱和溶液,课堂练习,饱和溶液的状态,生活小常识,海水晒盐等内容,欢迎下载使用。













