





人教版 (2019)必修 第一册第二节 氯及其化合物课文内容课件ppt
展开氯气是有毒物质,那么游泳馆为什么会有氯气呢?
氯气的发现应归功于瑞典化学家舍勒。舍勒是18世纪中后期欧洲的一位著名的科学家。舍勒发现氯气是在1774年,当时他正在研究软锰矿(即二氧化锰),当他使软锰矿与浓盐酸混合并加热时,产生了一种有刺激性气味的气体,这种气体就是氯气。
氯气是黄绿色有刺激性气味的气体,有毒,可溶于水,易液化,密度大于空气
遇氯气泄漏时,人员应该迅速撤离至上风处,且尽量居于较高位置
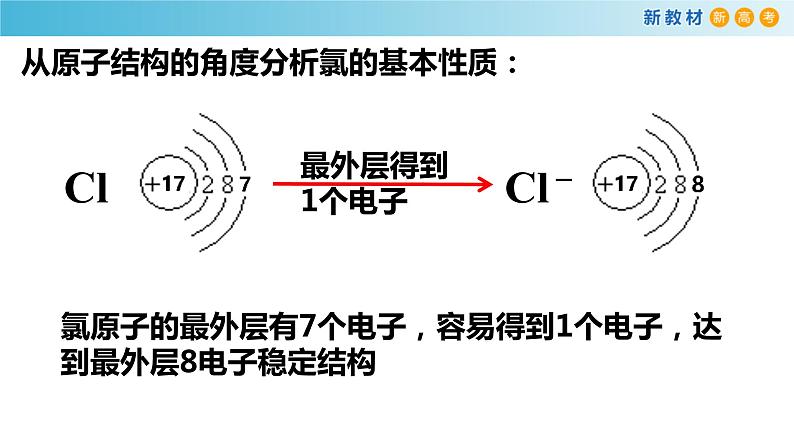
从原子结构的角度分析氯的基本性质:
氯原子的最外层有7个电子,容易得到1个电子,达到最外层8电子稳定结构
氯气是黄绿色有刺激性气味的气体,有毒,可溶于水,易液化,密度大于空气
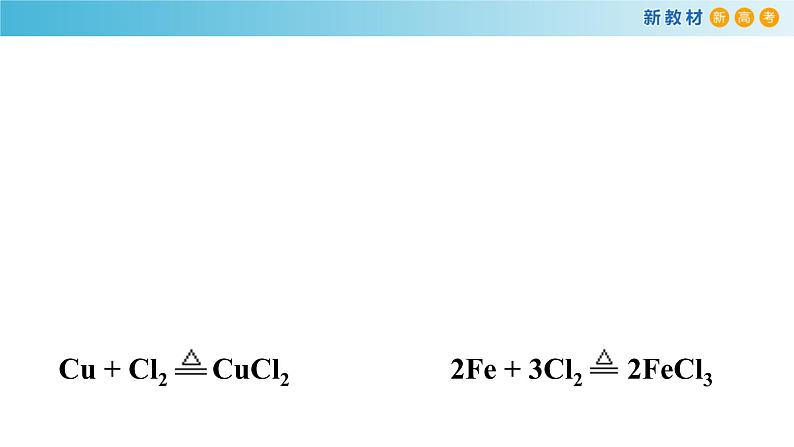
氯气能与大多数金属化合生成金属氯化物,如果金属有变价,一般得到高价态氯化物
实验2-7:氢气在氯气中燃烧
在空气中点燃氢气,将导管深入盛有氯气的集气瓶中,观察现象。
氢气在氯气中安静的燃烧,发出苍白色火焰,生成的HCl气体在集气瓶口与空气中的水蒸气结合,形成白雾。
工业制HCl,溶于水得到盐酸
什么是燃烧?燃烧的条件是什么?
燃烧是指物质与氧气发生的剧烈的发光发热的化学反应,燃烧的条件是:物质与氧气接触,达到着火点
氢气能在氯气中燃烧,说明燃烧不一定需要氧气
燃烧是指物质与氧化剂发生的剧烈的发光发热的氧化还原反应,燃烧的条件是:物质与氧化剂接触,达到着火点
氯气溶解度约为1:2,氯气溶于水得到的就是氯水。那么氯气溶于水时是否和水发生了化学反应呢?
向试管中加入一定量的氯水,滴加硝酸银溶液观察现象
向氯水中滴加硝酸银观察到有白色沉淀,这说明氯水有一定量的氯离子,从而证明了氯气溶于水的时候应该与水发生了反应
氯气溶于水时,部分氯气会与水反应
Cl2 + H2O = HCl + HClO
HClO是次氯酸,是一元弱酸,具有强氧化性,能够杀死水中的病菌起到消毒的作用,因此很多自来水厂会用氯气消毒杀菌
游泳馆为什么会有氯气呢?
用氯气对游泳池内的水进行消毒
有科学家提出,用氯气进行自来水消毒时会产生对人体有害的有机氯化物
国家规定了自来水中余氯含量的标准,同时也在积极研究新型自来水消毒剂(ClO2、O3等)
向分别装有干燥红色布条和湿润红色布条的试剂瓶中通入氯气,观察现象
干燥布条保持红色,而湿润布条的红色褪去,这是因为氯气与水反应生成的次氯酸具有强氧化性,能使某些染料和有机色素褪色,因此次氯酸可以做为漂白剂使用
过氧化钠为什么有漂白性?
为什么不使用次氯酸直接作为消毒剂,而是使用氯气消毒呢?
次氯酸光照下分解,所以将其转化为较稳定的物质再作为漂白剂。
根据氯气与水的反应,写出氯气与氢氧化钠溶液反应的化学方程式,改写为离子方程式,并用双线桥分析
Cl2 + 2NaOH= NaCl + NaClO + H2O
Cl2 + 2OH- = Cl- + ClO- + H2O
将氯气通入氢氧化钠溶液会得到氯化钠和次氯酸钠的混合溶液,这样的混合溶液称为漂白液,其有效成分为NaClO。
根据上面的反应,写出氯气与氢氧化钙溶液反应的方程式
2Cl2 + 2Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2H2O
将氯气通入冷的石灰乳中会得到以次氯酸钙为有效成分的漂白粉,氯气与氢氧化钙充分反应使次氯酸钙成为主要成分,就得到了漂粉精
次氯酸盐比次氯酸的稳定性强很多,同时次氯酸盐可以在溶液中转化为次氯酸,从而具有一定的漂白和消毒能力,所以漂白液、漂白粉、漂粉精都是常用的消毒剂和漂白剂
高中化学第二节 氯及其化合物说课ppt课件: 这是一份高中化学第二节 氯及其化合物说课ppt课件,共41页。PPT课件主要包含了核心素养发展目标,氯气的性质,化学性质,物理性质,黄绿色气体,刺激性,溶解性,能溶于水12,原子结构,非金属单质等内容,欢迎下载使用。
高中化学必修一 专题2.2.1 氯气的性质: 这是一份高中化学必修一 专题2.2.1 氯气的性质,共23页。
高中化学必修一 2.2.1 氯气的性质课件: 这是一份高中化学必修一 2.2.1 氯气的性质课件,共20页。













